Moment dipolowy jest jednym z kluczowych pojęć opisujących zachowanie cząsteczek w polu elektrycznym, sposobu rozmieszczenia ładunku w wiązaniach chemicznych oraz natury oddziaływań międzycząsteczkowych. Choć jego definicja matematyczna wydaje się prosta, konsekwencje fizyczne i chemiczne są niezwykle rozległe – od wyjaśnienia, dlaczego woda ma tak nietypowe właściwości, po zrozumienie budowy białek, działania materiałów dielektrycznych i technik spektroskopowych stosowanych w nowoczesnych laboratoriach.
Podstawy fizyczne momentu dipolowego
W najbardziej ogólnym ujęciu moment dipolowy opisuje rozdzielenie ładunków elektrycznych w układzie. Jeśli dodatni i ujemny ładunek znajdują się w tym samym miejscu, układ nie ma momentu dipolowego. Jeżeli natomiast zostaną rozdzielone w przestrzeni, pojawia się wektorowy parametr określany jako moment dipolowy, zwykle oznaczany symbolem μ. Jest on definiowany jako iloczyn wielkości ładunku oraz wektora od ładunku ujemnego do dodatniego.
W chemii interesuje nas przede wszystkim moment dipolowy cząsteczek. Nawet gdy cząsteczka jako całość jest elektrycznie obojętna, elektrony mogą być rozłożone nierównomiernie. Atomy o różnej elektroujemności przyciągają elektrony z różną siłą, co prowadzi do powstania częściowych ładunków: δ+ na mniej elektroujemnym atomie i δ− na bardziej elektroujemnym. W takim układzie wiązanie staje się spolaryzowane, a w skali całej cząsteczki może powstać makroskopowy moment dipolowy.
Jednostką momentu dipolowego w układzie SI jest kulomb razy metr (C·m), lecz w chemii znacznie wygodniejsza jest jednostka debye (D). Jeden debye odpowiada około 3,336 × 10⁻³⁰ C·m. Typowe cząsteczki polarnych związków organicznych mają momenty dipolowe rzędu 1–5 D, przy czym znane są zarówno mniejsze, jak i znacznie większe wartości w bardziej złożonych układach.
Moment dipolowy w cząsteczkach: struktura i elektronika
Cząsteczka będzie mieć trwały moment dipolowy, jeśli wektory poszczególnych wiązań polarnych nie znoszą się wzajemnie. Na wartość i kierunek momentu dipolowego wpływają: kształt cząsteczki, różnice elektroujemności, rozkład ładunku w układach sprzężonych oraz obecność wolnych par elektronowych. Nie jest więc wystarczająca sama obecność polarnych wiązań – konieczne jest także asymetryczne ułożenie tych wiązań w przestrzeni.
Przykład wody jako klasycznego dipola
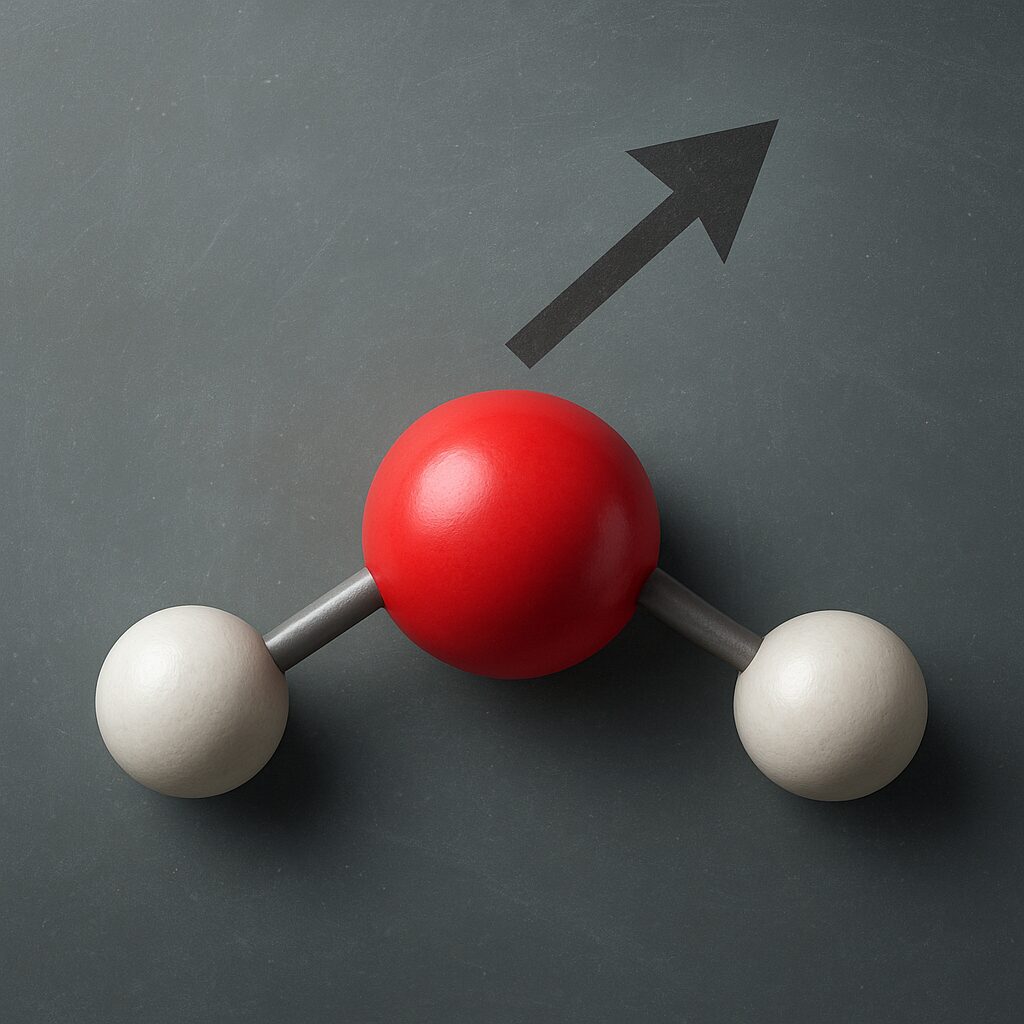
Woda jest najczęściej przytaczanym przykładem cząsteczki dipolowej. Dwa atomy wodoru są połączone z tlenem, który ma znacznie większą elektroujemność. Wiązania O–H są silnie spolaryzowane, a na atomie tlenu znajduje się para wolnych par elektronowych. Geometria cząsteczki H₂O jest zgięta (kąt około 104,5°), więc wektory momentów dipolowych wiązań nie wyzerowują się, lecz sumują wektorowo do niezerowego momentu dipolowego całości.
Właśnie dlatego cząsteczka wody jest intensywnie polarna, z momentem dipolowym około 1,85 D. Odpowiada to za silne oddziaływania dipol–dipol oraz powstawanie wiązania wodorowego między cząsteczkami wody, co skutkuje wysokim ciepłem parowania, znaczną lepkością oraz nieprzeciętnie wysoką temperaturą wrzenia w porównaniu z innymi związkami o podobnej masie cząsteczkowej.
Cząsteczki liniowe i symetria
Nie wszystkie cząsteczki o polarnych wiązaniach są dipolowe. Dwutlenek węgla, CO₂, ma każde wiązanie C=O spolaryzowane; tlen jest bardziej elektroujemny niż węgiel, więc powstają częściowe ładunki δ− przy atomach tlenu i δ+ przy atomie węgla. Jednak cząsteczka CO₂ jest liniowa, a dwa identyczne wektory dipolowe ustawione są w przeciwnych kierunkach. Ich suma wynosi zero, co oznacza, że całkowity moment dipolowy cząsteczki CO₂ jest równy zero.
Symetria odgrywa zatem kluczową rolę. Cząsteczki o wysokiej symetrii, takie jak metan CH₄ (tetraedr), czterochlorek węgla CCl₄ czy benzen, może zawierać polaryzowane wiązania, ale ich geometryczne rozmieszczenie sprawia, że wektory momentu dipolowego znoszą się. Takie cząsteczki są formalnie niepolarne, mimo nierównomiernego lokalnego rozkładu gęstości elektronowej w pojedynczych wiązaniach.
Rola wolnych par elektronowych
Wolne pary elektronowe, szczególnie na atomach bardziej elektroujemnych (np. tlen, azot, fluor), wpływają na rozkład gęstości elektronowej i kształt cząsteczki. Według teorii VSEPR wolne pary zajmują więcej miejsca niż pary wiążące, co zniekształca geometrię i może zwiększyć lub zmniejszyć moment dipolowy.
Cząsteczka amoniaku, NH₃, ma strukturę piramidalną, z atomem azotu na szczycie i trzema atomami wodoru u podstawy. Wolna para elektronowa na azocie powoduje spłaszczenie kąta H–N–H i zwiększone odpychanie, a wektory momentów wiązań N–H sumują się do niezerowego momentu dipolowego (około 1,47 D). Gdyby cząsteczka miała geometrię idealnie płaską i symetryczną, moment dipolowy byłby zdecydowanie inny, a właściwości układu – odmienne.
Układy sprzężone i rezonans
W związkach organicznych z rozległym sprzężeniem π, takich jak aldehydy, ketony, estry czy amidy, ładunek często nie jest lokowany wyłącznie na jednym atomie. Struktury rezonansowe opisują sytuację, w której rzeczywista gęstość elektronowa jest rozmyta między kilkoma atomami. Oznacza to, że moment dipolowy wynika z uśrednionego rozkładu ładunku, a nie z prostego pola dwóch punktowych ładunków.
Przykładowo w grupie karbonylowej C=O duża elektroujemność tlenu powoduje znaczne przesunięcie elektronów, ale w amidach część gęstości z tlenu przechodzi na azot wskutek sprzężenia między orbitalami π. Zmienia się tym samym zarówno wielkość, jak i rozkład momentu dipolowego. Obecność takich efektów wpływa na polarność całych cząsteczek, ich rozpuszczalność, siłę oddziaływań międzycząsteczkowych i reaktywność chemiczną.
Polaryzowalność i dipole indukowane
Moment dipolowy można podzielić na trwały (stały) oraz indukowany. Trwały moment dipolowy istnieje w cząsteczce nawet bez zewnętrznego pola elektrycznego, wynika z wbudowanego, asymetrycznego rozkładu ładunków. Dipol indukowany pojawia się natomiast wtedy, gdy zewnętrzne pole elektryczne, jon lub inna polarna cząsteczka deformuje chmurę elektronową danego układu.
Stopień, w jakim cząsteczka ulega odkształceniu pod wpływem pola, opisuje polaryzowalność. Atomy i cząsteczki o luźniej związanych elektronach (np. duże atomy halogenów, jak jod) są silnie polaryzowalne, łatwo tworzą chwilowe dipole i uczestniczą w oddziaływaniach dyspersyjnych. Te zjawiska są ważne nie tylko dla fizycznych właściwości substancji, ale także dla mechanizmów reakcji w fazie skondensowanej.
Znaczenie chemiczne i fizyczne momentu dipolowego
Moment dipolowy ma bezpośredni wpływ na właściwości fizykochemiczne związków chemicznych. Określa on w dużej mierze siłę i charakter oddziaływań międzycząsteczkowych, a także warunkuje rozpuszczalność, temperatury wrzenia, topnienia, lepkość oraz wiele parametrów istotnych w zastosowaniach technologicznych, biologicznych i środowiskowych.
Oddziaływania dipol–dipol i wiązania wodorowe
Cząsteczki o trwałym momencie dipolowym oddziałują ze sobą poprzez przyciąganie między ich częściowo dodatnimi i częściowo ujemnymi fragmentami. Gdy dodatni koniec jednej cząsteczki zbliża się do ujemnego końca drugiej, powstają oddziaływania dipol–dipol. Choć są słabsze niż typowe wiązania kowalencyjne czy jonowe, ich suma w makroskopowej próbce jest znaczna i w wielu przypadkach dominuje nad innymi typami sił międzycząsteczkowych.
W szczególnym przypadku, gdy w cząsteczce występuje silnie spolaryzowane wiązanie z wodorem połączonym z bardzo elektroujemnym atomem (O–H, N–H, F–H), oraz gdy w sąsiedztwie znajduje się wolna para elektronowa na innym elektroujemnym atomie, powstaje wiązanie wodorowe. Jego natura jest mieszana: częściowo elektrostatyczna, częściowo kowalencyjna. Bez zrozumienia momentu dipolowego trudno zinterpretować siłę i kierunkowość wiązań wodorowych, odpowiedzialnych za struktury białek, kwasów nukleinowych i właściwości wody.
Moment dipolowy a rozpuszczalność
Jednym z podstawowych praktycznych skutków istnienia momentu dipolowego jest wpływ na rozpuszczalność związków. Polarne rozpuszczalniki, takie jak woda, metanol, etanol czy aceton, stabilizują jony oraz cząsteczki polarne, ustawiając swoje dipole tak, by zminimalizować energię układu. Zasada “podobne rozpuszcza podobne” wynika w znacznej mierze z energetycznych korzyści wynikających z dopasowania rozkładu ładunku.
Niepolarne rozpuszczalniki, takie jak heksan, benzen czy toluen, nie są w stanie efektywnie otaczać jonów ani silnie polarnych cząsteczek, więc rozpuszczalność takich substancji jest mała. Z kolei cząsteczki o umiarkowanym momencie dipolowym, ale z rozległym szkieletem węglowodorowym, często wykazują rozpuszczalność pośrednią, co jest szeroko wykorzystywane w projektowaniu nośników farmaceutycznych, detergentów i materiałów funkcjonalnych.
Temperatury wrzenia i topnienia
Silniejsze oddziaływania międzycząsteczkowe zwykle prowadzą do wyższych temperatur wrzenia i topnienia. Cząsteczki polarne z dużym momentem dipolowym silniej się przyciągają, wymagając większej ilości energii do ich rozdzielenia podczas przejścia fazowego. Dlatego związki o zbliżonej masie molowej, lecz różnym momencie dipolowym, mogą mieć istotnie różne parametry fizyczne.
Doskonałym przykładem jest porównanie wody (H₂O) i siarkowodoru (H₂S). Obie cząsteczki mają podobną strukturę ogólną (AX₂ z wolnymi parami), lecz różnią się elektroujemnością centralnego atomu i możliwością tworzenia wiązań wodorowych. Woda tworzy rozległą sieć takowych wiązań, co przekłada się na znacznie wyższą temperaturę wrzenia niż wynikałoby to z samej masy cząsteczki. H₂S, słabiej polarny i mniej skłonny do wiązań wodorowych, wrze przy dużo niższej temperaturze.
Moment dipolowy w chemii organicznej i biochemii
W złożonych cząsteczkach organicznych rozkład momentu dipolowego jest nierównomierny, a fragmenty polarnych grup (np. –OH, –NH₂, –COOH, –C=O, –SO₂–) mogą silnie oddziaływać z otoczeniem. W białkach grupy te determinują sposób fałdowania łańcucha polipeptydowego, zdolność tworzenia mostków solnych (między grupami zasadowymi i kwasowymi) oraz stabilność struktury drugorzędowej i trzeciorzędowej.
Błony komórkowe są z kolei zbudowane z fosfolipidów, które posiadają wyraźnie spolaryzowaną główkę hydrofilową i hydrofobowy ogon węglowodorowy. Moment dipolowy główki fosfolipidu warunkuje jej oddziaływanie z wodą i jonami, co przekłada się na przepuszczalność, ładunek powierzchniowy błony oraz jej zachowanie w polu elektrycznym. Kanały jonowe i receptory błonowe często wykorzystują lokalne pola elektrostatyczne, wynikające z rozkładu momentów dipolowych aminokwasów, do selektywnego transportu i sygnalizacji.
Znaczenie w materiałach i technologiach
Materiały dielektryczne, używane w kondensatorach i układach elektronicznych, są zbudowane z cząsteczek o określonym momencie dipolowym i polaryzowalności. W zewnętrznym polu elektrycznym ich dipole orientują się, co pozwala magazynować energię pola w materiale. Współczynnik przenikalności elektrycznej zależy od łatwości takiej orientacji oraz od wielkości chwilowych i trwałych momentów dipolowych.
W polimerach, takich jak poliamidy, poliuretany czy poliestery, rozmieszczenie polarnych grup w łańcuchu odpowiada za właściwości mechaniczne, adhezyjne i barierowe. W zastosowaniach takich jak ogniwa słoneczne, diody elektroluminescencyjne i sensory chemiczne stosuje się projektowanie cząsteczek o kontrolowanym rozkładzie ładunku, co pozwala precyzyjnie kształtować ich właściwości optyczne, elektronowe i transportowe.
Pomiar i obliczanie momentu dipolowego
Choć moment dipolowy jest pojęciem matematycznym, jego wartość można określić zarówno doświadczalnie, jak i teoretycznie. Rozwój spektroskopii, technik dielektrycznych oraz metod obliczeniowych pozwala na szczegółowe badanie rozkładu ładunku w cząsteczkach, także złożonych biologicznie i technologicznie istotnych.
Metody doświadczalne
Jedną z najstarszych metod wyznaczania momentu dipolowego jest badanie zmian przenikalności elektrycznej roztworu w funkcji stężenia i temperatury. Z teorii Debye’a wynika, że orientacja dipoli w polu elektrycznym wpływa na przenikalność, co pozwala wyznaczyć średni moment dipolowy rozpuszczonych cząsteczek. Metoda ta jest szczególnie przydatna dla małych i średnich cząsteczek organicznych.
Spektroskopia rotacyjna w zakresie mikrofalowym jest z kolei niezwykle dokładna w przypadku cząsteczek gazowych. Linie rotacyjne są bezpośrednio związane z momentem bezwładności i rozkładem ładunku, więc analiza widma pozwala określić strukturę geometryczną i moment dipolowy z wyjątkową precyzją. Brazowanie momentu dipolowego poprzez obserwację intensywności linii w polu elektrycznym stanowi jedną z podstaw tej metody.
W spektroskopii IR i Ramana, choć głównym celem jest obserwacja drgań cząsteczek, pojawianie się lub zanikanie pasm w widmie jest powiązane ze zmiennością momentu dipolowego w trakcie drgań. Dzięki temu można pośrednio wnioskować o polaryzacji wiązań, ich symetrii i rozkładzie ładunku.
Techniki komputerowe i chemia kwantowa
Metody chemii kwantowej, takie jak teoria funkcjonału gęstości (DFT) czy obliczenia ab initio (np. HF, MP2, Coupled Cluster), umożliwiają wyznaczenie momentu dipolowego na podstawie rozkładu gęstości elektronowej. Oblicza się całkę ładunku pomnożoną przez wektor położenia, uzyskując wektor momentu dipolowego cząsteczki w danej geometrii optymalnej.
Choć wyniki obliczeń zależą od użytego poziomu teorii i zestawu funkcji bazowych, nowoczesne metody pozwalają uzyskać bardzo dobrą zgodność z eksperymentem. Dla wielu związków obliczony moment dipolowy różni się od zmierzonego o kilka procent, co jest akceptowalne z punktu widzenia projektowania nowych cząsteczek o określonych właściwościach. W dziedzinach takich jak modelowanie leków, materiały organiczne dla elektroniki czy kataliza, obliczanie momentu dipolowego stało się rutynowym etapem analizy.
W symulacjach dynamiki molekularnej moment dipolowy poszczególnych cząsteczek lub grup jest używany przy wyznaczaniu sił elektrostatycznych w układzie. Takie symulacje odtwarzają ruch atomów w czasie, umożliwiając badanie przewodnictwa jonowego, struktury wody hydratacyjnej wokół białek czy zachowania elektrolitów w porach nanostruktur. Dokładny opis dipoli jest niezbędny do realistycznego odwzorowania właściwości makroskopowych.
Momenty wielobiegunowe i uogólnienia
Moment dipolowy jest pierwszym niezerowym wyrazem rozwinięcia multipolowego rozkładu ładunku. Kiedy rozważamy układy bardziej złożone, pojawiają się również momenty kwadrupolowe, oktupolowe i wyższe. W praktyce dla większości zastosowań chemicznych wystarczający jest opis z wykorzystaniem monopolu (ładunku całkowitego) i dipola, ale w precyzyjnych obliczeniach oddziaływań między złożonymi cząsteczkami uwzględnia się także moment kwadrupolowy.
W przypadku cząsteczek, które nie mają trwałego momentu dipolowego, jak CO₂ czy benzen, moment kwadrupolowy może być znaczący i wpływać na oddziaływania międzycząsteczkowe w kryształach czy w fazie ciekłej. Opis taki jest szczególnie ważny w chemii ciała stałego, w projektowaniu materiałów krystalicznych oraz w analizie oddziaływań w sieciach supramolekularnych.
Moment dipolowy w perspektywie interdyscyplinarnej
Pojęcie momentu dipolowego, choć zakorzenione w chemii fizycznej, ma znaczenie wykraczające daleko poza klasyczne granice dyscypliny. Łączy elektrodynamikę, fizykę materii skondensowanej, biologię molekularną, inżynierię materiałową i nauki środowiskowe, tworząc wspólny język do opisu zjawisk związanych z rozmieszczeniem ładunku w materii.
Elektrostatyka w biologii
W układach biologicznych lokalne pola elektryczne powstają z sumy momentów dipolowych aminokwasów, grup funkcyjnych, ligandów i jonów. Enzymy wykorzystują te pola do stabilizacji stanów przejściowych reakcji, obniżając w ten sposób energię aktywacji. Wiele miejsc aktywnych ma zaaranżowany rozkład ładunków, który kieruje substrat w odpowiednią orientację, wzmacniając dany kierunek przepływu elektronów lub protonów.
Błony komórkowe, zawierające asymetrycznie rozmieszczone lipidy i białka, wykazują potencjał błonowy – różnicę potencjału elektrycznego po obu stronach. Choć jest on tworzony głównie przez dystrybucję jonów, momenty dipolowe białek i lipidów wpływają na lokalne pole, kształtując warunki, w jakich pracują kanały jonowe, pompy protonowe i inne elementy układu transportowego.
Moment dipolowy a spektroskopia i obrazowanie
W spektroskopii dielektrycznej bada się odpowiedź materiału na zmienne pole elektryczne. Zależność stałej dielektrycznej od częstotliwości dostarcza informacji o ruchliwości dipoli, ich czasie relaksacji i interakcjach z otoczeniem. W wodzie, elektrolitach i roztworach białek analiza ta ujawnia złożone procesy relaksacyjne, związane z tworzeniem i zrywaniem wiązań wodorowych oraz z ruchem jonów w polu.
Techniki takie jak NMR (rezonans magnetyczny jądrowy) wykorzystują wprawdzie głównie momenty magnetyczne jąder, ale chemiczne przesunięcia częstotliwości i stałe sprzężenia często korelują z polaryzacją wiązań i lokalnym rozkładem ładunku. W połączeniu z obliczeniami kwantowymi pozwala to wnioskować o wartościach momentu dipolowego i o jego zmianach podczas reakcji chemicznych czy zjawisk asocjacji.
Środowisko i chemia atmosfery
W chemii atmosfery moment dipolowy drobnych cząsteczek i aerozoli wpływa na ich zdolność do kondensacji pary wodnej, absorpcji promieniowania i oddziaływania z jonami. Cząsteczki o dużym momencie dipolowym, powstające w procesach spalania lub reakcji fotochemicznych, mogą pełnić rolę jąder kondensacji chmur, zmieniając własności optyczne atmosfery i bilans radiacyjny Ziemi.
Reaktywność gazów cieplarnianych, takich jak H₂O, CO₂, CH₄, N₂O czy cząsteczek halogenowanych, także jest częściowo determinowana przez ich rozkład ładunku. Moment dipolowy wpływa na przekroje czynne w zderzeniach, szybkości reakcji fotolizy i absorpcji promieniowania w zakresie podczerwonym. Zrozumienie tych zależności jest kluczowe dla wiarygodnych modeli klimatycznych.
Projektowanie molekuł funkcjonalnych
W chemii materiałowej i nanotechnologii moment dipolowy jest jednym z parametrów projektowych. Inżynierowie molekularni tworzą cząsteczki o określonym rozkładzie ładunku, aby uzyskać pożądane własności: przewodnictwo, luminescencję, zdolność samoorganizacji na powierzchniach czy selektywne wiązanie jonów i cząsteczek gościnnych. W supramolekularnej chemii host–guest dopasowanie kształtu i pola elektrostatycznego jest równie ważne jak dopasowanie rozmiaru.
W dziedzinie farmacji moment dipolowy wpływa na rozpuszczalność i dystrybucję leków w organizmie. Zbyt polarna cząsteczka trudno przenika przez błony lipidowe, ale rozpuszcza się dobrze we krwi; zbyt niepolarna – ma słabą biodostępność i może kumulować się w tkankach tłuszczowych. Projektowanie leków wymaga więc kompromisu między polarnością a lipofilnością, wyrażaną często w parametrach takich jak logP, co jest pośrednio związane z sumarycznym momentem dipolowym i jego rozkładem.
FAQ
Czy każda cząsteczka z polarnym wiązaniem ma moment dipolowy?
Nie. Samo istnienie polarnych wiązań nie gwarantuje niezerowego momentu dipolowego. Decydująca jest geometria cząsteczki i symetria rozmieszczenia wiązań. Przykładowo CO₂ ma dwa silnie spolaryzowane wiązania C=O, ale jest liniowy – wektory momentów wiązań dokładnie się znoszą. Podobnie CCl₄ zawiera polaryzowane wiązania C–Cl, lecz symetria tetraedryczna sprawia, że suma wektorowa momentów jest równa zero.
Jak moment dipolowy wpływa na temperaturę wrzenia substancji?
Im większy moment dipolowy, tym silniejsze są oddziaływania dipol–dipol między cząsteczkami. Aby doprowadzić do wrzenia, trzeba je pokonać, co wymaga dostarczenia większej energii. Dlatego związki o zbliżonej masie molowej, lecz większym momencie dipolowym, mają zwykle wyższe temperatury wrzenia. Wyjątkowo silne podwyższenie obserwuje się przy obecności wiązań wodorowych, jak w wodzie, alkoholach czy kwasach karboksylowych.
W jaki sposób można zmierzyć moment dipolowy cząsteczki?
Doświadczalnie moment dipolowy wyznacza się głównie poprzez pomiar własności dielektrycznych roztworów lub analizę widm spektroskopowych. W metodach dielektrycznych bada się zależność przenikalności elektrycznej od stężenia i temperatury. W spektroskopii rotacyjnej mierzy się położenie i intensywność linii mikrofalowych, które są czułe na rozkład ładunku. Z pomocą odpowiednich modeli teoretycznych pozwala to obliczyć wartość momentu dipolowego.
Jaka jest różnica między trwałym a indukowanym momentem dipolowym?
Trwały moment dipolowy wynika z wewnętrznej budowy cząsteczki – różnic elektroujemności, geometrii i obecności wolnych par elektronowych. Istnieje nawet bez zewnętrznego pola. Indukowany moment dipolowy pojawia się dopiero wtedy, gdy zewnętrzne pole elektryczne, jon lub inna polarna cząsteczka deformuje chmurę elektronową. Jego wartość zależy od polaryzowalności układu i znika po usunięciu czynnika indukującego z otoczenia.
Dlaczego moment dipolowy jest tak ważny w biochemii i farmacji?
Moment dipolowy decyduje o tym, jak cząsteczki oddziałują z wodą, błonami komórkowymi, białkami i kwasami nukleinowymi. W biochemii wpływa na fałdowanie białek, stabilność kompleksów enzym–substrat i specyficzność wiązania ligandów. W farmacji polarność leku określa jego rozpuszczalność w płynach ustrojowych, przenikalność przez błony lipidowe i sposób wiązania z receptorami. Odpowiedni rozkład ładunku jest więc kluczowy dla skuteczności i bezpieczeństwa terapii.