Przemiana izobaryczna to jeden z podstawowych typów przemian termodynamicznych, w których ciśnienie pozostaje stałe, a zmieniają się inne parametry stanu, takie jak objętość, temperatura i energia wewnętrzna. Zrozumienie jej natury pozwala wyjaśnić działanie silników cieplnych, turbin gazowych, procesów atmosferycznych oraz zjawisk zachodzących w instalacjach przemysłowych. Znajomość przemiany izobarycznej jest kluczowa zarówno w fizyce, jak i w inżynierii chemicznej, energetyce oraz meteorologii.
Podstawy teoretyczne przemiany izobarycznej
Przemiana izobaryczna to taka, która przebiega przy stałym ciśnieniu zewnętrznym działającym na układ. W opisie termodynamicznym oznacza to, że w trakcie rozpatrywanej zmiany stanów spełniony jest warunek p = const. Parametr p opisuje nacisk siły na jednostkę powierzchni, a jego niezmienność pozwala znacząco uprościć analizę zjawiska. W praktyce wykonanie idealnie izobarycznego procesu wymaga, aby układ był połączony z dużym zbiornikiem ciśnienia, który nie zmienia swojego stanu mimo wymiany energii.
W termodynamice klasycznej stan gazu opisuje się zazwyczaj za pomocą wielkości p, V, T oraz liczby moli n. Dla gazu doskonałego te wielkości powiązane są równaniem stanu pV = nRT, gdzie R to uniwersalna stała gazowa. Jeśli ciśnienie jest stałe, zmiana temperatury musi prowadzić do proporcjonalnej zmiany objętości, co wynika bezpośrednio z przytoczonego równania. Innymi słowy, w przemianie izobarycznej T jest wprost proporcjonalna do V przy niezmiennym n.
Matematycznie można to zapisać jako V/T = const, o ile liczba cząsteczek gazu się nie zmienia. To wyrażenie bywa utożsamiane z prawem Gay-Lussaca, jednym z klasycznych praw gazowych. Dla gazów rzeczywistych zależność ta jest jedynie przybliżeniem, ważnym dla niezbyt wysokich ciśnień i niezbyt niskich temperatur. Odchylenia od idealności opisuje się wtedy za pomocą współczynnika ściśliwości lub bardziej złożonych równań stanu, takich jak równanie van der Waalsa.
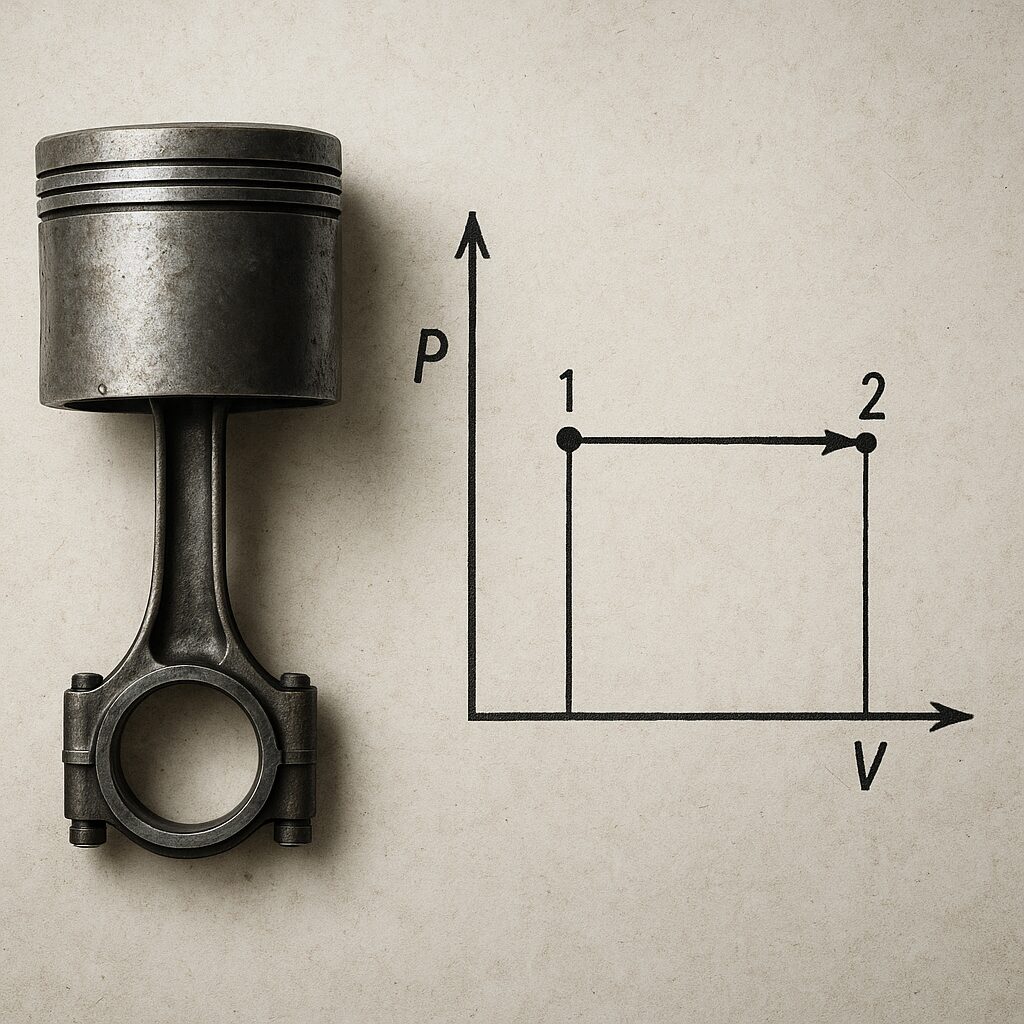
W opisach dydaktycznych przemiana izobaryczna jest często przedstawiana na wykresach p–V i V–T. Na wykresie p–V ma ona postać linii poziomej, na której kolejne punkty odpowiadają różnym parom V i T, ale temu samemu p. Na wykresie V–T będzie to natomiast linia prosta wychodząca z punktu odpowiadającego zeru bezwzględnemu, jeśli przyjmujemy model gazu idealnego. Taka wizualizacja pomaga intuicyjnie zrozumieć, jak rozszerza się lub kurczy gaz w zależności od temperatury przy stałym ciśnieniu.
Istotnym elementem teorii jest również rozróżnienie między energią wewnętrzną a entalpią. Dla gazu doskonałego energia wewnętrzna zależy jedynie od temperatury, natomiast entalpia H = U + pV jest wygodną wielkością termodynamiczną właśnie w przemianach izobarycznych. Zmiana entalpii dH w warunkach p = const odpowiada wprost ilości ciepła dostarczonego do układu lub odprowadzonego z niego, co jest fundamentem bilansów energetycznych dla procesów izobarycznych.
Równania, praca i ciepło w przemianie izobarycznej
W opisie ilościowym przemiany izobarycznej kluczowe znaczenie mają równania wiążące wykonana pracę, wymienione ciepło oraz zmiany funkcji stanu. Załóżmy, że analizujemy układ będący gazem doskonałym. Podczas izobarycznego rozszerzania się gazu wykonuje on pracę przeciwko zewnętrznemu ciśnieniu. Jeśli objętość zwiększa się z V₁ do V₂, praca mechaniczna dana jest prostym wyrażeniem W = p (V₂ − V₁). Ponieważ p jest stałe, można tu traktować je jako czynnik wyłączony przed nawias.
Interpretacja fizyczna tej pracy jest intuicyjna: układ wypiera tłok, podnosi ciężarki, napędza maszynę lub generuje przepływ. W przypadku sprężania izobarycznego praca ma znak ujemny z punktu widzenia układu, co oznacza, że to otoczenie wykonuje pracę nad gazem. Bilans energii wewnętrznej opisuje pierwsza zasada termodynamiki: dU = δQ − δW, gdzie δQ jest ciepłem, a δW pracą przekazaną na zewnątrz. Dla procesu izobarycznego szczególnie wygodne okazuje się zastąpienie energii wewnętrznej entalpią.
Wielkość entalpia definiuje się jako H = U + pV. Jeśli ciśnienie jest stałe, różniczka dH przyjmuje postać dH = dU + p dV, przy założeniu, że zmiany ciśnienia są zaniedbywalne. Podstawiając z pierwszej zasady termodynamiki, otrzymujemy dH = δQ + V dp. Gdy dp = 0, upraszcza się to do relacji dH = δQ. Z tego wynika, że w przemianie izobarycznej ciepło dostarczone do gazu równa się zmianie jego entalpii. Jest to niezwykle praktyczne w obliczeniach cieplnych, gdyż pozwala bezpośrednio powiązać bilans energetyczny z mierzalnymi parametrami, takimi jak temperatura.
Dla gazu doskonałego entalpia zależy wyłącznie od temperatury, a jej zmiana wyraża się poprzez ciepło właściwe przy stałym ciśnieniu cₚ. Mamy więc ΔH = n cₚ (T₂ − T₁). Zastępując ΔH ilością dostarczonego ciepła Q w procesie izobarycznym, otrzymujemy równanie Q = n cₚ (T₂ − T₁). Jest ono jednym z podstawowych narzędzi analizy przemian termodynamicznych w inżynierskiej praktyce. Współczynnik cₚ, specyficzny dla danego gazu lub mieszaniny, często można znaleźć w tablicach, co czyni obliczenia prostymi i przejrzystymi.
Kolejnym istotnym elementem analizy jest powiązanie ciepła właściwego przy stałym ciśnieniu cₚ z ciepłem właściwym przy stałej objętości cᵥ. Dla gazu idealnego zachodzi związek cₚ − cᵥ = R, gdzie R jest stałą gazową w przeliczeniu na mol. Wprowadza się ponadto bezwymiarowy współczynnik κ = cₚ/cᵥ. Choć κ odgrywa szczególnie ważną rolę w przemianach adiabatycznych, jego znajomość jest także przydatna przy bardziej złożonych cyklach, w których fazy izobaryczne przeplatają się z innymi typami przemian, na przykład izochorycznymi lub izotermicznymi.
W obliczeniach praktycznych często rozpatruje się tzw. sprawność procesów, czyli stosunek uzyskanej pracy do dostarczonego ciepła. Dla pojedynczej przemiany izobarycznej sprawność mechaniczna nie ma bezpośredniego ogólnego wyrażenia, ponieważ praca W zależy od różnicy objętości, a ciepło Q od różnicy temperatur. Jednak w obrębie całych cykli termodynamicznych, takich jak cykl Braytona czy cykl Otta wzbogacony o odcinki izobaryczne, relacje między Q i W nabierają kluczowego znaczenia. Przemiana izobaryczna staje się tam jednym z etapów determinujących ilość pozyskiwanej energii użytkowej.
Istotne jest również uwzględnienie odchyleń od zachowania idealnego. Przy wysokich ciśnieniach lub niskich temperaturach, kiedy cząsteczki gazu silnie ze sobą oddziałują, równanie pV = nRT przestaje być dokładne, a ciepła właściwe mogą zależeć nie tylko od temperatury, lecz także od ciśnienia. W takich przypadkach używa się tabel termodynamicznych, równań empirycznych albo metod numerycznych, by prawidłowo oszacować zarówno ciepło wymienione w procesie izobarycznym, jak i wykonaną pracę. Przemiana nadal jest izobaryczna w sensie praktycznym, ale jej opis wymaga bardziej wyrafinowanych narzędzi.
Zastosowania przemiany izobarycznej w technice, przyrodzie i badaniach naukowych
Przemiana izobaryczna ma ogromne znaczenie praktyczne, ponieważ wiele rzeczywistych procesów zachodzi przy w przybliżeniu stałym ciśnieniu, zwłaszcza w otwartej atmosferze. Jednym z najprostszych przykładów jest podgrzewanie lub chłodzenie powietrza atmosferycznego bez zmiany wysokości. Ponieważ ciśnienie atmosferyczne na danym poziomie jest niemal niezmienne w krótkich skalach czasu, zmiany temperatury prowadzą głównie do zmiany gęstości i objętości powietrza. Tak powstają prądy konwekcyjne, których podstawą jest właśnie rozszerzanie się gazu w warunkach quasi-izobarycznych.
W meteorologii analiza takich zjawisk wykorzystuje pojęcia energii potencjalnej i stabilności atmosfery. Gdy powietrze ogrzewa się przy stałym ciśnieniu, jego entalpia rośnie. Rozszerzające się powietrze staje się lżejsze od otoczenia i zaczyna się unosić. Procesy te są ważnym składnikiem cyrkulacji atmosferycznej, powstawania chmur i burz. Modele numeryczne klimatu uwzględniają szereg przemian izobarycznych i zbliżonych do izobarycznych, na przykład w warstwach o określonej ciśnieniowej strukturze, gdzie stosuje się tzw. układ współrzędnych ciśnienia zamiast klasycznego układu wysokościowego.
W technice energetycznej jednym z kluczowych zastosowań przemiany izobarycznej jest praca turbin gazowych oraz silników odrzutowych. W klasycznym opisie cyklu Braytona znajduje się etap podgrzewania sprężonego powietrza w komorze spalania przy niemal stałym ciśnieniu. Dostarczane jest tam ciepło poprzez spalanie paliwa, a wzrost temperatury powoduje istotne zwiększenie objętości i energii strumienia gazów. Następnie gazy te wykonują pracę na łopatkach turbiny lub w dyszy wylotowej silnika odrzutowego, zamieniając część energii termicznej na energię mechaniczną.
W inżynierii chemicznej i procesowej liczne operacje jednostkowe mogą być aproksymowane jako izobaryczne. Dotyczy to na przykład podgrzewania cieczy w otwartych zbiornikach, gdzie ciśnienie jest praktycznie równe atmosferycznemu. Również destylacja prowadzona w kolumnach przy określonym ciśnieniu posługuje się bilansami entalpii opartymi na założeniu p = const. Obliczanie mocy wymienników ciepła, projektowanie kotłów, chłodnic oraz reaktorów chemicznych wymaga znajomości ilości ciepła przekazywanego w przemianach o stałym ciśnieniu, w tym danych o ciepłach właściwych i entalpiach mieszanin.
W laboratoriach fizycznych i chemicznych przemiany izobaryczne są wykorzystywane do wyznaczania własności materiałów. Pomiar ciepła właściwego przy stałym ciśnieniu, zarówno dla gazów, jak i dla cieczy oraz ciał stałych, często odbywa się w kalorymetrach pracujących przy ustalonym ciśnieniu zbliżonym do atmosferycznego. Dane te są później używane w modelowaniu procesów przemysłowych, prognozowaniu zachowania się substancji w różnych warunkach oraz w badaniach fundamentalnych nad strukturą materii i jej oddziaływaniami.
Na poziomie mikroświata, w opisie statystycznym, przemiana izobaryczna odpowiada takim zmianom, w których liczba cząsteczek i temperatura zmieniają się w obecności rezerwuaru ciśnienia. Teoretyczny opis wykorzystuje narzędzia mechaniki statystycznej i funkcji rozdziału, dostosowane do warunków p = const. Choć jest to zaawansowana matematycznie dziedzina, daje głębszy wgląd w naturę entalpii, ciepła oraz pracy w skali molekularnej, co z kolei przekłada się na rozwój nowych materiałów, lepsze modele reakcji chemicznych oraz bardziej precyzyjne przewidywania zachowania się substancji w ekstremalnych warunkach.
Interesującym obszarem zastosowań są również nauki o Ziemi i geofizyka. W wielu modelach wnętrza Ziemi oraz przepływów magmy przyjmuje się lokalne procesy o stałym ciśnieniu lub zbliżone do izobarycznych, aby uprościć opis skomplikowanych zjawisk sprzężonych termicznie i mechanicznie. Podobne podejście stosuje się w astrofizyce, analizując struktury gwiazd, gdzie w różnych warstwach ciśnienie można traktować jako quasi-stałe w krótkich skalach czasowych, podczas gdy energia jest transportowana głównie przez promieniowanie lub konwekcję.
Na końcu warto podkreślić rolę przemiany izobarycznej w dydaktyce i komunikacji naukowej. Stanowi ona jedno z pierwszych zagadnień, dzięki którym uczniowie i studenci uczą się łączyć pojęcia makroskopowe, takie jak ciśnienie, temperatura, objętość i ciepło, z abstrakcyjnymi funkcjami stanu, jak entalpia czy energia wewnętrzna. Zrozumienie tych zależności jest fundamentem dalszej nauki o termodynamice, fizyce statystycznej, inżynierii procesowej oraz energetyce. Dzięki temu możliwe jest świadome projektowanie systemów technicznych i odpowiedzialne zarządzanie energią w skali globalnej.
FAQ – najczęściej zadawane pytania o przemianę izobaryczną
Na czym dokładnie polega przemiana izobaryczna?
Przemiana izobaryczna to proces termodynamiczny zachodzący przy stałym ciśnieniu zewnętrznym, w którym zmieniają się inne wielkości stanu, przede wszystkim objętość i temperatura. Typowo analizuje się go dla gazów, choć można go rozpatrywać także dla cieczy i ciał stałych. W takim procesie ciepło dostarczone do układu równe jest zmianie entalpii, a dla gazu idealnego łatwo obliczyć je z wykorzystaniem ciepła właściwego przy stałym ciśnieniu.
Jak obliczyć pracę w przemianie izobarycznej?
Praca wykonana przez gaz w przemianie izobarycznej jest równa iloczynowi stałego ciśnienia i zmiany objętości: W = p (V₂ − V₁). Jeśli gaz się rozszerza, praca ma znak dodatni z punktu widzenia układu, co oznacza, że gaz oddaje energię mechaniczną otoczeniu. Przy sprężaniu znak jest ujemny, ponieważ to otoczenie wykonuje pracę na gazie. W praktyce często korzysta się z wykresu p–V, na którym praca odpowiada polu pod linią izobaryczną.
Jaka jest rola entalpii w procesach izobarycznych?
Entalpia jest szczególnie wygodną funkcją stanu właśnie w procesach izobarycznych. Dla przemiany przy stałym ciśnieniu zmiana entalpii ΔH jest dokładnie równa ilości ciepła wymienionego przez układ z otoczeniem: Q = ΔH. Umożliwia to prosty bilans energetyczny, zwłaszcza w systemach otwartych, takich jak kotły, wymienniki ciepła czy komory spalania. Dodatkowo, dla gazów doskonałych entalpia zależy wyłącznie od temperatury, co upraszcza obliczenia techniczne.
Gdzie w praktyce spotykamy przemiany izobaryczne?
Procesy zbliżone do izobarycznych zachodzą m.in. w atmosferze, przy ogrzewaniu i chłodzeniu powietrza na danej wysokości, w komorach spalania turbin gazowych i silników odrzutowych, w podgrzewaczach i chłodnicach pracujących przy ciśnieniu atmosferycznym, a także w wielu operacjach przemysłowych prowadzonych w kolumnach destylacyjnych czy zbiornikach otwartych. W laboratoriach większość pomiarów ciepła właściwego wykonuje się również przy stałym ciśnieniu.
Jakie są różnice między przemianą izobaryczną a izochoryczną?
W przemianie izobarycznej stałe jest ciśnienie, a może zmieniać się objętość, natomiast w izochorycznej stała pozostaje objętość, a zmienia się ciśnienie. W izobarycznej ciepło powiązane jest ze zmianą entalpii, a gaz wykonuje pracę pΔV. W izochorycznej nie występuje praca objętościowa, ponieważ nie ma zmiany V, a ciepło jest równe zmianie energii wewnętrznej. Różnica ta ma duże znaczenie przy analizie cykli silnikowych i projektowaniu procesów cieplnych.