Błona komórkowa to jedna z najbardziej fundamentalnych struktur w biologii, stanowiąca granicę między wnętrzem komórki a jej otoczeniem. Choć jest niezwykle cienka i pozornie delikatna, decyduje o przetrwaniu, komunikacji i specjalizacji komórek w każdym organizmie. Zrozumienie jej budowy i funkcji pozwala wyjaśnić wiele zjawisk biologicznych – od przewodzenia impulsów nerwowych, przez odporność, aż po działanie leków i powstawanie nowotworów.
Budowa błony komórkowej – mozaika lipidów i białek
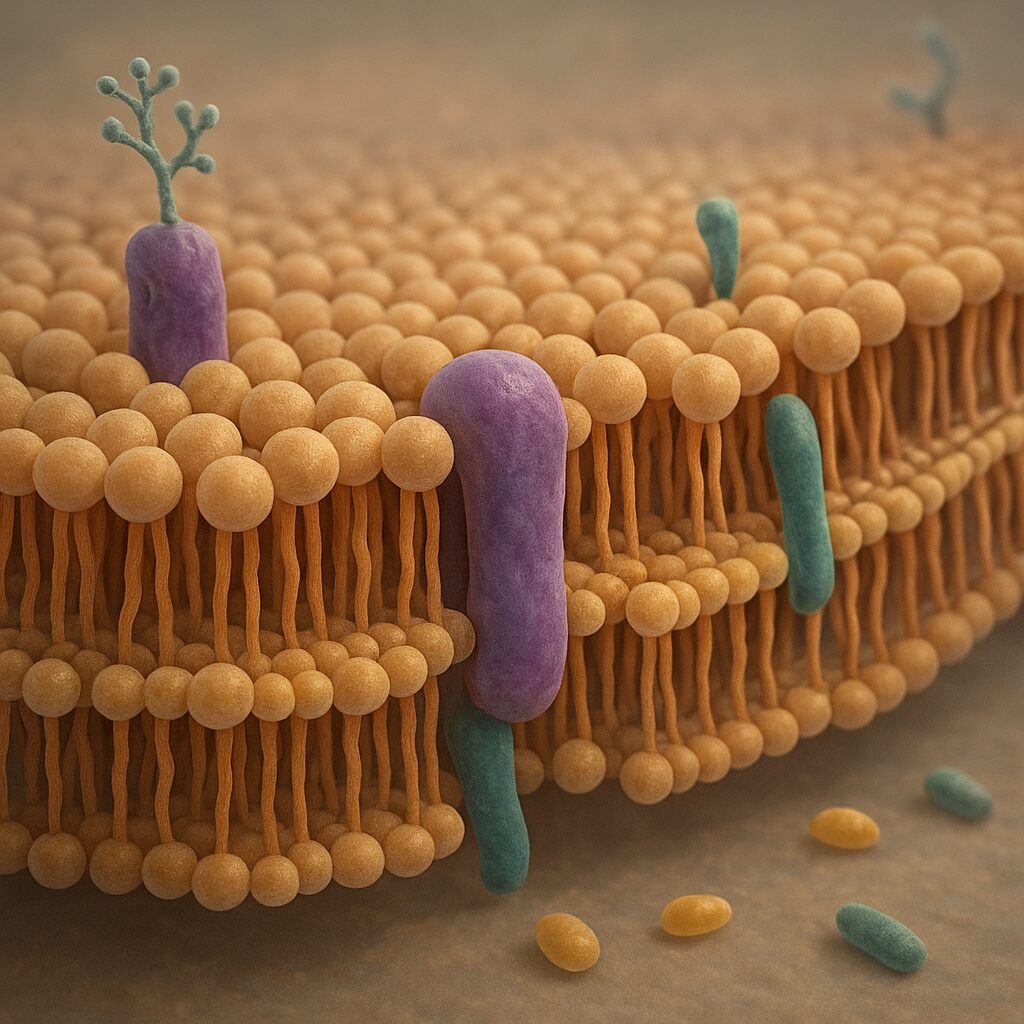
Błona komórkowa jest klasycznym przykładem tzw. modelu płynnej mozaiki. Oznacza to, że jej składniki nie są ułożone sztywno, ale tworzą dynamiczną, płynną strukturę, w której elementy mogą się przemieszczać w płaszczyźnie błony. Podstawę stanowi dwuwarstwa fosfolipidowa, w którą wbudowane są różne rodzaje białek, cukrów oraz inne lipidy, takie jak cholesterol.
Dwuwarstwa fosfolipidowa
Fosfolipidy to specjalna grupa lipidów, które posiadają część hydrofilową (głowę) oraz hydrofobowe ogony. W środowisku wodnym ich cząsteczki spontanicznie układają się w dwuwarstwę: hydrofilowe głowy zwrócone są na zewnątrz, ku wodnemu otoczeniu i cytoplazmie, a hydrofobowe ogony skierowane są do wnętrza błony. Taka konformacja tworzy barierę dla większości cząsteczek rozpuszczalnych w wodzie.
Dwuwarstwa fosfolipidowa jest strukturą półpłynną. Cząsteczki mogą się przemieszczać bocznie, obracać wokół własnej osi, a rzadziej „przeskakiwać” z jednej warstwy do drugiej. Ta płynność zależy od długości i stopnia nasycenia łańcuchów tłuszczowych oraz od obecności dodatkowych lipidów, takich jak cholesterol. Im więcej nienasyconych kwasów tłuszczowych, tym błona jest bardziej płynna, co wpływa na jej przepuszczalność i funkcjonowanie białek błonowych.
Rola cholesterolu i innych lipidów
Cholesterol pełni rolę „stabilizatora” błony komórkowej, zwłaszcza w komórkach zwierzęcych. Wbudowany między ogony fosfolipidów, ogranicza nadmierną ruchliwość łańcuchów tłuszczowych w wysokich temperaturach i zapobiega zbytniemu usztywnieniu błony w niskich. Dzięki temu błona zachowuje optymalną płynność w szerokim zakresie temperatur. Obecność cholesterolu wpływa również na powstawanie tzw. mikrodomen lipidowych, które mogą uczestniczyć w procesach sygnałowych.
Oprócz fosfolipidów i cholesterolu w błonie występują też glikolipidy – lipidy połączone z krótkimi łańcuchami cukrowymi. Tworzą one wraz z białkami warstwę nazywaną glikokaliksem, która pełni istotną funkcję w rozpoznawaniu komórek i ochronie ich powierzchni.
Białka błonowe – enzymy, receptory, transportery
Białka stanowią ok. 50% masy błony komórkowej (choć proporcje mogą się różnić w zależności od typu komórki). Wyróżniamy białka integralne, wnikające w głąb dwuwarstwy lipidowej lub ją przekraczające, oraz białka peryferyczne, luźno związane z jej powierzchnią. To właśnie białka decydują o większości specyficznych funkcji błony.
Wśród białek integralnych znajdują się kanały jonowe, receptory dla hormonów, białka transportujące substancje odżywcze czy pompy jonowe napędzane energią ATP. Białka te mają fragmenty hydrofobowe zakotwiczone w błonie oraz fragmenty hydrofilowe wystające do przestrzeni zewnątrz- i wewnątrzkomórkowej. Białka peryferyczne pełnią często rolę elementów cytoszkieletu, enzymów lub biorą udział w przekazywaniu sygnałów.
Glikokaliks i znaczenie cukrów na powierzchni komórki
Na zewnątrz błony komórkowej wielu komórek znajduje się warstwa złożona z oligosacharydów połączonych z białkami (glikoproteiny) i lipidami (glikolipidy). Tę cukrową otoczkę nazywa się glikokaliksem. Glikokaliks bierze udział w przyleganiu komórek do siebie, rozpoznawaniu własnych i obcych komórek przez układ odpornościowy oraz w tworzeniu barier ochronnych, np. w nabłonku jelitowym.
Dzięki specyficznym sekwencjom cukrowym komórki mogą „rozpoznawać się” wzajemnie, co ma kluczowe znaczenie dla procesów takich jak zapłodnienie, reakcje odpornościowe czy rozwój zarodkowy. Zmienność w składzie glikokaliksu bywa wykorzystywana przez komórki nowotworowe do unikania nadzoru immunologicznego.
Podstawowe funkcje błony komórkowej
Choć błona komórkowa jest cienka, pełni niezwykle liczne funkcje. Zapewnia fizyczną barierę, kontroluje przepływ substancji, pośredniczy w przekazywaniu informacji, uczestniczy w ruchu komórki oraz w jej interakcjach z innymi komórkami i macierzą zewnątrzkomórkową.
Bariera i ochrona komórki
Najbardziej oczywista funkcja błony komórkowej to tworzenie bariery oddzielającej wnętrze komórki od środowiska zewnętrznego. Dzięki właściwościom dwuwarstwy fosfolipidowej wiele cząsteczek nie może swobodnie przenikać przez błonę. Dotyczy to zwłaszcza dużych, naładowanych jonów oraz cząsteczek polarnych. Ta selektywność chroni przed niekontrolowanym napływem substancji toksycznych i utratą cennych metabolitów.
Z drugiej strony, błona nie jest strukturą całkowicie nieprzepuszczalną. Małe, niepolarne cząsteczki, takie jak tlen czy dwutlenek węgla, mogą dyfundować przez nią swobodnie. Możliwa jest też dyfuzja wody, choć jej przepływ jest dodatkowo ułatwiany przez specjalne białka – akwaporyny. Dzięki temu komórki mogą utrzymywać odpowiednie stężenia jonów i substancji odżywczych.
Selektywna przepuszczalność i transport
Jedną z kluczowych właściwości błony jest selektywna przepuszczalność. Komórka nie może zdać się na przypadkowe przenikanie substancji; musi kontrolować, co, kiedy i w jakiej ilości przez błonę przechodzi. Temu służą różne mechanizmy transportu: bierny i czynny.
Transport bierny zachodzi zgodnie z gradientem stężenia lub potencjału, bez wydatku energii. Należą do niego dyfuzja prosta, dyfuzja ułatwiona z udziałem nośników lub kanałów oraz osmoza. Transport czynny natomiast wymaga zużycia energii, najczęściej w postaci ATP, ponieważ odbywa się wbrew gradientowi stężenia.
Utrzymywanie homeostazy komórkowej
Dzięki swoim właściwościom błona komórkowa pomaga utrzymać homeostazę – względną równowagę warunków wewnątrz komórki. Odpowiednie stężenia jonów sodu, potasu, wapnia czy chloru warunkują prawidłowe pH cytoplazmy, objętość komórki, a także funkcjonowanie enzymów i innych białek.
Przykładem może być pompa sodowo-potasowa, która aktywnie usuwa jony sodu na zewnątrz komórki, a wprowadza jony potasu do jej wnętrza. Działanie tego mechanizmu zużywa znaczną część energii komórkowej, ale jest niezbędne do utrzymania potencjału błonowego, kluczowego np. dla przewodzenia impulsów nerwowych.
Przekazywanie sygnałów i komunikacja międzykomórkowa
Błona komórkowa jest również platformą dla systemu komunikacji komórkowej. Na jej powierzchni znajdują się receptory rozpoznające sygnały chemiczne – hormony, neuroprzekaźniki, cytokiny. Przyłączenie odpowiedniego ligandu do receptora błonowego inicjuje kaskadę sygnałową wewnątrz komórki, prowadząc do zmiany aktywności enzymów, ekspresji genów czy reorganizacji cytoszkieletu.
Niektóre receptory działają jako kanały jonowe otwierane ligandem, inne jako enzymy (np. kinazy tyrozynowe), a jeszcze inne wykorzystują białka G i przekaźniki wtórne. Zaburzenia w funkcjonowaniu tych receptorów leżą u podstaw licznych chorób, w tym nowotworów, chorób autoimmunologicznych czy zaburzeń metabolicznych. Wiele leków działa właśnie poprzez modulację receptorów błonowych.
Adhezja komórek i tworzenie tkanek
Błona komórkowa uczestniczy również w adhezji, czyli przyleganiu komórek do siebie oraz do elementów macierzy zewnątrzkomórkowej. Na jej powierzchni znajdują się cząsteczki adhezyjne – takie jak kadheryny, integryny czy selektyny – które umożliwiają stabilne połączenia międzykomórkowe i przekazywanie sił mechanicznych.
Dzięki tym połączeniom komórki mogą tworzyć tkanki o określonej spoistości i funkcji, np. nabłonki, mięśnie czy tkankę nerwową. Uszkodzenie lub nieprawidłowa regulacja białek adhezyjnych może prowadzić do zaburzeń rozwoju, chorób zapalnych czy zwiększonej zdolności komórek nowotworowych do tworzenia przerzutów.
Endocytoza i egzocytoza – transport pęcherzykowy
Nie wszystkie substancje mogą być transportowane przez błonę za pomocą kanałów lub transporterów. Duże cząsteczki, kompleksy białkowe czy całe mikroorganizmy są przemieszczane dzięki procesom endocytozy i egzocytozy, w których błona komórkowa bierze udział w tworzeniu i łączeniu pęcherzyków.
Endocytoza polega na wpuklaniu się błony i zamykaniu fragmentu środowiska zewnętrznego wewnątrz pęcherzyka, który odszczepia się do cytoplazmy. Wyróżnia się m.in. fagocytozę (pochłanianie dużych cząstek, np. bakterii) oraz pinocytozę (pobieranie płynów i rozpuszczonych substancji). Egzocytoza to proces odwrotny – pęcherzyki wewnątrzkomórkowe łączą się z błoną, uwalniając swoją zawartość na zewnątrz, np. hormony, neuroprzekaźniki czy enzymy trawienne.
Znaczenie błony komórkowej w zdrowiu, chorobie i badaniach naukowych
Zrozumienie, czym jest i jak funkcjonuje błona komórkowa, ma ogromne znaczenie praktyczne. Odgrywa ona kluczową rolę zarówno w fizjologii człowieka, jak i w patogenezie wielu chorób. Jest też celem licznych terapii farmakologicznych oraz narzędziem wykorzystywanym w nowoczesnych technologiach biologicznych.
Błona komórkowa a działanie leków
Wiele leków, aby zadziałać, musi przeniknąć przez błonę komórkową lub oddziaływać z receptorami w niej zakotwiczonymi. Struktura chemiczna cząsteczki leku – jej rozpuszczalność w tłuszczach, ładunek elektryczny, wielkość – decyduje o tym, czy i jak łatwo przekroczy ona barierę lipidową. Leki lipofilowe często dyfundują przez błonę stosunkowo łatwo, natomiast leki hydrofilowe wymagają transporterów lub pozostają w przestrzeni zewnątrzkomórkowej, działając na receptory błonowe.
Niektóre leki blokują kanały jonowe, zmieniając pobudliwość komórek nerwowych czy mięśniowych. Inne modulują aktywność receptorów, naśladując naturalne ligandy lub je blokując. Istnieją też leki, które zaburzają strukturę błon komórek bakteryjnych, prowadząc do ich śmierci. W farmakologii coraz większą rolę odgrywają systemy dostarczania leków oparte na pęcherzykach lipidowych (liposomach), które mogą fuzjować z błoną komórek docelowych.
Błona komórkowa w chorobach metabolicznych i nowotworach
Zaburzenia składu lipidowego lub białkowego błony mogą przyczyniać się do powstawania chorób metabolicznych. Przykładowo, w insulinooporności dochodzi do zmian w ekspresji i funkcjonowaniu receptorów insulinowych oraz transporterów glukozy. To z kolei zmniejsza zdolność komórek do pobierania glukozy z krwi, co leży u podstaw cukrzycy typu 2.
W komórkach nowotworowych często obserwuje się zmiany w strukturze glikokaliksu, gęstości receptorów oraz składzie lipidów błonowych. Ułatwia to im unikanie rozpoznania przez układ odpornościowy, zwiększa migrację i inwazyjność, a także wpływa na wrażliwość na leki. Badanie tych zmian stanowi ważny obszar onkologii molekularnej.
Rola błony komórkowej w układzie nerwowym
W neuronach błona komórkowa pełni kluczową rolę w generowaniu i przewodzeniu impulsów elektrycznych. Różnica stężeń jonów po obu stronach błony oraz obecność specyficznych kanałów jonowych tworzą warunki do powstania potencjału spoczynkowego i potencjałów czynnościowych. Szybkie, selektywne otwieranie i zamykanie kanałów dla sodu i potasu prowadzi do lokalnych zmian potencjału błonowego, które propagują się wzdłuż aksonu.
Na zakończeniach nerwowych błona komórkowa bierze udział w procesie egzocytozy pęcherzyków synaptycznych, uwalniających neuroprzekaźniki do szczeliny synaptycznej. Następnie neuroprzekaźniki wiążą się z receptorami błonowymi neuronu postsynaptycznego, inicjując dalsze zmiany elektryczne. Wszelkie zaburzenia w strukturze lub funkcjonowaniu błony neuronów mogą prowadzić do chorób neurologicznych, takich jak padaczka, neuropatie czy choroby neurodegeneracyjne.
Błona komórkowa w mikroorganizmach
U bakterii błona komórkowa pełni dodatkowe funkcje, które w komórkach eukariotycznych przejęły mitochondria czy chloroplasty. Na przykład w błonie bakterii zachodzi fosforylacja oksydacyjna, czyli proces wytwarzania ATP przy użyciu łańcucha oddechowego. Wiele antybiotyków działa poprzez uszkadzanie błon bakteryjnych lub blokowanie ich kluczowych białek transportowych, co prowadzi do zaburzenia homeostazy i śmierci komórki.
Wirusy, choć same nie posiadają typowej błony komórkowej, często wykorzystują błonę gospodarza do tworzenia swoich otoczek lipidowych. Podczas uwalniania z zakażonej komórki wirus może „zabrać” fragment błony, w którym znajdują się wbudowane wirusowe białka. Te białka służą później do rozpoznawania kolejnych komórek docelowych i wnikania do nich.
Technologie oparte na błonach – od liposomów do biosensorów
Współczesna biotechnologia chętnie wykorzystuje właściwości błon komórkowych. Tworzenie sztucznych pęcherzyków lipidowych (liposomów) pozwala na zamykanie w nich leków, białek czy kwasów nukleinowych. Takie liposomy mogą być modyfikowane, aby rozpoznawały określone typy komórek, co umożliwia precyzyjne dostarczanie substancji terapeutycznych, np. w terapii nowotworów.
Innym kierunkiem jest konstruowanie biosensorów, w których białka błonowe, np. receptory lub kanały jonowe, są wbudowywane w sztuczne błony. Zmiany ich aktywności pod wpływem określonych cząsteczek mogą być przetwarzane na sygnały elektryczne lub optyczne, tworząc czułe systemy detekcji, użyteczne w diagnostyce medycznej i monitoringu środowiskowym.
Ewolucyjne znaczenie błony komórkowej
Pojawienie się pierwszych struktur przypominających błony komórkowe było jednym z kluczowych etapów w ewolucji życia na Ziemi. Samorzutne tworzenie się pęcherzyków lipidowych w wodnym środowisku mogło umożliwić oddzielenie i koncentrację cząsteczek zdolnych do katalizy oraz powielania. W ten sposób wyłoniły się protokomórki, które dały początek współczesnym formom życia.
Ewolucja błon obejmowała dostosowanie ich składu lipidowego i białkowego do różnych warunków środowiskowych. Organizmy żyjące w wysokich temperaturach, bardzo słonym środowisku czy w warunkach beztlenowych mają błony o specyficznych właściwościach fizykochemicznych. Analiza składu błon różnych organizmów stanowi cenne źródło informacji o ich adaptacjach i historii ewolucyjnej.
Wybrane mechanizmy transportu przez błonę komórkową
Aby zrozumieć, w jaki sposób błona komórkowa kontroluje przemieszczanie substancji, warto przyjrzeć się bliżej konkretnym mechanizmom transportu. Od nich zależy odżywianie komórki, usuwanie produktów przemiany materii, pobudliwość elektryczna oraz reakcje na bodźce środowiskowe.
Dyfuzja prosta i osmoza
Dyfuzja prosta to spontaniczne przemieszczanie się cząsteczek z obszaru o wyższym stężeniu do obszaru o niższym stężeniu, aż do wyrównania stężeń. Przez dwuwarstwę lipidową mogą w ten sposób przenikać małe cząsteczki niepolarne, takie jak gazy oddechowe lub niektóre lipofilowe związki. Ten rodzaj transportu nie wymaga udziału białek transportujących ani nakładu energii.
Osmoza natomiast dotyczy przepływu wody przez półprzepuszczalną błonę. Jeśli po obu jej stronach znajdują się roztwory o różnym stężeniu substancji rozpuszczonej, woda będzie przemieszczać się z roztworu mniej stężonego do bardziej stężonego. Dla komórek oznacza to konieczność regulacji ciśnienia osmotycznego, aby uniknąć nadmiernego pęcznienia lub kurczenia się.
Dyfuzja ułatwiona – rola kanałów i nośników
Wiele cząsteczek polarnych lub naładowanych nie może dyfundować swobodnie przez rdzeń hydrofobowy błony. Do ich transportu wykorzystuje się dyfuzję ułatwioną, z udziałem specyficznych białek: kanałów jonowych i transporterów (nośników). Transport ten wciąż zachodzi zgodnie z gradientem stężenia lub ładunku, więc nie wymaga bezpośredniego zużycia energii.
Kanały jonowe tworzą wodne pory w błonie, przez które mogą szybko przemieszczać się określone jony, np. Na+, K+, Ca2+ czy Cl−. Kanały mogą być otwierane lub zamykane pod wpływem zmian napięcia (kanały zależne od napięcia), przyłączenia ligandu (kanały ligandozależne) lub bodźca mechanicznego. Transportery natomiast przyłączają cząsteczkę po jednej stronie błony, przechodzą konformacyjną zmianę i uwalniają ją po stronie przeciwnej.
Transport czynny i pompy jonowe
Transport czynny pozwala na gromadzenie substancji wbrew ich gradientowi stężenia, co wymaga nakładu energii. Pierwotny transport czynny wykorzystuje bezpośrednio energię z hydrolizy ATP, natomiast wtórny transport czynny czerpie energię ze zgromadzonego gradientu jonowego.
Klasycznym przykładem pierwotnego transportu czynnego jest pompa sodowo-potasowa, która wypompowuje jony sodu na zewnątrz komórki i sprowadza jony potasu do jej wnętrza. Ten proces jest niezbędny do utrzymania potencjału błonowego i objętości komórki. Z kolei transport wtórny wykorzystuje różnicę stężenia jonów (często sodu) do napędzania transportu innych substancji, np. glukozy czy aminokwasów, w tym samym lub przeciwnym kierunku.
Transport pęcherzykowy – endocytoza i egzocytoza w praktyce
Wspomniana wcześniej endocytoza i egzocytoza są nie tylko sposobem na transport dużych cząsteczek, ale także ważnym elementem regulacji składu błony. Podczas endocytozy fragment błony zostaje „wciągnięty” do wnętrza komórki, natomiast egzocytoza dostarcza nowe fragmenty błony z pęcherzyków. Dzięki temu komórka może modyfikować liczbę dostępnych receptorów czy transporterów na swojej powierzchni.
Szczególnym rodzajem endocytozy jest endocytoza zależna od receptorów, w której specyficzne cząsteczki są najpierw rozpoznawane przez receptory błonowe, a następnie internalizowane w postaci pęcherzyków pokrytych białkiem klatryną. Pozwala to na bardzo selektywny, wydajny transport substancji, takich jak lipoproteiny, hormony czy czynniki wzrostu.
Specjalizacje błon w różnych typach komórek
Choć ogólna zasada budowy błony jest wspólna dla wszystkich komórek, jej skład i struktura lokalna mogą być silnie zróżnicowane. W komórkach nabłonkowych powierzchnia skierowana do światła narządu (powierzchnia apikalna) może mieć zupełnie inne właściwości niż powierzchnia bazolateralna, zwrócona ku tkankom i naczyniom. Takie spolaryzowanie błony umożliwia kierunkowy transport substancji, np. w jelicie lub kanalikach nerkowych.
W komórkach mięśniowych błona tworzy wpuklenia (kanaliki T), dzięki którym sygnał elektryczny może szybko docierać w głąb komórki, inicjując skurcz. W fotoreceptorach siatkówki błony tworzą skomplikowane struktury dysków, w których znajdują się białka odpowiedzialne za odbiór światła. Te przykłady pokazują, jak elastyczna i plastyczna jest organizacja błon komórkowych.
FAQ – najczęściej zadawane pytania o błonę komórkową
Jakie jest najważniejsze zadanie błony komórkowej?
Najważniejszym zadaniem błony komórkowej jest oddzielenie wnętrza komórki od środowiska zewnętrznego przy jednoczesnym zachowaniu kontrolowanego kontaktu z otoczeniem. Błona tworzy barierę, która zapobiega przypadkowemu napływowi i ucieczce substancji, a jednocześnie dzięki białkom transportującym i receptorom umożliwia selektywną wymianę jonów, składników odżywczych, produktów przemiany materii oraz informacji chemicznych.
Dlaczego błona komórkowa nazywana jest płynną mozaiką?
Określenie płynna mozaika odnosi się do dwóch kluczowych cech błony: jej płynności oraz zróżnicowania składu. Fosfolipidy i inne lipidy tworzą ruchomą, półpłynną dwuwarstwę, w której cząsteczki mogą się przemieszczać bocznie. W tej „podstawie” zakotwiczone są różne białka – kanały, receptory, enzymy – tworząc coś w rodzaju mozaiki. Taka organizacja zapewnia zarówno elastyczność, jak i wysoką specjalizację funkcji błony.
W jaki sposób przez błonę komórkową przechodzą substancje odżywcze?
Substancje odżywcze mogą przekraczać błonę na kilka sposobów, zależnie od ich wielkości i właściwości chemicznych. Małe cząsteczki niepolarne dyfundują bezpośrednio przez dwuwarstwę lipidową. Cząsteczki polarne, takie jak glukoza czy aminokwasy, wykorzystują transportery białkowe w procesie dyfuzji ułatwionej lub transportu czynnego. Większe kompleksy – na przykład lipoproteiny – są pobierane drogą endocytozy zależnej od receptorów.
Czym różni się transport bierny od czynnego przez błonę?
Transport bierny nie wymaga dostarczania energii metabolicznej, ponieważ substancje przemieszczają się zgodnie z gradientem stężenia lub potencjału elektrochemicznego. Należą do niego dyfuzja prosta, dyfuzja ułatwiona oraz osmoza. Transport czynny zachodzi wbrew gradientowi, co wymaga nakładu energii, zazwyczaj z hydrolizy ATP lub z wcześniej wytworzonego gradientu jonowego. Dzięki temu komórka może akumulować substancje w wysokim stężeniu lub usuwać jony na zewnątrz.
Jakie znaczenie ma błona komórkowa w powstawaniu chorób?
Nieprawidłowości w budowie lub funkcjonowaniu błony komórkowej mogą leżeć u podstaw wielu chorób. Zmiany w receptorach i transporterach mogą prowadzić do insulinooporności, zaburzeń gospodarki lipidowej czy nadciśnienia. Mutacje w kanałach jonowych wywołują choroby kanałopatii, wpływając na pracę serca i układu nerwowego. Z kolei modyfikacje glikokaliksu i białek adhezyjnych sprzyjają rozwojowi nowotworów i ich zdolności do tworzenia przerzutów.