Łańcuch oddechowy stanowi kluczowy etap pozyskiwania energii w komórkach organizmów tlenowych. To tu, na błonach mitochondriów i błonach komórkowych bakterii, zachodzi kontrolowany przepływ elektronów, który zamienia energię zmagazynowaną w zredukowanych cząsteczkach na użyteczną energię chemiczną w postaci ATP. Zrozumienie struktury i działania łańcucha oddechowego pozwala wyjaśnić, skąd bierze się energia potrzebna do pracy mięśni, przewodzenia impulsów nerwowych czy syntezy związków budujących nasze ciało.
Podstawy bioenergetyki i rola łańcucha oddechowego
Żywe komórki nieustannie zużywają energię, aby utrzymać porządek wewnętrzny, prowadzić reakcje metaboliczne i reagować na zmiany środowiska. Główną uniwersalną „walutą energetyczną” jest ATP – adenozynotrifosforan. Jego rozkład do ADP i fosforanu nieorganicznego uwalnia energię, która może zostać sprzężona z innymi procesami. Jednak ATP musi być stale odnawiane, a najefektywniejszym sposobem jego produkcji u organizmów tlenowych jest fosforylacja oksydacyjna, zachodząca właśnie w łańcuchu oddechowym.
Łańcuch oddechowy to ciąg przenośników elektronów osadzonych w błonie. Energia pochodzi z utleniania zredukowanych koenzymów, głównie NADH i FADH2, które powstają w szlaku glikolizy, reakcji pomostowej oraz cyklu kwasu cytrynowego. Elektrony z tych nośników przepływają przez kolejne kompleksy białkowe, a ich energia stopniowo uwalnia się i jest używana do pompowania protonów przez błonę, co tworzy gradient elektrochemiczny. Na końcu elektrony są przekazywane na tlen cząsteczkowy, który zostaje zredukowany do wody.
Bez łańcucha oddechowego możliwości pozyskiwania energii przez komórki drastycznie by się zmniejszyły. Organizm musiałby polegać wyłącznie na fermentacji lub innych procesach beztlenowych, znacznie mniej wydajnych energetycznie. To dlatego mitochondria – organella, w których u eukariontów zachodzi łańcuch oddechowy – często określane są jako „elektrownie komórki”. U bakterii i archeonów podobne procesy zachodzą w błonie komórkowej, pokazując ewolucyjną uniwersalność tego mechanizmu pozyskiwania energii.
Budowa i lokalizacja łańcucha oddechowego
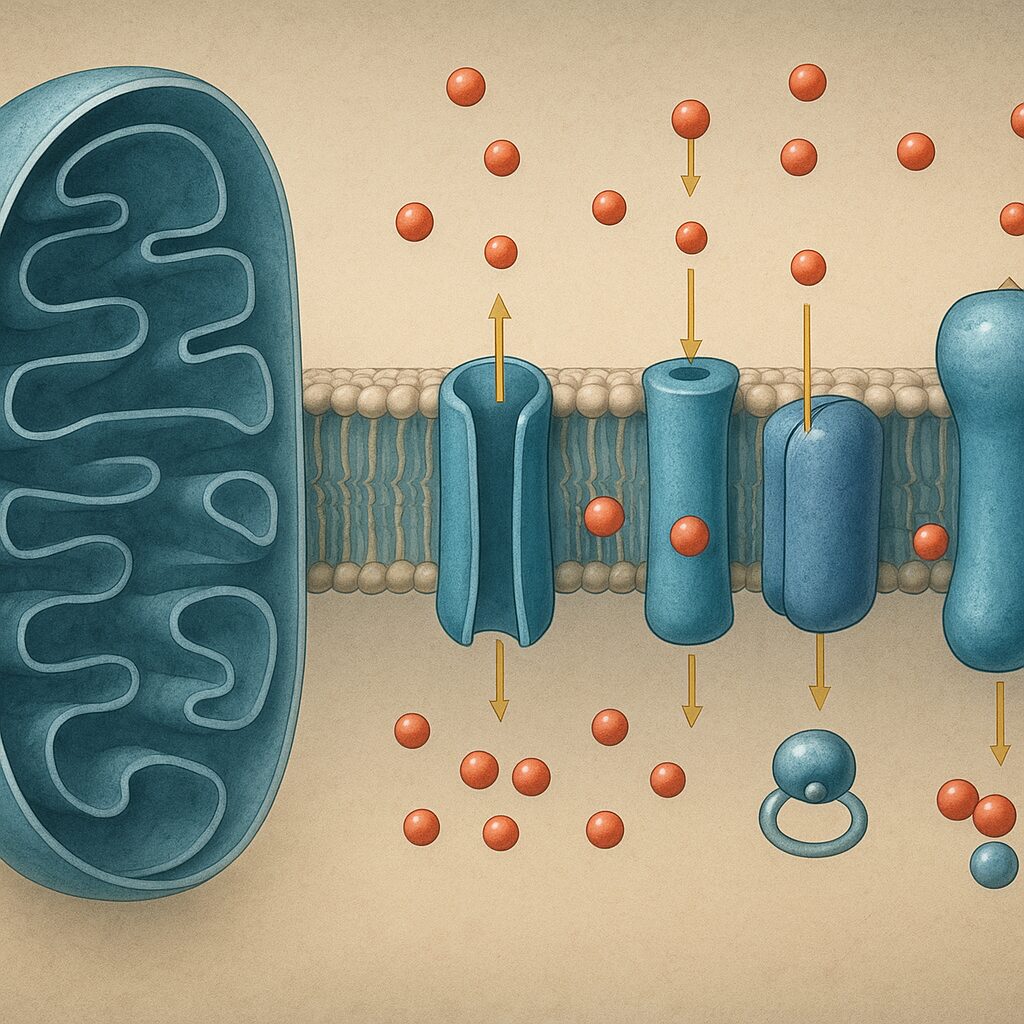
W komórkach eukariotycznych łańcuch oddechowy zlokalizowany jest w błonie wewnętrznej mitochondrium. Błona ta jest silnie pofałdowana, tworząc grzebienie mitochondrialne, co znacząco zwiększa jej powierzchnię i pozwala na umieszczenie dużej liczby kompleksów oddechowych. Przestrzeń między błoną wewnętrzną a zewnętrzną nazywana jest przestrzenią międzybłonową, natomiast wnętrze mitochondrium wypełnia macierz mitochondrialna, bogata w enzymy cyklu kwasu cytrynowego oraz cząsteczki NAD+ i FAD.
Łańcuch oddechowy składa się z czterech głównych kompleksów białkowych oraz dwóch ruchliwych nośników. Kompleks I, czyli dehydrogenaza NADH:ubichinon, przyjmuje elektrony z NADH, które powstały m.in. w cyklu kwasu cytrynowego i reakcji dehydrogenacji pirogronianu. Kompleks II, będący jednocześnie składnikiem cyklu Krebsa (dehydrogenaza bursztynianowa), przenosi elektrony z FADH2. Oba kompleksy przekazują elektrony na ubichinon (koenzym Q), ruchliwy nośnik lipidowy poruszający się w warstwie lipidów błony.
Ubichinon, po przyjęciu pary elektronów, ulega redukcji do ubichinolu i przenosi je do kompleksu III – cytochromu bc1. Ten złożony kompleks przekazuje elektrony na kolejny ruchliwy nośnik, cytochrom c, który jest małym białkiem z grupą hemową, poruszającym się po zewnętrznej powierzchni błony wewnętrznej. Ostatecznie cytochrom c dostarcza elektrony do kompleksu IV, czyli oksydazy cytochromu c, gdzie następuje ich przekazanie na tlen i powstanie cząsteczek wody.
Równolegle z przepływem elektronów zachodzi proces pompowania protonów przez błonę wewnętrzną mitochondrium. Kompleksy I, III i IV transportują protony z macierzy mitochondrialnej do przestrzeni międzybłonowej. W efekcie po stronie przestrzeni międzybłonowej gromadzi się nadmiar protonów, podczas gdy po stronie macierzy ich stężenie spada. Tworzy to gradient stężenia i ładunku – tzw. siłę protonomotoryczną.
Struktura łańcucha oddechowego nie jest jednak całkowicie stała i sztywna. Skład i liczba kompleksów mogą zmieniać się w zależności od typu tkanki, zapotrzebowania na energię czy warunków fizjologicznych. W tkance mięśniowej, zwłaszcza w mięśniu sercowym, mitochondria są szczególnie liczne i obfitują w elementy łańcucha oddechowego, co umożliwia im zaspokajanie ogromnego zapotrzebowania na ATP. Natomiast w niektórych organizmach i tkankach występują dodatkowe oksydazy alternatywne, które mogą omijać część kompleksów klasycznego łańcucha.
Mechanizm działania: przepływ elektronów i fosforylacja oksydacyjna
Działanie łańcucha oddechowego można opisać przez pryzmat dwóch ściśle powiązanych procesów: transportu elektronów i wytwarzania ATP. Elektrony wędrują od zredukowanych koenzymów w stronę tlenu, przechodząc przez szereg przenośników o coraz wyższym potencjale redoks. Ta kaskada powoduje, że przepływ elektronów jest termodynamicznie korzystny, a uwalniana stopniowo energia pozwala na pompowanie protonów. System ten jest znacznie bardziej kontrolowany i bezpieczny niż nagłe spalenie substratu w ogniu, choć w obu przypadkach końcowym akceptorem elektronów jest tlen.
Elektrony z NADH trafiają do kompleksu I, gdzie NADH ulega utlenieniu do NAD+, a elektrony przechodzą przez szereg centrów żelazowo-siarkowych. Uwalniana energia napędza przepompowywanie protonów z macierzy do przestrzeni międzybłonowej. FADH2, powstający w kompleksie II, przekazuje elektrony bezpośrednio na ubichinon, jednak ten etap nie wiąże się z pompowaniem protonów przez kompleks II. To dlatego utlenianie NADH dostarcza więcej energii i skutkuje większą liczbą cząsteczek ATP niż utlenianie FADH2.
Ubichinon i cytochrom c stanowią kluczowe ruchome elementy łańcucha. Ubichinon, będący cząsteczką hydrofobową, swobodnie przemieszcza się w dwuwarstwie lipidowej, zbierając elektrony z różnych miejsc – nie tylko z kompleksu I i II, ale także z innych dehydrogenaz, np. związanych z utlenianiem kwasów tłuszczowych. Kompleks III uczestniczy w tak zwanym cyklu Q, w którym ubichinon przechodzi złożone przemiany redoks, a energia tych przemian wykorzystywana jest do dalszego pompowania protonów.
Oksydaza cytochromu c, czyli kompleks IV, jest ostatnim etapem łańcucha. Tu elektrony przekazywane są na tlen cząsteczkowy, który wiąże się z jonami wodoru, tworząc wodę. Proces ten jest niezwykle precyzyjnie kontrolowany, aby ograniczyć powstawanie reaktywnych form tlenu. Kompleks IV również pompuje protony do przestrzeni międzybłonowej, dopełniając budowę gradientu protonowego. To właśnie obecność tlenu jako ostatniego akceptora elektronów warunkuje wydajność całego systemu i tłumaczy, dlaczego brak tlenu tak szybko zaburza funkcjonowanie komórek.
Drugą częścią układanki jest wykorzystanie gradientu protonów do syntezy ATP. Odpowiada za to syntaza ATP – duży kompleks białkowy zbudowany z części błonowej i wystającej do macierzy główki katalitycznej. Protony przepływają z przestrzeni międzybłonowej z powrotem do macierzy przez kanał w części błonowej syntazy ATP. Ten ruch napędza obroty fragmentu białka, które przenoszą się na część katalityczną, umożliwiając połączenie ADP i fosforanu nieorganicznego w ATP. Proces ten określany jest jako fosforylacja oksydacyjna.
Hipoteza chemiosmotyczna, sformułowana przez Petera Mitchella, wyjaśnia mechanizm sprzężenia transportu elektronów z syntezą ATP za pośrednictwem gradientu protonowego. Została ona początkowo przyjęta z dużym sceptycyzmem, ponieważ przełamywała dotychczasowe schematy myślenia o bioenergetyce, jednak liczne eksperymenty potwierdziły jej słuszność. Dziś uznaje się ją za podstawę rozumienia tego, jak łańcuch oddechowy zamienia energię reakcji redoks na energię wiązań chemicznych w ATP.
Warto podkreślić, że łańcuch oddechowy nie jest idealnie szczelny. Część elektronów może „uciekać” z normalnej drogi i przedwcześnie redukować tlen, prowadząc do powstawania reaktywnych form tlenu, takich jak anionorodnik ponadtlenkowy czy nadtlenek wodoru. Nadmiar tych cząsteczek może uszkadzać białka, lipidy i DNA, dlatego komórki wyposażone są w rozmaite systemy antyoksydacyjne: enzymatyczne (np. dysmutaza ponadtlenkowa, katalaza, peroksydazy glutationowe) oraz nieenzymatyczne (np. glutation, witaminy C i E). Równowaga między produkcją reaktywnych form tlenu a ich neutralizacją jest istotnym elementem zachowania homeostazy komórkowej.
Znaczenie fizjologiczne, regulacja i konsekwencje zaburzeń łańcucha oddechowego
Łańcuch oddechowy spełnia kluczową funkcję nie tylko jako źródło ATP, ale także jako regulator wielu procesów metabolicznych. Wysoka aktywność łańcucha wiąże się z intensywnym zużyciem tlenu i substratów energetycznych, takich jak glukoza i kwasy tłuszczowe. W stanach zwiększonego zapotrzebowania na energię – podczas wysiłku fizycznego, pracy mózgu czy termogenezy – mitochondria przyspieszają utlenianie substratów i zwiększają tempo fosforylacji oksydacyjnej. Zdolność do elastycznego dostosowywania intensywności pracy łańcucha oddechowego jest warunkiem utrzymania stabilnego funkcjonowania komórki i całego organizmu.
Regulacja łańcucha oddechowego zachodzi na kilku poziomach. Najważniejszym czynnikiem jest dostępność ADP – im więcej ADP, tym intensywniej syntaza ATP może pracować, a tym samym szybciej „zużywany” jest gradient protonowy. To z kolei nasila przepływ elektronów i zużycie tlenu. Taki mechanizm sprzężenia zwrotnego zapewnia, że ATP jest produkowane głównie wtedy, gdy jest potrzebne. Dodatkowo aktywność kompleksów łańcucha może być modulowana przez fosforylację białek, zmiany w składzie lipidów błonowych czy dostępność substratów redukcyjnych, takich jak NADH.
Istnieją również zjawiska rozprzęgania fosforylacji oksydacyjnej, w których gradient protonów ulega częściowemu lub całkowitemu rozproszeniu bez produkcji ATP. Może to następować za sprawą białek rozprzęgających (UCP) lub substancji chemicznych, takich jak dinitrofenol. W mitochondriach brunatnej tkanki tłuszczowej białko UCP1 umożliwia przepływ protonów z pominięciem syntazy ATP, dzięki czemu energia gradientu protonowego przekształcana jest w ciepło. Zjawisko to odgrywa ważną rolę w termoregulacji, zwłaszcza u noworodków i zwierząt hibernujących.
Zaburzenia w funkcjonowaniu łańcucha oddechowego mogą prowadzić do poważnych konsekwencji zdrowotnych. Mutacje w genach kodujących białka kompleksów oddechowych, zarówno w genomie jądrowym, jak i mitochondrialnym, skutkują różnorodnymi chorobami mitochondrialnymi. Objawy takich schorzeń są często niespecyficzne i obejmują osłabienie mięśni, nietolerancję wysiłku, zaburzenia neurologiczne, uszkodzenie narządu wzroku czy serca. Ponieważ mitochondria występują najliczniej w tkankach o dużym zapotrzebowaniu na energię, to właśnie one są najbardziej podatne na skutki dysfunkcji łańcucha oddechowego.
Niektóre toksyny i leki mogą bezpośrednio hamować elementy łańcucha oddechowego. Przykładowo cyjanek potasu i tlenek węgla blokują działanie oksydazy cytochromu c, uniemożliwiając redukcję tlenu. Skutkuje to gwałtownym zatrzymaniem fosforylacji oksydacyjnej i szybkim niedoborem ATP, co może prowadzić do śmierci komórki. Inne związki, jak rotenon czy antymycyna A, blokują wcześniejsze etapy łańcucha, hamując odpowiednio kompleks I oraz kompleks III. Zrozumienie tych mechanizmów jest ważne nie tylko z punktu widzenia toksykologii, ale także farmakologii i projektowania leków.
Łańcuch oddechowy odgrywa także ważną rolę w procesach starzenia się i rozwoju chorób cywilizacyjnych. Przewlekłe zaburzenia pracy mitochondriów, nadmierna produkcja reaktywnych form tlenu oraz gromadzenie się uszkodzeń w DNA mitochondrialnym mogą przyczyniać się do rozwoju chorób neurodegeneracyjnych, takich jak choroba Parkinsona czy Alzheimera. Korelacje między dysfunkcją łańcucha oddechowego a insulinoopornością, otyłością i chorobami sercowo-naczyniowymi wskazują, że mitochondria są nie tylko silnikiem komórki, lecz także istotnym ośrodkiem regulacji metabolicznej całego organizmu.
Wreszcie warto podkreślić znaczenie łańcucha oddechowego w kontekście ewolucji. Obecność podobnych systemów transportu elektronów u bakterii, archeonów i eukariontów sugeruje, że zdolność do wykorzystywania gradientów protonowych jako źródła energii jest bardzo dawnym i fundamentalnym osiągnięciem życia na Ziemi. Hipoteza endosymbiotyczna zakłada, że mitochondria wywodzą się z dawnych bakterii tlenowych, które weszły w symbiotyczny związek z komórką eukariotyczną. Przejęcie tych wydajnych systemów bioenergetycznych mogło umożliwić powstanie złożonych form życia wielokomórkowego.
FAQ – najczęściej zadawane pytania o łańcuch oddechowy
Czym dokładnie jest łańcuch oddechowy i gdzie zachodzi?
Łańcuch oddechowy to zespół białkowych kompleksów enzymatycznych, które przenoszą elektrony z NADH i FADH2 na tlen cząsteczkowy, tworząc wodę. W tym procesie energia reakcji redoks wykorzystywana jest do pompowania protonów przez błonę, co prowadzi do wytworzenia gradientu elektrochemicznego. U eukariontów łańcuch oddechowy zlokalizowany jest w błonie wewnętrznej mitochondriów, a u bakterii – w błonie komórkowej, pełniąc analogiczną funkcję energetyczną.
Jaką rolę pełni tlen w łańcuchu oddechowym?
Tlen pełni funkcję końcowego akceptora elektronów. W kompleksie IV, czyli oksydazie cytochromu c, elektrony są przekazywane na cząsteczkę tlenu, która łączy się z protonami, tworząc wodę. Dzięki wysokiemu potencjałowi redoks tlenu cały przepływ elektronów jest termodynamicznie korzystny, a uwalniana stopniowo energia może zostać wykorzystana do pompowania protonów. Brak tlenu powoduje zatrzymanie przepływu elektronów, spadek syntezy ATP i zmusza komórki do przejścia na mniej wydajne procesy beztlenowe.
Czym jest fosforylacja oksydacyjna i jak powiązana jest z łańcuchem oddechowym?
Fosforylacja oksydacyjna to proces syntezy ATP sprzężony z utlenianiem substratów w łańcuchu oddechowym. Transport elektronów przez kompleksy I–IV prowadzi do utworzenia gradientu protonowego, a następnie protony przepływają przez syntazę ATP z powrotem do macierzy mitochondrialnej. Ten przepływ napędza obroty części białka i umożliwia połączenie ADP z fosforanem nieorganicznym. W ten sposób energia chemiczna zmagazynowana w NADH i FADH2 zamieniana jest na wysokoenergetyczne wiązania w ATP.
Dlaczego NADH daje więcej ATP niż FADH2?
NADH oddaje elektrony do kompleksu I, który pompuje protony przez błonę, a następnie elektrony przechodzą przez kompleksy III i IV, również pompujące protony. Umożliwia to wytworzenie większego gradientu protonowego i syntezę większej liczby cząsteczek ATP. FADH2 wprowadza elektrony na poziomie kompleksu II, który nie pompuje protonów. W efekcie elektrony z FADH2 omijają pierwsze miejsce generowania gradientu, co skutkuje mniejszą ilością przepompowanych protonów i niższym uzyskiem ATP na jedną cząsteczkę zredukowanego koenzymu.
Jakie są skutki zaburzeń w funkcjonowaniu łańcucha oddechowego?
Zaburzenia łańcucha oddechowego prowadzą do niedoboru ATP, nadmiernej produkcji reaktywnych form tlenu i zaburzeń metabolizmu komórkowego. Objawiają się osłabieniem mięśni, szybką męczliwością, uszkodzeniem narządów o dużym zapotrzebowaniu energetycznym, takich jak serce, mózg czy mięśnie szkieletowe. Choroby mitochondrialne mogą wynikać z mutacji w DNA mitochondrialnym lub jądrowym. Ponadto wiele toksyn, np. cyjanek czy tlenek węgla, działa poprzez bezpośrednie hamowanie kompleksów łańcucha oddechowego, co może być szybko śmiertelne.