Pompa sodowo-potasowa jest jednym z kluczowych mechanizmów podtrzymujących życie komórek. Jej działanie umożliwia utrzymanie odpowiedniego stężenia jonów po obu stronach błony komórkowej, co leży u podstaw przewodnictwa nerwowego, kurczenia mięśni, funkcjonowania nerek czy regulacji objętości komórek. Zrozumienie zasady działania tej pompy pozwala lepiej pojąć, jak organizmy utrzymują homeostazę i reagują na bodźce ze środowiska.
Budowa i lokalizacja pompy sodowo-potasowej
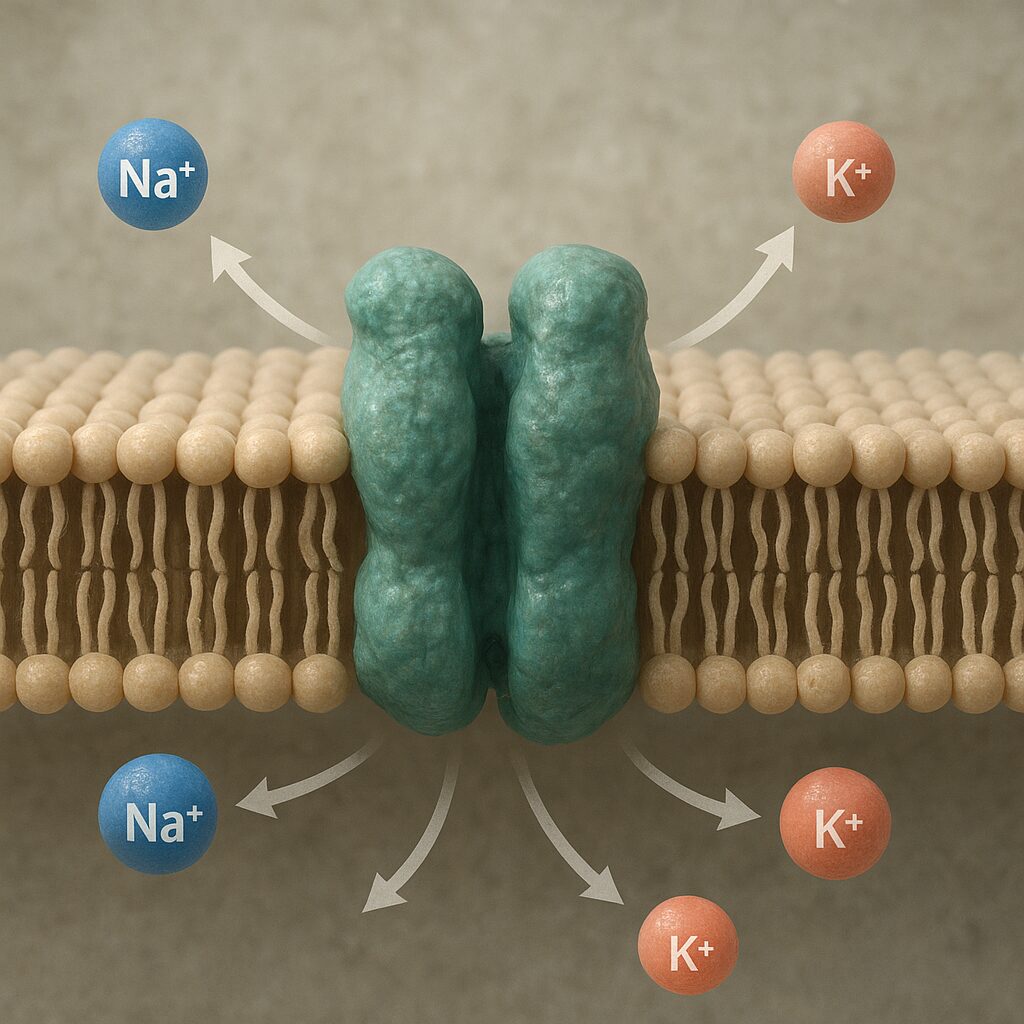
Pompa sodowo-potasowa, nazywana także Na⁺/K⁺-ATP-azą, jest białkiem błonowym występującym niemal we wszystkich typach komórek organizmów zwierzęcych. Wbudowana jest w błonę komórkową, a dokładniej w jej dwuwarstwę lipidową. Składa się z kilku podjednostek, które razem tworzą sprawnie działający kompleks enzymatyczny.
Najważniejsza jest podjednostka α, zawierająca miejsce wiązania jonów oraz miejsce wiązania ATP, czyli cząsteczki służącej jako źródło energii. Podjednostka β stabilizuje strukturę kompleksu i pomaga w jego zakotwiczeniu w błonie. W niektórych komórkach występuje dodatkowo podjednostka γ (czasem nazywana FXYD), która moduluje aktywność pompy w zależności od warunków fizjologicznych.
Pompa sodowo-potasowa znajduje się przede wszystkim w:
- błonach neuronów, gdzie uczestniczy w generowaniu i utrzymywaniu potencjału spoczynkowego oraz w regeneracji po potencjale czynnościowym,
- komórkach mięśniowych, umożliwiając prawidłowy przebieg skurczu i rozkurczu,
- komórkach nabłonka nerek i jelit, regulując transport jonów i wody,
- komórkach mięśnia sercowego, gdzie pośrednio wpływa na siłę skurczu i rytm serca.
Charakterystyczną cechą tego białka jest obecność wielu segmentów przechodzących przez błonę, tzw. domen transbłonowych. Tworzą one kanał oraz miejsca wiązania dla jonów sodu i potasu. Zmiany konformacji białka, indukowane przez przyłączanie i hydrolizę ATP, powodują naprzemienne otwieranie się pompy w stronę wnętrza i zewnętrza komórki.
Mechanizm działania: transport aktywny i rola ATP
Pompa sodowo-potasowa jest klasycznym przykładem transportu aktywnego. Oznacza to, że przemieszcza jony wbrew ich gradientowi stężeń – z obszaru o niższym stężeniu do obszaru o wyższym. Taki proces wymaga dostarczenia energii, którą zapewnia hydroliza ATP do ADP i nieorganicznego fosforanu.
Standardowy cykl działania pompy Na⁺/K⁺ można przedstawić w kilku krokach:
- Od strony cytoplazmy do białka przyłączają się trzy jony sodu (Na⁺).
- ATP wiąże się z miejscem katalitycznym i ulega hydrolizie, co prowadzi do fosforylacji pompy.
- Fosforylacja wywołuje zmianę konformacji białka – otwarcie kanału w stronę przestrzeni zewnątrzkomórkowej i uwolnienie trzech jonów Na⁺ na zewnątrz.
- Od strony zewnątrzkomórkowej do pompy przyłączają się dwa jony potasu (K⁺).
- Następuje defosforylacja białka i powrót do pierwotnej konformacji, co powoduje transport dwóch jonów K⁺ do wnętrza komórki.
W rezultacie każdy pełny cykl pompy prowadzi do wypompowania trzech jonów sodu na zewnątrz i wpompowania dwóch jonów potasu do środka, przy zużyciu jednej cząsteczki ATP. Bilans ładunków jest zatem nierówny – na zewnątrz przenoszony jest jeden dodatni ładunek więcej niż do wnętrza. Z tego powodu pompa sodowo-potasowa jest elektrogenna, czyli przyczynia się do powstania różnicy potencjałów elektrycznych po obu stronach błony.
Znaczenie energetyczne tego procesu jest ogromne. W neuronach i komórkach mięśniowych pompa sodowo-potasowa może zużywać nawet znaczną część ATP produkowanego przez komórkę. Mimo wysokiego kosztu energetycznego, utrzymanie prawidłowego gradientu jonów Na⁺ i K⁺ jest niezbędne do funkcjonowania wielu procesów fizjologicznych, w tym pracy układu nerwowego i mięśniowego.
Znaczenie gradientu sodowo-potasowego dla funkcji komórki
Utrzymywany przez pompę gradient jonów Na⁺ i K⁺ ma fundamentalne znaczenie dla funkcjonowania komórek. Wnętrze komórki charakteryzuje się wysokim stężeniem potasu i niskim stężeniem sodu, podczas gdy środowisko zewnątrzkomórkowe zawiera więcej sodu i mniej potasu. Taki rozkład stężeń warunkuje szereg procesów biologicznych.
Po pierwsze, różnica stężeń jonów i wynikająca z niej różnica potencjałów elektrycznych po obu stronach błony komórkowej tworzy tzw. potencjał spoczynkowy. W komórkach nerwowych wartość ta wynosi zwykle około -70 mV. Potencjał spoczynkowy jest niezbędny do powstawania i przewodzenia impulsów nerwowych.
Po drugie, gradient sodowy jest wykorzystywany przez inne białka transportujące, tzw. kotransportery i wymienniki, jako źródło energii dla transportu wtórnie aktywnego. Przykładem jest kotransporter glukozy i sodu w jelicie cienkim, który umożliwia wchłanianie glukozy do komórek nabłonka mimo jej często wyższego stężenia wewnątrz komórki niż w świetle jelita. Dzięki wcześniejszej pracy pompy Na⁺/K⁺ gradient sodu jest tak duży, że jego wnikanie do komórki „pociąga” za sobą cząsteczki innych substancji.
Po trzecie, gradient sodowo-potasowy wpływa na regulację objętości komórki. Gdy do wnętrza komórki napływa zbyt dużo jonów i wody, pompa może zwiększyć swoją aktywność, usuwając nadmiar sodu na zewnątrz. Zapobiega to nadmiernemu pęcznieniu komórki i jej rozerwaniu. Z tego punktu widzenia pompa sodowo-potasowa jest kluczowa dla utrzymania homeostazy wodno-elektrolitowej na poziomie pojedynczych komórek.
Dodatkowo gradient Na⁺/K⁺ wpływa na aktywność wielu enzymów, białek transportowych i receptorów. Warto zaznaczyć, że zaburzenia tego gradientu natychmiast odbijają się na działaniu całych tkanek i narządów, szczególnie tak wrażliwych jak mózg czy mięsień sercowy.
Rola pompy sodowo-potasowej w przewodnictwie nerwowym
Komórki nerwowe, czyli neurony, wykorzystują różnice w stężeniach jonów oraz potencjale błonowym do przekazywania informacji w postaci impulsów elektrycznych, tzw. potencjałów czynnościowych. Pompa sodowo-potasowa nie generuje sama impulsu, ale stwarza warunki niezbędne do jego wystąpienia, utrzymując właściwy rozkład Na⁺ i K⁺.
Potencjał spoczynkowy neuronu powstaje w głównej mierze dzięki selektywnej przepuszczalności błony dla potasu oraz dzięki działaniu pompy Na⁺/K⁺. Gdy neuron otrzymuje bodziec, dochodzi do chwilowego zwiększenia przepuszczalności błony dla sodu i szybki napływ Na⁺ do komórki depolaryzuje błonę. Następnie otwierają się kanały potasowe, co umożliwia wypływ K⁺ na zewnątrz i przywrócenie ujemnego potencjału wewnątrz komórki.
Po zakończeniu potencjału czynnościowego, rozkład jonów Na⁺ i K⁺ po obu stronach błony ulega zaburzeniu – wewnątrz neuronu jest nieco więcej sodu, a na zewnątrz więcej potasu, niż w warunkach spoczynkowych. W tym momencie aktywność pompy sodowo-potasowej przywraca pierwotny gradient stężeń, wypompowując Na⁺ na zewnątrz i wprowadzając K⁺ do środka. Bez tego mechanizmu neuron po serii impulsów straciłby zdolność do dalszego generowania potencjałów czynnościowych.
Szczególnie w mózgu, który jest strukturą niezwykle aktywną elektrycznie, pompa sodowo-potasowa zużywa ogromne ilości energii. Szacuje się, że u człowieka znacząca część całkowitego zużycia tlenu przez mózg idzie na produkcję ATP, wykorzystywanego właśnie przez Na⁺/K⁺-ATP-azę. W stanie niedotlenienia lub niedokrwienia, gdy brakuje ATP, praca pompy ustaje, co szybko prowadzi do zaburzeń przewodnictwa nerwowego i potencjalnie nieodwracalnego uszkodzenia komórek nerwowych.
Znaczenie w pracy mięśni i mięśnia sercowego
Mięśnie szkieletowe, gładkie i mięsień sercowy opierają swoje działanie na kontrolowanych zmianach potencjału błonowego oraz na precyzyjnym gospodarowaniu jonami, zwłaszcza wapnia, sodu i potasu. Pompa sodowo-potasowa pełni w tym kontekście rolę fundamentu, na którym nadbudowane są inne mechanizmy regulacyjne.
Podczas skurczu włókna mięśniowego dochodzi do depolaryzacji błony, zwykle poprzez otwarcie kanałów sodowych i napływ Na⁺. Następnie, podobnie jak w neuronach, następuje repolaryzacja z udziałem kanałów potasowych. Każdy taki cykl powoduje niewielkie przesunięcia jonów między wnętrzem a zewnętrzem komórki. Aby włókno mięśniowe mogło kurczyć się wielokrotnie, pompa Na⁺/K⁺ musi stale przywracać wyjściowy rozkład stężeń.
W przypadku serca znaczenie pompy jest jeszcze bardziej złożone. Utrzymywanie prawidłowych stężeń Na⁺ i K⁺ wpływa nie tylko na potencjał czynnościowy kardiomiocytów, ale również na pośrednią regulację stężenia jonów wapnia (Ca²⁺) wewnątrz komórki. Wapń jest bezpośrednim wyzwalaczem skurczu mięśnia sercowego, a jego wewnątrzkomórkowy poziom zależy m.in. od wymiennika sodowo-wapniowego (NCX), którego działanie z kolei jest uzależnione od gradientu sodowego.
Jeżeli aktywność pompy sodowo-potasowej jest zaburzona, może dochodzić do poważnych konsekwencji klinicznych, takich jak arytmie serca, osłabienie siły skurczu czy nawet zatrzymanie krążenia. Niektóre leki stosowane w kardiologii, np. glikozydy nasercowe, oddziałują pośrednio na Na⁺/K⁺-ATP-azę, modyfikując gradient jonów i tym samym zwiększając siłę skurczu serca. Pokazuje to, że zrozumienie roli pompy ma bezpośrednie przełożenie na praktykę medyczną.
Regulacja aktywności pompy sodowo-potasowej
Aktywność pompy Na⁺/K⁺ nie jest stała – komórka może ją modulować w zależności od swoich potrzeb i warunków środowiskowych. Regulacja ta zachodzi na kilku poziomach: od zmian w ekspresji genu kodującego podjednostki pompy, przez modyfikacje potranslacyjne białka, po wpływ czynników zewnętrznych, takich jak hormony czy stężenie jonów.
Istotnym regulatorem jest stężenie sodu wewnątrz komórki. Wzrost wewnątrzkomórkowego Na⁺ zwiększa powinowactwo pompy do ATP i pobudza jej aktywność, co pomaga szybciej usunąć nadmiar sodu. Z kolei niskie stężenie Na⁺ w cytoplazmie może prowadzić do spadku aktywności pompy. Podobnie stężenie potasu w otoczeniu komórki wpływa na szybkość transportu tego jonu do wnętrza komórki.
Na poziomie hormonalnym aktywność pompy modyfikują m.in. hormony tarczycy, aldosteron oraz insulina. Hormony tarczycy mogą zwiększać liczbę pomp w błonie komórkowej, co przyspiesza metabolizm i zużycie tlenu. Aldosteron nasila syntezę białek pompy w komórkach kanalików nerkowych, zwiększając wydalanie sodu i zatrzymywanie potasu. Insulina wpływa na aktywność Na⁺/K⁺-ATP-azy m.in. w mięśniach i tkance tłuszczowej, co ma znaczenie w regulacji stężenia potasu we krwi po posiłku.
Nie bez znaczenia są także modyfikacje potranslacyjne, takie jak fosforylacja przez kinazy białkowe, które mogą szybko zmieniać wydajność pompy w odpowiedzi na sygnały z otoczenia. Dzięki temu komórka jest w stanie dynamicznie dostosowywać transport jonów do zmieniających się warunków, na przykład podczas wysiłku fizycznego lub w odpowiedzi na stres.
Pompa sodowo-potasowa w nerkach i regulacji gospodarki wodno-elektrolitowej
Nerki pełnią kluczową rolę w regulacji składu płynów ustrojowych, a pompa Na⁺/K⁺ jest jednym z głównych narzędzi, dzięki którym mogą to robić. W komórkach kanalika nerkowego pompa ta znajduje się zwykle w błonie podstawno-bocznej, skąd aktywnie transportuje sód z komórki do płynu śródmiąższowego, umożliwiając jego dalsze przechodzenie do krwi.
Jednocześnie sód wnika do komórki od strony światła kanalika przez różne transportery współprzenoszące inne substancje, np. glukozę, aminokwasy czy fosforany. Dzięki temu nerka jest w stanie jednocześnie odzyskiwać z przesączu kłębuszkowego liczne cenne związki i regulować ich stężenie we krwi. Ruch sodu jest często sprzężony z ruchem wody, dlatego pompa sodowo-potasowa pośrednio decyduje o objętości wydalanego moczu.
W odcinkach nefronu odpowiedzialnych za zagęszczanie moczu, gradient sodowy tworzony m.in. przez Na⁺/K⁺-ATP-azę stabilizuje różnice osmotyczne między korą a rdzeniem nerki. To właśnie te różnice pozwalają na odzyskiwanie wody z filtratu i utrzymanie prawidłowego stężenia elektrolitów w osoczu. Gdy pompa działa nieprawidłowo, może dojść do zaburzeń w regulacji sodu i potasu, co prowadzi do nieprawidłowego ciśnienia tętniczego, obrzęków lub odwodnienia.
W układzie nerkowym duże znaczenie ma wspomniany wcześniej hormon aldosteron, który zwiększa syntezę i aktywność pomp sodowo-potasowych w komórkach dystalnych części nefronu i cewkach zbiorczych. W efekcie więcej sodu jest wchłaniane zwrotnie do krwi, a więcej potasu wydalane z moczem. Zwiększa to objętość płynów ustrojowych i sprzyja wzrostowi ciśnienia krwi. Zrozumienie tych zależności jest podstawą terapii wielu chorób nadciśnieniowych i zaburzeń elektrolitowych.
Farmakologiczne i toksyczne oddziaływania na pompę sodowo-potasową
Pompa Na⁺/K⁺ jest celem działania niektórych substancji farmakologicznych oraz toksyn. Z jednej strony umożliwia to wykorzystanie jej w terapii określonych chorób, z drugiej – stanowi potencjalne źródło niebezpiecznych zaburzeń.
Przykładem leków oddziałujących na Na⁺/K⁺-ATP-azę są glikozydy nasercowe, takie jak digoksyna. Leki te hamują pompę w komórkach mięśnia sercowego, co prowadzi do zwiększenia wewnątrzkomórkowego stężenia sodu. Zmniejsza się w ten sposób wydajność wymiennika sodowo-wapniowego, co skutkuje wzrostem stężenia wapnia w komórce. Więcej Ca²⁺ dostępnego w cytoplazmie oznacza silniejszy skurcz serca, dlatego glikozydy stosowane są w leczeniu niewydolności krążenia. Jednocześnie wąski zakres terapeutyczny tych leków sprawia, że łatwo o skutki uboczne, w tym zaburzenia rytmu serca.
Innym przykładem są toksyny roślinne i zwierzęce, które mogą blokować działanie pompy, prowadząc do groźnych zaburzeń w przewodnictwie nerwowym i pracy mięśni. Długotrwałe zahamowanie Na⁺/K⁺-ATP-azy uniemożliwia utrzymanie gradientu jonowego, co skutkuje obrzękiem komórek, utratą potencjału błonowego i w skrajnych przypadkach ich śmiercią.
W fizjologii eksperymentalnej oraz farmakologii badawczej wykorzystuje się także swoiste inhibitory pompy, takie jak ouabaina, aby analizować znaczenie gradientu Na⁺/K⁺ w różnych procesach komórkowych. Pozwala to lepiej zrozumieć zarówno podstawowe mechanizmy fizjologiczne, jak i mechanizmy działania leków.
Znaczenie pompy sodowo-potasowej w patofizjologii
Zaburzenia funkcji pompy sodowo-potasowej mogą wynikać zarówno z mutacji genetycznych, jak i z nabytych chorób metabolicznych, zaburzeń ukrwienia czy niedoborów energetycznych. Konsekwencje tych nieprawidłowości są widoczne szczególnie w tkankach o dużym zapotrzebowaniu energetycznym, takich jak mózg, serce i mięśnie szkieletowe.
W chorobach neurologicznych, np. w niektórych formach padaczki czy migreny, dysfunkcja Na⁺/K⁺-ATP-azy może prowadzić do zaburzeń pobudliwości neuronów i ich nadmiernej aktywności. W ostrych stanach niedokrwiennych mózgu (udar) spadek produkcji ATP uniemożliwia prawidłową pracę pompy, co jest jednym z kluczowych etapów prowadzących do obrzęku i obumierania komórek nerwowych.
W kardiologii zaburzenia pracy pompy wpływają na przewodnictwo w sercu i mogą sprzyjać powstawaniu arytmii. Podwyższone lub obniżone stężenie potasu we krwi (hiperkaliemia, hipokaliemia) wpływa na równowagę między pompą a kanałami jonowymi, co przekłada się na zmianę czasu trwania potencjału czynnościowego kardiomiocytów.
W chorobach metabolicznych, takich jak cukrzyca, długotrwałe zmiany w metabolizmie energetycznym oraz wrażliwości na insulinę mogą pośrednio modyfikować aktywność Na⁺/K⁺-ATP-azy w różnych tkankach. Ma to konsekwencje dla krążenia obwodowego, funkcji nerek oraz przewodnictwa w obwodowym układzie nerwowym. Warto podkreślić, że choć pompa sodowo-potasowa jest pojedynczym białkiem, jego rola w organizmie jest wielowymiarowa i ściśle powiązana z wieloma chorobami.
Znaczenie ewolucyjne i porównawcze pompy sodowo-potasowej
Pompa Na⁺/K⁺ należy do szerokiej rodziny ATP-az P-typowych, które ewolucyjnie pojawiły się bardzo wcześnie i występują w różnych organizmach. Choć klasyczna pompa sodowo-potasowa jest szczególnie istotna u zwierząt, mechanizmy wykorzystujące energię ATP do transportu jonów przez błonę są obecne także u roślin, grzybów czy drobnoustrojów.
W toku ewolucji organizmy dostosowywały skład i aktywność pomp jonowych do warunków środowiskowych, w jakich żyją. U zwierząt lądowych utrzymanie równowagi wodno-elektrolitowej było kluczowe dla uniezależnienia się od środowiska wodnego. Pompa sodowo-potasowa, współdziałając z innymi białkami transportującymi, umożliwiła precyzyjne kontrolowanie składu płynów ustrojowych, co było warunkiem powstania skomplikowanych układów narządów, w tym wydajnego układu nerwowego.
Porównania międzygatunkowe wskazują, że podstawowy mechanizm działania pompy jest dobrze zachowany. Różnice dotyczą głównie regulacji aktywności, izoform podjednostek oraz stopnia ekspresji w poszczególnych tkankach. Badania te pomagają lepiej zrozumieć, jak zmiany w jednym, pozornie prostym mechanizmie molekularnym mogą wpływać na przystosowanie organizmów do różnych nisz ekologicznych.
Pompa sodowo-potasowa a energetyka komórki
Utrzymanie działania pompy Na⁺/K⁺ wymaga stałego dostarczania ATP, które powstaje głównie w mitochondriach w procesie fosforylacji oksydacyjnej. Wysokie tempo pracy pompy w komórkach nerwowych i mięśniowych sprawia, że ich zapotrzebowanie na tlen i substraty energetyczne jest wyjątkowo duże. Zależność między produkcją ATP a aktywnością Na⁺/K⁺-ATP-azy jest na tyle ścisła, że zakłócenia jednego z tych elementów natychmiast odbijają się na drugim.
W warunkach niedotlenienia, np. podczas intensywnego wysiłku bez odpowiedniego dopływu tlenu lub w stanach patologicznych (zawał, udar), spada produkcja ATP. Komórka przechodzi na mniej wydajny metabolizm beztlenowy, co nie wystarcza do utrzymania wysokiej aktywności pompy. Gradualne zmniejszanie różnicy stężeń Na⁺ i K⁺ sprzyja obrzękowi komórek, zaburzeniom przewodnictwa i w skrajnych przypadkach martwicy.
Analogicznie, przewlekłe zaburzenia metaboliczne (np. w chorobach mitochondrialnych) mogą powodować chroniczne niedostatki ATP, co przekłada się na osłabioną aktywność pompy. Objawia się to często zmęczeniem mięśni, zaburzeniami neurologicznymi czy niewydolnością narządową. W efekcie Na⁺/K⁺-ATP-aza jest nie tylko biernym konsumentem energii, ale także wskaźnikiem ogólnej kondycji metabolicznej komórki.
Perspektywy badań i zastosowań związanych z pompą sodowo-potasową
Współczesna nauka intensywnie bada strukturę i funkcję pompy sodowo-potasowej na poziomie molekularnym. Rozwój metod obrazowania, takich jak krio-mikroskopia elektronowa, umożliwił uzyskanie bardzo szczegółowych modeli przestrzennych białka w różnych stanach konformacyjnych. Pozwala to lepiej zrozumieć, w jaki sposób zmiany struktury umożliwiają transport jonów i wiązanie ATP.
Badane są również różnice między izoformami pompy, występującymi w różnych tkankach i na różnych etapach rozwoju organizmu. Może to w przyszłości umożliwić projektowanie bardziej selektywnych leków, oddziałujących na konkretne typy Na⁺/K⁺-ATP-azy, co ograniczy działania niepożądane. Ponadto analizuje się rolę pompy w procesach starzenia, neurodegeneracji oraz w odpowiedzi komórek na stres oksydacyjny i zapalny.
Na poziomie klinicznym coraz lepiej rozumiane jest znaczenie genetycznych wariantów białek pompy w podatności na różne choroby, w tym nadciśnienie, zaburzenia rytmu serca czy schorzenia neurologiczne. Potencjalne terapie genowe lub molekularne ukierunkowane na korekcję funkcji Na⁺/K⁺-ATP-azy mogą w przyszłości stanowić element nowoczesnej medycyny personalizowanej.
FAQ – najczęściej zadawane pytania
Jaką podstawową funkcję pełni pompa sodowo-potasowa w komórce?
Pompa sodowo-potasowa utrzymuje różnicę stężeń jonów sodu i potasu po obu stronach błony komórkowej. Wypompowuje trzy jony sodu na zewnątrz komórki i wprowadza dwa jony potasu do jej wnętrza, zużywając przy tym ATP. Dzięki temu powstaje potencjał błonowy, możliwy jest transport wtórnie aktywny wielu substancji, regulacja objętości komórek oraz prawidłowe funkcjonowanie układu nerwowego i mięśni.
Dlaczego działanie pompy sodowo-potasowej wymaga ATP?
Pompa sodowo-potasowa przenosi jony sodu i potasu wbrew ich gradientowi stężeń, czyli z miejsc o niższym stężeniu do miejsc o wyższym. Taki transport jest energetycznie niekorzystny i nie może zajść spontanicznie. ATP dostarcza potrzebnej energii poprzez hydrolizę do ADP i fosforanu. Fosforylacja białka pompy wywołuje zmiany jego konformacji, które umożliwiają naprzemienne otwieranie się w stronę wnętrza i zewnętrza komórki.
Co się stanie, gdy pompa sodowo-potasowa przestanie działać?
Zatrzymanie pracy pompy prowadzi do stopniowego zaniku gradientu jonów Na⁺ i K⁺. Komórka traci potencjał błonowy, co uniemożliwia przewodnictwo nerwowe i prawidłową pracę mięśni. Zaburzona zostaje regulacja objętości komórki – zaczyna ona pęcznieć z powodu napływu jonów i wody. W tkankach wrażliwych na niedotlenienie, jak mózg czy serce, skutki pojawiają się szybko i mogą prowadzić do nieodwracalnego uszkodzenia komórek oraz śmierci organizmu.
W jaki sposób pompa sodowo-potasowa wpływa na pracę serca?
W sercu pompa Na⁺/K⁺ utrzymuje prawidłowe stężenia sodu i potasu w kardiomiocytach, co warunkuje właściwy kształt potencjału czynnościowego i rytm pracy serca. Pośrednio wpływa też na stężenie jonów wapnia, kluczowych dla siły skurczu. Zaburzenia jej działania mogą wywoływać arytmie, osłabiać lub nadmiernie nasilać kurczliwość mięśnia sercowego. Niektóre leki kardiologiczne, jak glikozydy nasercowe, modulują aktywność pompy, aby poprawić wydolność serca u chorych z niewydolnością krążenia.