Transdukcja genetyczna należy do najciekawszych mechanizmów przekazywania materiału dziedzicznego między komórkami. Zjawisko to łączy w sobie elementy mikrobiologii, genetyki molekularnej oraz wirusologii, a jego zrozumienie stało się kluczowe zarówno dla badań podstawowych, jak i dla nowoczesnej biotechnologii. Pozwala ono wyjaśnić, w jaki sposób geny mogą przeskakiwać między organizmami, tworząc nowe kombinacje cech, co ma znaczenie dla ewolucji, medycyny oraz inżynierii genetycznej.
Czym jest transdukcja genetyczna i jak ją odkryto
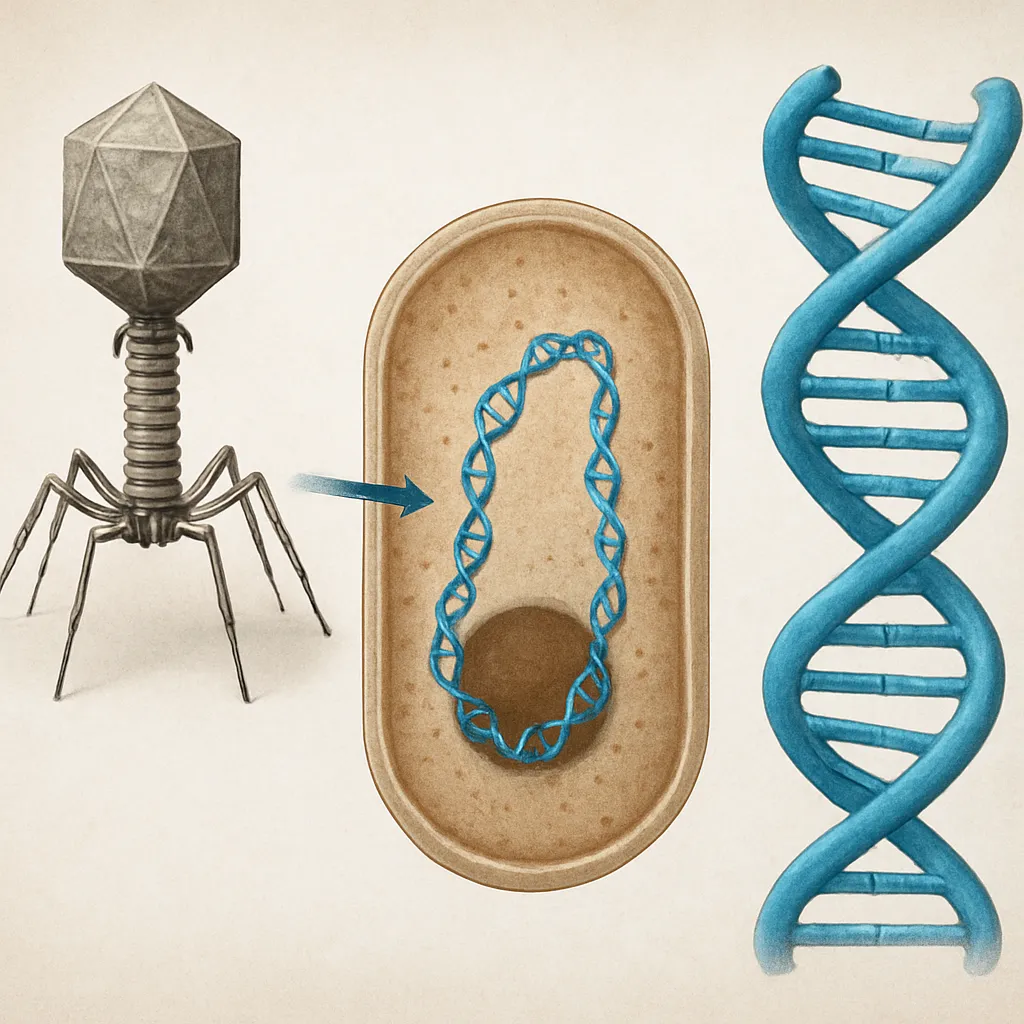
Transdukcja genetyczna to proces przenoszenia materiału genetycznego z jednej komórki bakteryjnej do innej za pośrednictwem bakteriofaga, czyli wirusa infekującego bakterie. Innymi słowy, geny dawcy zostają „zapakowane” do cząstki wirusowej, a następnie wprowadzone do komórki biorcy podczas kolejnej infekcji. W efekcie komórka biorcy otrzymuje dodatkowe fragmenty DNA, które mogą wbudować się do jej własnego genomu.
Zjawisko zostało odkryte w latach 50. XX wieku przez Joshuy Lederberga i Nortona Zindera. Badając bakterie Salmonella, zaobserwowali oni przekazywanie cech genetycznych między szczepami, mimo zastosowania filtrów zatrzymujących komórki. Aby wyjaśnić to zjawisko, zaproponowano udział czynnika o rozmiarach wirusa. Późniejsze eksperymenty wykazały, że tym czynnikiem są bakteriofagi, zdolne przenosić fragmenty bakteryjnego DNA z jednej komórki do drugiej.
Kluczowe jest rozróżnienie transdukcji od innych sposobów przekazywania materiału genetycznego u bakterii. Obok transdukcji wyróżnia się:
- transformację – pobieranie „nagiego” DNA z otoczenia przez komórkę bakteryjną,
- koniugację – bezpośrednie przekazywanie DNA poprzez mostek cytoplazmatyczny pomiędzy dwiema komórkami.
Transdukcja różni się od tych procesów tym, że wymaga obecności wirusa, który działa jak swoisty wektor przenoszący informację genetyczną. Mechanizm ten okazał się niezwykle istotny, ponieważ dowiódł, że wirusy mogą służyć nie tylko do niszczenia komórek, lecz również do wymiany i rekombinacji informacji dziedzicznej.
Rodzaje transdukcji: ogólna, specjalizowana i uwarunkowana
Transdukcja ogólna
Transdukcja ogólna (generalized transduction) występuje, gdy bakteriofag w trakcie swojego cyklu litycznego przypadkowo pakuje fragmenty DNA gospodarza zamiast własnego genomu. Podczas infekcji bakteriofag wstrzykuje swój materiał genetyczny do komórki bakteryjnej, przejmuje kontrolę nad jej maszynerią i doprowadza do degradacji chromosomu bakteryjnego. Fragmenty bakteryjnego DNA swobodnie unoszą się w cytoplazmie i mogą zostać omyłkowo włączone do nowo powstających cząstek wirusowych.
Tak powstają tzw. cząstki defektywne, które zawierają bakteryjne DNA zamiast wirusowego. Gdy taki „błędnie” złożony fag zainfekuje kolejną komórkę, wprowadza do niej fragmenty genomu poprzedniego gospodarza. Ponieważ defektywny fag nie zawiera pełnego zestawu wirusowych genów, zazwyczaj nie jest w stanie przeprowadzić pełnego cyklu replikacyjnego, ale skutecznie dostarcza obcy materiał genetyczny do biorcy.
W komórce biorcy mogą zajść dwa scenariusze:
- wprowadzone DNA ulega degradacji, jeśli nie znajdzie odpowiednich sekwencji homologicznych lub mechanizmów ochronnych,
- wprowadzone DNA ulega rekombinacji homologicznej z chromosomem biorcy, prowadząc do trwałego włączenia nowych genów.
Transdukcja ogólna jest „niespecyficzna” – w zasadzie dowolny fragment genomu dawcy może zostać przeniesiony, jeśli tylko odpowiednio zostanie spakowany do cząstki fagowej. Skutkiem jest możliwość losowego mieszania i rozprzestrzeniania genów, co ma szczególne znaczenie w rozwoju oporności na antybiotyki i w adaptacji bakterii do nowych warunków środowiskowych.
Transdukcja specjalizowana
Transdukcja specjalizowana (specialized transduction) związana jest z bakteriofagami umiarkowanymi, które mogą integrować swój genom z chromosomem bakteryjnym. Klasycznym przykładem jest fag lambda infekujący Escherichia coli. W stanie lizogenicznym genom faga wbudowuje się w określone miejsce chromosomu bakterii, tworząc profaga. W takim stanie może pozostawać przez wiele pokoleń, replikuje się synchronicznie z komórką gospodarza i nie powoduje jej natychmiastowej lizy.
Pod wpływem bodźców stresowych, takich jak promieniowanie UV czy uszkodzenie DNA, profag może ulec aktywacji i przejść do cyklu litycznego. W procesie wycinania się z chromosomu bakterii zwykle zachodzi precyzyjne odłączenie sekwencji wirusowych. Jednak czasem dochodzi do błędu – wraz z genomem faga zostaje wycięty sąsiadujący fragment bakteryjnego DNA, natomiast fragment genu wirusa może pozostać w chromosomie gospodarza.
W efekcie powstaje cząstka wirusowa zawierająca kombinację DNA fagowego i ściśle określonych genów bakteryjnych leżących w pobliżu miejsca integracji. Ponieważ tylko geny z konkretnego regionu chromosomu mogą zostać przeniesione, zjawisko to nazywa się transdukcją specjalizowaną. Po infekcji następnej komórki bakterii fragment bakteryjnego DNA dawcy wraz z genomem faga może wbudować się w genom biorcy, przekazując w ten sposób wyspecyfikowane geny.
Transdukcja specjalizowana ma szczególne znaczenie w rozprzestrzenianiu genów odpowiedzialnych za toksyczność i czynniki wirulencji. Wiele klasycznych toksyn bakteryjnych jest kodowanych przez geny przenoszone właśnie przez profagi. Przykładowo toksyna błonicza u Corynebacterium diphtheriae czy toksyna cholery u Vibrio cholerae są powiązane z obecnością określonych profagów. Bez tych prophagów bakterie byłyby znacznie mniej patogenne.
Transdukcja uwarunkowana i zjawiska pokrewne
Oprócz klasycznej transdukcji ogólnej i specjalizowanej opisano także zjawiska pośrednie, które określa się czasem mianem transdukcji uwarunkowanej lub pośredniej. W zależności od właściwości danego bakteriofaga i organizmu gospodarza mechanizmy pakowania i przenoszenia DNA mogą być modyfikowane. Część fagów preferencyjnie pakuje fragmenty DNA o określonych sekwencjach rozpoznawanych przez ich system pakujący, co powoduje częściową selektywność, choć nie tak ścisłą jak w transdukcji specjalizowanej.
Istnieją również zjawiska z pogranicza transdukcji i plazmidowej wymiany informacji, w których fag przenosi elementy ruchome takie jak transpozony lub integrony. Takie elementy mogą później przeskakiwać pomiędzy różnymi miejscami genomu, potęgując różnorodność genetyczną. Mechanizmy te są skomplikowane, lecz ich wspólną cechą pozostaje udział cząstek wirusowych jako wektorów transferu DNA.
Molekularne mechanizmy transdukcji: od infekcji do rekombinacji
Cykl życiowy bakteriofaga jako podstawa transdukcji
Aby zrozumieć transdukcję, trzeba przyjrzeć się cyklowi życiowemu bakteriofaga. Wirus ten rozpoznaje swojego gospodarza dzięki specyficznym receptorom na powierzchni komórki bakteryjnej, takimi jak białka błonowe, lipopolisacharydy lub kwasy tejchojowe. Po adsorpcji fag wstrzykuje swój genom – DNA lub RNA – do wnętrza komórki, podczas gdy kapsyd pozostaje na zewnątrz.
W cyklu litycznym wprowadzony genom przejmuje kontrolę nad aparatem biosyntezy komórki. Wczesne geny wirusowe kodują białka odpowiedzialne za degradację DNA gospodarza, modyfikację transkrypcji oraz przygotowanie środowiska do syntezy białek późnych. Następnie syntetyzowane są nowe kopie genomu wirusa i białka strukturalne kapsydu oraz ogonka. Ostatnim etapem jest składanie nowych cząstek wirusowych i liza komórki gospodarza, prowadząca do uwolnienia potomnych fagów.
To właśnie na etapie pakowania genomu wirusa i składania kapsydów dochodzi do zjawisk umożliwiających transdukcję. Błędne rozpoznanie fragmentów DNA prowadzi do umieszczenia w kapsydzie cząsteczki bakteryjnego DNA lub kombinacji gospodarza i wirusa. Mechanizmy te zależą od specyfiki systemu pakującego oraz od struktury genomu gospodarza.
Pakowanie DNA i jego błędy
Pakowanie DNA do kapsydu bakteriofaga jest procesem wysoko zorganizowanym. Zwykle rozpoczyna się od rozpoznania specyficznej sekwencji początkowej na genomie wirusa przez kompleks enzymatyczny zawierający m.in. endonukleazy oraz tzw. terminazę. Kompleks ten wiąże DNA, wprowadza je do wnętrza kapsydu, a po osiągnięciu odpowiedniej długości lub specyficznej sekwencji kończącej dokonuje cięcia, zamykając pakiet genetyczny.
W transdukcji ogólnej błędy polegają na tym, że system pakujący rozpoznaje fragment bakteryjnego DNA jako rzekomą sekwencję początkową fagowego genomu. Jeżeli długość pakowanego fragmentu odpowiada pojemności kapsydu, zostaje on ustawiony do końca procesu jako „prawidłowa” nić. W ten sposób powstają cząstki wirusowe, które formalnie są poprawnie zbudowane, ale posiadają zupełnie inny ładunek genetyczny niż oryginalny fag.
W transdukcji specjalizowanej decydujące znaczenie ma etap nieprecyzyjnego wycinania profaga z chromosomu gospodarza. Aktywacja profaga uruchamia zestaw białek wycinających, które zwykle odcinają sekwencję wirusową w ściśle określonych miejscach. Jeśli jednak cięcie nastąpi nieco dalej, zostaje zabrany sąsiadujący gen bakteryjny, a fragment DNA faga pozostaje w genomie bakterii. Tak zmodyfikowany genom wirusa jest następnie powielany i pakowany do nowych kapsydów, stając się nośnikiem wyspecjalizowanych genów bakteryjnych.
Los wprowadzonego DNA w komórce biorcy
Po wniknięciu do komórki biorcy bakteryjne DNA przeniesione przez faga musi zmierzyć się z systemami obronnymi gospodarza. Bakterie dysponują licznymi mechanizmami ochrony przed obcym DNA, takimi jak systemy restrykcyjno-modyfikacyjne czy bardziej złożone systemy CRISPR–Cas. Jeżeli obce DNA zostanie rozpoznane jako niepożądane, może ulec szybkiemu pocięciu i degradacji.
Jeśli jednak fragment DNA przetrwa, może ulec integracji z genomem biorcy. Najczęściej zachodzi to poprzez rekombinację homologiczną, zależną od białek takich jak RecA. Warunkiem jest obecność odpowiednich sekwencji homologicznych pomiędzy wprowadzonym fragmentem a genomem gospodarza. Im większy stopień podobieństwa sekwencji, tym większe prawdopodobieństwo zajścia rekombinacji.
Po włączeniu do genomu nowy fragment może zmienić cechy komórki, np. wprowadzić geny kodujące enzymy metaboliczne, białka błonowe czy czynniki wirulencji. W niektórych przypadkach możliwe jest utrzymywanie się dodatkowego DNA w formie replikonów pozachromosomalnych, jednak klasyczna transdukcja najczęściej kończy się integracją z głównym chromosomem.
Należy podkreślić, że transdukcja nie zawsze prowadzi do stabilnego utrwalenia przeniesionych genów. Wprowadzone fragmenty mogą być niestabilne, ulegać utracie lub mutacjom. Mimo to, w skali populacji bakteryjnej nawet rzadkie udane zdarzenia transdukcji mają ogromne znaczenie dla ewolucji i różnorodności genetycznej.
Znaczenie transdukcji w ewolucji bakterii i medycynie
Rola w horyzontalnym transferze genów
Transdukcja jest jednym z głównych mechanizmów tzw. poziomego, czyli horyzontalnego transferu genów. W przeciwieństwie do pionowego dziedziczenia, gdzie materiał genetyczny przekazywany jest z komórki macierzystej do potomnych, horyzontalny transfer umożliwia wymianę informacji między niespokrewnionymi organizmami, a nawet pomiędzy różnymi gatunkami.
W środowiskach naturalnych, takich jak gleba, woda czy mikrobiom jelitowy, bakterie stale poddawane są presji selekcyjnej. Dostępność substancji odżywczych, obecność toksycznych związków chemicznych czy antybiotyków powodują, że nawet pojedynczy gen mogący zwiększyć przeżywalność organizmu staje się kluczowy. Transdukcja umożliwia szybkie rozprzestrzenianie się takich korzystnych genów w całej społeczności mikroorganizmów.
Do genów szczególnie często przenoszonych należą:
- geny oporności na antybiotyki, w tym β-laktamazy czy modyfikujące rybosomy,
- geny metabolizmu rzadkich lub toksycznych związków chemicznych,
- geny kodujące systemy sekrecyjne i białka umożliwiające kolonizację nowych nisz ekologicznych.
Dzięki transdukcji ewolucja bakterii nie jest jedynie wynikiem spontanicznych mutacji, ale także wynikiem aktywnej wymiany gotowych rozwiązań genetycznych. W perspektywie długoterminowej prowadzi to do złożonych sieci pokrewieństwa genów, w których klasyczne pojęcie „drzewa życia” zastępowane jest pojęciem „sieci życia”, z licznymi połączeniami poprzecznymi.
Transdukcja a oporność na antybiotyki
Rozprzestrzenianie się oporności na antybiotyki jest jednym z największych problemów współczesnej medycyny. Choć koniugacja i plazmidy często są wskazywane jako główni winowajcy, transdukcja odgrywa istotną, nierzadko niedocenianą rolę. Bakteriofagi mogą przenosić geny oporności zapisane zarówno w chromosomie, jak i na mobilnych elementach genetycznych włączonych do genomu gospodarza.
W szpitalnych i środowiskowych zbiorowiskach bakterii obecność fagów umożliwia tworzenie lokalnych „gorących punktów” rekombinacji genów. Bakterie wrażliwe mogą w krótkim czasie nabyć oporność poprzez wbudowanie fragmentów DNA pochodzących z lizy innych bakterii. W dodatku niektóre fagowe geny mogą modulować odpowiedź na stres, zwiększając tolerancję na antybiotyki.
Analizy genomów bakterii patogennych wykazały liczne ślady dawnych wydarzeń transdukcyjnych, w tym regiony zawierające skupiska genów oporności i wirulencji. Obszary takie nazywane są czasem „wyspami patogenności” i często wykazują cechy wskazujące na pochodzenie wirusowe lub plazmidowe. Zrozumienie ich historii ewolucyjnej jest kluczem do opracowywania nowych strategii przeciwdziałania narastającej oporności.
Znaczenie dla powstawania patogenów i wirulencji
Transdukcja odgrywa istotną rolę w kształtowaniu zdolności chorobotwórczych bakterii. Wiele bakterii, które same w sobie są względnie niegroźne, staje się niebezpiecznymi patogenami dopiero po nabyciu określonych genów wirulencji. Fagi działają tu jak wektory przenoszące moduły genowe, które mogą radykalnie zmienić interakcję bakterii z organizmem gospodarza.
Przykłady obejmują:
- przenoszenie genów toksyn enterotoksyn i cytotoksyn,
- przekazywanie genów układów sekrecyjnych typu III i IV, umożliwiających wstrzykiwanie białek efektorowych do komórek gospodarza,
- rozszerzanie repertuaru adhezyn i białek powierzchniowych odpowiadających za przyleganie do tkanek.
Patogenność wielu szczepów Escherichia coli, Staphylococcus aureus czy Streptococcus pyogenes jest w dużej mierze uwarunkowana obecnością konkretnych profagów. Utrata takich elementów może obniżyć wirulencję, co sugeruje, że modulowanie stanu lizogenicznego fagów mogłoby być jednym z kierunków terapii. Jednak manipulacja tymi procesami w organizmach żywych jest skomplikowana i wciąż w dużej mierze pozostaje w sferze badań eksperymentalnych.
Transdukcja w biotechnologii i inżynierii genetycznej
Wykorzystanie fagów jako narzędzi badawczych
Transdukcja, choć naturalnie zachodzi w środowisku, została również zaadaptowana przez naukowców jako narzędzie do manipulacji genami. Już w połowie XX wieku bakteriofagi stały się jednym z podstawowych układów modelowych w genetyce molekularnej. Umożliwiły badania nad naturą genu, replikacją DNA oraz mechanizmami regulacji ekspresji genów.
Za pomocą fagów prowadzi się transfer specyficznych fragmentów DNA pomiędzy szczepami bakterii w celach doświadczalnych. Pozwala to badać funkcje genów poprzez obserwację zmian fenotypowych po ich wprowadzeniu lub wyciszeniu. Fag może działać jak kontrolowany wektor, dostarczający DNA w precyzyjnie zaprojektowanej formie, co przyspiesza konstruowanie mutantów i linii laboratoryjnych o określonych właściwościach.
Systemy fagowe w klonowaniu i edycji genomu
Współczesna biotechnologia wykorzystuje elementy fagowe w zaawansowanych narzędziach inżynierii genetycznej. Przykładem są systemy oparte na fagowych rekombinazach, które umożliwiają precyzyjne wprowadzanie zmian w genomie bakterii oraz innych organizmów. Rekombinazy te rozpoznają określone sekwencje i dokonują ich łączenia lub rozdzielania, co pozwala na kontrolowane modyfikacje struktury DNA.
Kluczowe znaczenie mają także systemy oparte na fagach do wprowadzania bibliotek mutacji, konstrukcji reporterowych czy kasowania genów. W wielu laboratoriach wykorzystuje się tzw. transdukcję P1 u E. coli do szybkiego przenoszenia markerów genetycznych między różnymi liniami tego samego gatunku. Dzięki temu możliwe jest łączenie wielu cech w jednym szczepie bez konieczności wielokrotnego przeprowadzania niezależnych transformacji.
W szerszym kontekście transdukcja przyczyniła się do rozwoju technologii CRISPR–Cas. System ten pierwotnie wyewoluował jako bakteryjny mechanizm obrony przed infekcją fagową. Badania nad interakcjami bakterii i wirusów ujawniły istnienie sekwencji CRISPR służących do pamięci immunologicznej, co później przełożyło się na stworzenie uniwersalnego narzędzia do edycji genomu w wielu organizmach.
Fagoterapia a transdukcja: korzyści i ryzyka
Bakteriofagi są rozważane jako alternatywa lub uzupełnienie dla klasycznych antybiotyków w leczeniu zakażeń bakteryjnych. W fagoterapii wykorzystuje się fagów zdolnych do selektywnego niszczenia patogennych szczepów. Jedną z zalet takiej terapii jest wysoka swoistość w stosunku do określonych bakterii oraz możliwość namnażania się fagów w miejscu zakażenia.
Transdukcja w kontekście fagoterapii jest jednak zjawiskiem ambiwalentnym. Z jednej strony, efektywna liza bakterii przez fagi może przyczyniać się do zmniejszenia liczby komórek opornych. Z drugiej strony, istnieje ryzyko, że fag użyty terapeutycznie będzie w stanie przeprowadzać transdukcję genów oporności lub wirulencji pomiędzy bakteriami obecnymi w organizmie pacjenta. Projektowanie bezpiecznych fagów leczniczych wymaga zatem dokładnej charakterystyki ich potencjału transdukcyjnego oraz starannego wyboru szczepów.
Aktualne strategie obejmują stosowanie fagów ściśle litycznych, które nie integrują się z genomem gospodarza, co ma ograniczać ryzyko transdukcji specjalizowanej. Niemniej nawet fagi lityczne mogą teoretycznie uczestniczyć w transdukcji ogólnej, jeśli w trakcie pakowania DNA dojdzie do błędów. Dalsze badania koncentrują się więc na inżynieryjnym modyfikowaniu systemów pakujących, aby zmniejszyć prawdopodobieństwo włączenia bakteryjskich fragmentów DNA.
Transdukcja poza bakteriami: perspektywy i ograniczenia
Transdukcja u archeonów i różnorodność wirusów prokariotycznych
Choć transdukcja klasycznie kojarzona jest z bakteriami, podobne zjawiska zachodzą także u archeonów – prokariotów zamieszkujących m.in. środowiska ekstremalne. Archealne wirusy często wykazują niezwykłą morfologię i odmienne strategie replikacji, ale w wielu przypadkach również są zdolne do przenoszenia fragmentów DNA gospodarza pomiędzy komórkami.
Różnorodność wirusów infekujących prokarionty znacznie przewyższa liczbę opisanych dotąd gatunków bakterii. Z każdym kolejnym odkrytym fagiem lub wirusem archealnym pojawia się możliwość istnienia nowych, dotąd nieopisanych mechanizmów transferu genów. Badania metagenomiczne środowisk morskich, glebowych i termalnych wskazują, że wirusy stanowią ogromny rezerwuar materiału genetycznego, aktywnie mieszając geny pomiędzy różnymi liniami ewolucyjnymi.
Granice definicji transdukcji w kontekście wirusów eukariotycznych
W przypadku organizmów eukariotycznych termin „transdukcja” bywa używany w innym kontekście, np. sygnalizacji komórkowej, co może prowadzić do nieporozumień. W sensie genetycznym analogią transdukcji bakteryjnej jest transdukcja wirusowa z udziałem wektorów wirusowych stosowanych w terapii genowej. Wektory te bazują na zmodyfikowanych wirusach, zdolnych do wprowadzania określonych genów do komórek ludzkich lub zwierzęcych.
W odróżnieniu od naturalnych fagów, wektory terapeutyczne są projektowane tak, by zminimalizować przypadkowe pakowanie i przenoszenie endogennego DNA gospodarza. Stawia się nacisk na bezpieczeństwo, kontrolę miejsca integracji oraz ograniczenie ryzyka mutagenezy insercyjnej. Mimo podobieństw mechanistycznych, takich jak pakowanie genomu do kapsydu czy integracja z chromosomem, skala i kontekst zastosowań w eukariontach wymaga innego zestawu pojęć i regulacji.
FAQ – najczęściej zadawane pytania o transdukcję genetyczną
Na czym polega podstawowa różnica między transdukcją a transformacją?
Transdukcja i transformacja są dwiema formami poziomego transferu genów, ale różnią się nośnikiem DNA. W transdukcji pośrednikiem jest bakteriofag, który przenosi fragment genomu jednej komórki do drugiej podczas infekcji. W transformacji komórka sama pobiera „nagie” DNA obecne w środowisku, bez udziału wirusa. W efekcie transdukcja jest bardziej ukierunkowana na komórki podatne na danego faga, a transformacja zależy od kompetencji bakteryjnej i warunków otoczenia.
Czy transdukcja zawsze prowadzi do trwałego włączenia nowego DNA?
Nie, wprowadzone podczas transdukcji DNA nie zawsze zostaje trwale zachowane. Po infekcji fagowej obcy fragment może zostać szybko zdegradowany przez systemy obronne bakterii, takie jak enzymy restrykcyjne czy CRISPR–Cas. Do stabilnej integracji dochodzi głównie wtedy, gdy wprowadzone DNA odnajdzie sekwencje homologiczne w genomie gospodarza i ulegnie rekombinacji. Nawet po integracji możliwe jest późniejsze usunięcie lub mutacja takiego fragmentu, więc efekt transdukcji bywa zmienny w czasie.
Dlaczego transdukcja ma tak duże znaczenie dla rozwoju oporności na antybiotyki?
Transdukcja umożliwia szybkie rozprzestrzenianie genów oporności na antybiotyki w populacjach bakteryjnych. Bakteriofagi, infekując liczne komórki, mogą przypadkowo zapakować geny oporności z genomu jednego szczepu i przenieść je do innych, czasem odległych ewolucyjnie. W środowiskach, gdzie obecne są antybiotyki, takie jak szpitale czy fermy hodowlane, nawet rzadkie zdarzenia transdukcyjne są silnie faworyzowane selekcyjnie, co przyspiesza powstawanie wieloopornych patogenów.
Czy transdukcja może występować między różnymi gatunkami bakterii?
Tak, transdukcja międzygatunkowa jest możliwa, choć zwykle mniej wydajna niż w obrębie jednego gatunku. Warunkiem jest zdolność faga do infekowania co najmniej dwóch różnych gatunków lub obecność pokrewnych receptorów na ich powierzchni. Dodatkowo konieczny jest pewien stopień homologii sekwencji, aby wprowadzone DNA mogło ulec rekombinacji. Mimo tych ograniczeń udokumentowano przypadki przenoszenia genów oporności i wirulencji pomiędzy różnymi gatunkami, co zwiększa złożoność sieci ewolucyjnych.
Jak naukowcy wykorzystują transdukcję w laboratorium?
W laboratoriach transdukcję stosuje się głównie do kontrolowanego przenoszenia genów między szczepami bakteryjnymi. Klasycznym narzędziem jest fag P1 w E. coli, który umożliwia szybkie „przesiadanie” markerów genetycznych, takich jak geny oporności czy mutacje delecyjne. Dzięki temu można konstruować szczepy łączące wiele pożądanych cech bez wieloetapowych klonowań. Transdukcja służy też do mapowania genów, analizy funkcji genomu oraz przygotowywania bibliotek mutacyjnych na potrzeby badań funkcjonalnych.