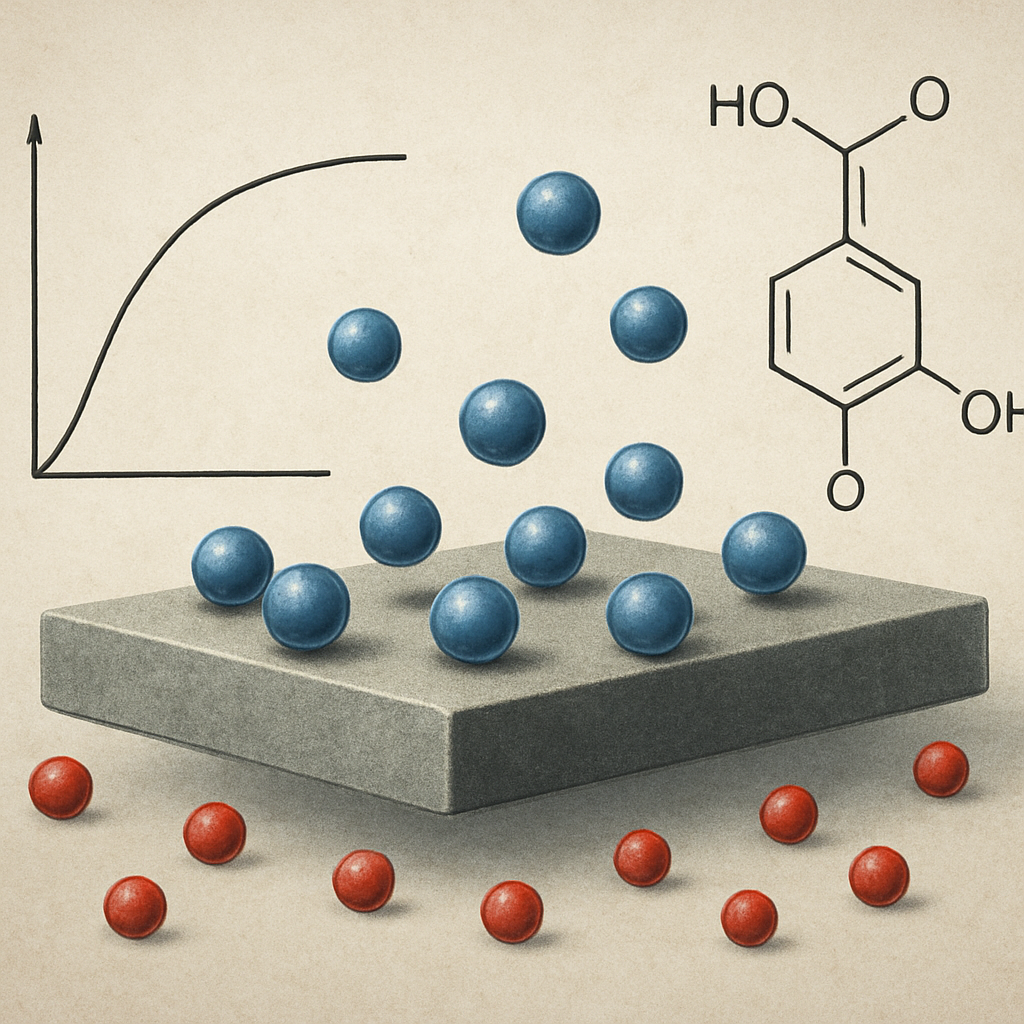
Izoterma Langmuira jest jednym z fundamentalnych narzędzi opisu zjawiska adsorpcji, czyli gromadzenia się cząsteczek na granicy faz, najczęściej na powierzchni ciała stałego stykającego się z gazem lub roztworem. Pozwala ona powiązać ilość zaadsorbowanej substancji z jej stężeniem lub ciśnieniem, a tym samym zrozumieć naturę oddziaływań między cząsteczkami adsorbatu a powierzchnią adsorbentu. Jej matematyczna prostota kryje w sobie szereg założeń fizykochemicznych, które do dziś stanowią punkt odniesienia w chemii powierzchni, katalizie, inżynierii środowiska i technologii materiałów porowatych.
Podstawy zjawiska adsorpcji i rola izoterm
Adsorpcja to proces, w którym cząsteczki jednej fazy (gazowej lub ciekłej) gromadzą się na powierzchni drugiej fazy, najczęściej stałej. W odróżnieniu od absorpcji, gdzie substancja wnika do wnętrza fazy, adsorpcja zachodzi przede wszystkim na powierzchni. Jest to proces o ogromnym znaczeniu praktycznym: od działania katalizatorów heterogenicznych, przez oczyszczanie wody, po magazynowanie wodoru w materiałach porowatych. Aby opisać ilościowo adsorpcję, wprowadza się pojęcie izoterm, czyli zależności między ilością zaadsorbowanej substancji a jej ciśnieniem lub stężeniem w fazie otaczającej przy stałej temperaturze.
Najprostszym i najbardziej klasycznym modelem jest właśnie izoterma Langmuira. Wyprowadzono ją na początku XX wieku, zakładając, że powierzchnia adsorbentu składa się z określonej liczby jednakowych, niezależnych miejsc adsorpcyjnych. Cząsteczka adsorbatu może zająć jedno takie miejsce, tworząc monowarstwę – pojedynczą warstwę cząsteczek na powierzchni. Model ten jest szczególnie użyteczny, gdy interesuje nas właśnie tworzenie monowarstwy, a nie wielowarstwowych filmów, które opisuje się m.in. równaniem BET.
W praktyce inżynierskiej i badaniach laboratoryjnych izoterma Langmuira służy do wyznaczania takich parametrów jak maksymalna pojemność sorpcyjna powierzchni czy efektywne powinowactwo adsorbatu do adsorbentu. Dane te są kluczowe zarówno dla projektowania kolumn adsorpcyjnych, jak i dla analizy struktury nowych materiałów, np. metal–organic frameworks (MOF) lub nowoczesnych węgli aktywnych, których powierzchnia właściwa sięga często tysięcy metrów kwadratowych na gram.
Założenia i matematyczne wyprowadzenie izotermy Langmuira
Kluczowy element zrozumienia izotermy Langmuira stanowią założenia modelu. Są one w pewnym sensie idealizacją rzeczywistości, ale umożliwiają stworzenie prostej i jednocześnie użytecznej zależności między ilością zaadsorbowanej substancji a jej ciśnieniem lub stężeniem. Podstawowe założenia modelu Langmuira można streścić w kilku punktach, które opisują charakter oddziaływań oraz naturę powierzchni.
Najważniejsze założenia modelu
- Powierzchnia adsorbentu jest jednorodna – wszystkie miejsca adsorpcyjne są energetycznie równoważne. Oznacza to, że każda cząsteczka adsorbatu widzi taką samą energię wiązania niezależnie od konkretnej lokalizacji na powierzchni.
- Adsorpcja zachodzi w formie monowarstwy – każdemu miejscu na powierzchni odpowiada co najwyżej jedna cząsteczka adsorbatu. Po zajęciu danego miejsca nie jest możliwe utworzenie nad nim kolejnej warstwy w ramach tego modelu.
- Brak jest oddziaływań bocznych między zaadsorbowanymi cząsteczkami – przyjmuje się, że cząsteczki nie wpływają na siebie wzajemnie, np. nie zmieniają energii adsorpcji sąsiednich miejsc.
- Stan równowagi adsorpcyjno-desorpcyjnej – przy ustalonym ciśnieniu (lub stężeniu) i temperaturze proces adsorpcji i desorpcji przebiega z równymi szybkościami, co umożliwia opis ilościowy przy użyciu stałej równowagi.
- Adsorpcja ma charakter lokalny – każda zaadsorbowana cząsteczka związana jest z konkretnym miejscem, nie dochodzi do swobodnej migracji po powierzchni w sposób naruszający stabilność monowarstwy.
Wyprowadzenie równania izotermy
W języku matematycznym izoterma Langmuira wyraża się równaniem:
q = (qmax · b · p) / (1 + b · p)
gdzie:
- q – ilość substancji zaadsorbowanej na jednostkę masy lub powierzchni adsorbentu,
- qmax – maksymalna pojemność monowarstwowa, odpowiadająca całkowitemu obsadzeniu wszystkich miejsc adsorpcyjnych,
- p – ciśnienie równowagowe adsorbatu w fazie gazowej (lub odpowiednio stężenie C w roztworze, przy modyfikacji równania),
- b – stała równowagi związana z energią adsorpcji, interpretowana często jako miara powinowactwa adsorbatu do powierzchni.
Wyprowadzenie zaczyna się od równania kinetycznego. Szybkość adsorpcji jest proporcjonalna do liczby wolnych miejsc oraz ciśnienia, natomiast szybkość desorpcji do liczby miejsc zajętych. Wprowadza się wielkość θ, oznaczającą ułamek pokrycia powierzchni: θ = q/qmax. Wtedy:
- szybkość adsorpcji: rads = ka · p · (1 − θ),
- szybkość desorpcji: rdes = kd · θ.
W stanie równowagi rads = rdes, zatem:
ka · p · (1 − θ) = kd · θ
Po przekształceniu i wprowadzeniu stałej b = ka/kd otrzymujemy:
θ = (b · p) / (1 + b · p)
Ponieważ q = θ · qmax, podstawienie prowadzi bezpośrednio do znanego równania Langmuira. Jest ono stosunkowo proste, a jednocześnie posiada wyraźną interpretację fizyczną, pozwalając na określenie zarówno parametrów związanych z pojemnością, jak i z energią oddziaływań adsorpcyjnych.
Interpretacja parametrów qmax i b
Parametr qmax odzwierciedla liczbę dostępnych miejsc adsorpcyjnych na powierzchni. W przypadku gazów może być przeliczony na powierzchnię właściwą przy założeniu wielkości cząsteczek i sposobu ich upakowania. Jest zatem bezpośrednio powiązany z tak istotnymi cechami materiałów porowatych jak rozmiar porów, struktura szkieletu oraz stopień rozwinięcia powierzchni. Dla adsorpcji z roztworu qmax określa maksymalne obciążenie materiału sorbującego danym jonem lub cząsteczką.
Stała b jest czułym wskaźnikiem energii oddziaływania. Im większa jej wartość, tym silniejsze jest powinowactwo adsorbatu do powierzchni i tym łatwiej powstaje warstwa adsorpcyjna przy niskich ciśnieniach lub stężeniach. W praktyce, zmiany b z temperaturą pozwalają oszacować efektywną entalpię adsorpcji korzystając z zależności typu van’t Hoffa. Z kolei różnice b dla różnych adsorbatów na tej samej powierzchni mówią wiele o selektywności adsorpcji, co wykorzystuje się w projektowaniu procesów separacyjnych oraz katalizatorów o ukierunkowanej aktywności.
Zastosowania izotermy Langmuira w chemii i technice
Znajomość izoterm adsorpcji oraz umiejętność dopasowania izotermy Langmuira do danych eksperymentalnych stanowi ważne narzędzie w wielu dziedzinach nauk chemicznych i inżynierskich. Model ten, mimo swoich uproszczeń, jest powszechnie używany w analizie procesów sorpcji z gazów i roztworów, w projektowaniu adsorbentów technicznych, a także w interpretacji wyników pomiarów powierzchni właściwej oraz struktury porowatej materiałów.
Kataliza heterogeniczna i powierzchnie aktywne
W katalizie heterogenicznej reakcja chemiczna zachodzi na granicy faz gaz–ciało stałe lub ciecz–ciało stałe. Reagujące cząsteczki muszą najpierw zaadsorbować się na powierzchni katalizatora, następnie przejść szereg przemian elementarnych i ostatecznie ulec desorpcji w formie produktów. Odpowiedni opis adsorpcji reagentów jest więc niezbędny do zrozumienia kinetyki procesu. Izoterma Langmuira służy tu jako podstawa wielu modeli, m.in. mechanizmu Langmuira–Hinshelwooda, w którym zakłada się, że reagujące cząsteczki są zaadsorbowane na tych samych miejscach, oraz mechanizmu Eley’a–Rideala, gdy reaguje cząsteczka zaadsorbowana z cząsteczką z fazy gazowej.
W takich modelach stopień pokrycia powierzchni θ wyrażony równaniem Langmuira wiąże się bezpośrednio z szybkością reakcji. Ostatecznie można uzyskać równania kinetyczne, które opisują zależność szybkości reakcji od ciśnienia reagentów oraz temperatury. Dzięki temu możliwe jest dopasowanie parametrów modelu do wyników eksperymentalnych i ocenienie, które etapy – adsorpcja, reakcja na powierzchni czy desorpcja – kontrolują szybkość procesu. Informacje te są kluczowe przy projektowaniu aktywnych oraz selektywnych katalizatorów do procesów przemysłowych, takich jak reforming parowy, utlenianie czy synteza amoniaku.
Oczyszczanie wody i ścieków
W inżynierii środowiska izoterma Langmuira stosowana jest bardzo często do opisu adsorpcji związków organicznych, jonów metali ciężkich czy barwników na różnego rodzaju sorbentach: węglach aktywnych, zeolitach, biosorbentach pochodzenia roślinnego lub mikrobiologicznego. Doświadczalnie wyznacza się ilość zanieczyszczenia zaadsorbowaną przy różnych stężeniach w roztworze, a następnie dopasowuje równanie Langmuira w wersji „roztworowej”, w której zamiast ciśnienia p występuje stężenie C:
q = (qmax · b · C) / (1 + b · C)
Takie dopasowanie pozwala określić maksymalną pojemność sorpcyjną sorbentu oraz powinowactwo do danego zanieczyszczenia. Uzyskane parametry wykorzystuje się do projektowania kolumn adsorpcyjnych oraz dobierania odpowiedniej masy sorbentu w procesach technologicznych. Porównując qmax i b dla różnych materiałów, można wybrać najbardziej efektywny sorbent dla konkretnych zanieczyszczeń, ocenić ekonomiczną zasadność regeneracji, a także analizować wpływ parametrów środowiskowych, takich jak pH czy zasolenie, na wydajność usuwania szkodliwych substancji.
Charakteryzacja materiałów porowatych i pomiary powierzchni właściwej
Materiały porowate – zeolity, tlenki metali, węgle aktywne, MOF-y, aerogele – charakteryzuje się często poprzez pomiar izoterm adsorpcji gazów, najczęściej azotu w temperaturze ciekłego azotu. Dane te analizuje się przy użyciu różnych modeli, w tym właśnie izotermy Langmuira, aby wyznaczyć parametry charakteryzujące strukturę porów i powierzchnię właściwą. Odpowiednio dopasowana izoterma monowarstwowa pozwala oszacować ilość adsorbatu odpowiadającą pełnemu pokryciu powierzchni monowarstwą, co w połączeniu z geometrycznym modelem cząsteczki adsorbatu prowadzi do wyznaczenia powierzchni właściwej materiału.
Choć w praktyce bardzo często korzysta się z modelu BET, który rozszerza założenia Langmuira na przypadek wielowarstwowej adsorpcji fizycznej, to właśnie parametry wynikające z fazy monowarstwowej mają podstawowe znaczenie w interpretacji wyników. Model Langmuira jest także stosowany w analizie adsorpcji gazów takich jak dwutlenek węgla czy metan na materiałach przeznaczonych do ich magazynowania, gdzie zrozumienie zachowania monowarstwy przy różnych ciśnieniach ma kluczowe znaczenie dla przewidywania pojemności sorpcyjnej pod wysokim ciśnieniem.
Biochemia, powierzchnie biomimetyczne i sensory
Izoterma Langmuira znalazła istotne zastosowanie również w biochemii i naukach o życiu, zwłaszcza w opisie wiązania ligandów do miejsc aktywnych na białkach lub innych makromolekułach o skończonej liczbie miejsc wiążących. Analogiczne równania opisują zależność stopnia obsadzenia receptorów od stężenia ligandu w roztworze, przy czym stała b odpowiada efektywnej stałej asocjacji, a qmax – całkowitej liczbie dostępnych miejsc. Podobne podejście stosuje się w analizie biosensorów, w których warstwy funkcjonalne na powierzchni elektrody lub falowodu optycznego wiążą specyficzne cząsteczki analitu, a zmiana sygnału jest ściśle powiązana ze stopniem pokrycia powierzchni.
Modele oparte na izotermie Langmuira używane są także w opisie monowarstw Langmuira-Blodgett tworzonych na granicy faz ciecz–gaz, gdzie obserwuje się zachowanie uporządkowanych filmów molekularnych przy ściskaniu lub rozciąganiu. Analiza ciśnienia powierzchniowego w funkcji powierzchni przypadającej na cząsteczkę pozwala niekiedy wykorzystać podobne założenia, aby interpretować dane w kontekście uporządkowania, przejść fazowych czy stabilności warstw.
Ograniczenia modelu Langmuira i modyfikacje
Mimo szerokiej użyteczności, model Langmuira jest jedynie przybliżeniem rzeczywistego zachowania układów adsorpcyjnych. Założenia o jednorodności powierzchni, braku oddziaływań bocznych między cząsteczkami oraz ścisłej monowarstwowości rzadko są spełnione w praktyce. Analiza odchyleń od izotermy Langmuira prowadzi jednak do głębszego zrozumienia natury oddziaływań powierzchniowych i do rozwoju bardziej wyrafinowanych modeli.
Niejednorodność powierzchni i oddziaływania boczne
Rzeczywiste powierzchnie ciał stałych, szczególnie materiały porowate, rzadko są jednorodne energetycznie. Obecność defektów, różnych typów centrów aktywnych, zróżnicowanej wielkości i kształtu porów powoduje, że energia adsorpcji zależy od konkretnego miejsca. W efekcie, zamiast jednej wartości b, należałoby rozważać pewien rozkład wartości, co skutkuje nielangmuirowskim kształtem izoterm. Zjawisko to opisują m.in. izotermy Freundlicha czy Sipsa, które uwzględniają heterogeniczność powierzchni przez wprowadzenie dodatkowych parametrów.
Oddziaływania boczne między zaadsorbowanymi cząsteczkami – przyciągające lub odpychające – również naruszają założenie niezależności miejsc adsorpcyjnych. Jeśli cząsteczki przyciągają się, może dochodzić do współadsorpcji w klastrach lub uporządkowanych strukturach, co wpływa na kształt izotermy, szczególnie w zakresie średnich pokryć. W przypadkach istotnych oddziaływań bocznych stosuje się rozszerzone modele, takie jak izoterma Langmuira z parametrem oddziaływań, oparta na koncepcji sieciowych modeli statystycznych.
Przejście do wielowarstwowości i modele rozszerzone
W wielu układach, zwłaszcza przy fizysorpcji gazów w niskich temperaturach, adsorpcja nie ogranicza się do jednej warstwy. Po utworzeniu monowarstwy kolejne cząsteczki mogą przyłączać się nad już zaadsorbowanymi, tworząc wielowarstwowe filmy. Langmuir zakłada brak takiej możliwości, co powoduje, że przy wyższych ciśnieniach model nie opisuje poprawnie danych eksperymentalnych. W odpowiedzi na to opracowano izotermę BET (Brunauera–Emmetta–Tellera), która rozszerza model Langmuira na przypadek wielowarstwowej adsorpcji, przyjmując jednak nadal pewne uproszczenia dotyczące energii oddziaływań w poszczególnych warstwach.
Inne modyfikacje, jak izoterma Tótha lub Redlicha–Petersona, próbują lepiej dopasować się do danych złożonych materiałów porowatych. Mimo to, parametry wyznaczone za pomocą izotermy Langmuira nadal pozostają ważnym punktem odniesienia, szczególnie przy porównywaniu właściwości różnych sorbentów, analizie wstępnej nowych materiałów oraz w dydaktyce, gdzie prostota modelu umożliwia przejrzyste wprowadzenie w tematykę adsorpcji.
Znaczenie izotermy Langmuira jako modelu odniesienia
Niezależnie od ograniczeń, izoterma Langmuira pełni rolę modelu podstawowego, na tle którego ocenia się bardziej złożone opisy. Często stanowi ona pierwszy krok analizy, pozwalający na szybkie oszacowanie pojemności monowarstwowej i powinowactwa adsorbatu, a także na wstępne porównanie różnych systemów adsorpcyjnych. Jej prostota matematyczna umożliwia łatwą liniaryzację i dopasowywanie do danych eksperymentalnych, co jest szczególnie istotne w zastosowaniach inżynierskich.
W wielu obszarach badań, od chemii powierzchni po biochemię receptor–ligand, model Langmuira jest głęboko zakorzeniony nie tylko jako narzędzie obliczeniowe, ale również jako sposób myślenia o zajmowaniu dyskretnych miejsc wiążących na powierzchni czy w makromolekule. Jego wpływ na rozwój chemii fizycznej, inżynierii chemicznej oraz nauk o materiałach jest trudny do przecenienia, a znajomość założeń i interpretacji izotermy Langmuira stanowi ważny element przygotowania każdego, kto zajmuje się projektowaniem procesów sorpcji, katalizatorów i nowoczesnych materiałów porowatych.
FAQ – najczęstsze pytania o izotermę Langmuira
Na czym polega podstawowa różnica między izotermą Langmuira a Freundlicha?
Izoterma Langmuira opiera się na założeniu jednorodnej powierzchni z określoną liczbą równoważnych miejsc adsorpcyjnych oraz tworzeniu monowarstwy. Prowadzi to do istnienia maksymalnej pojemności sorpcyjnej qmax. Izoterma Freundlicha jest empiryczna, nie zakłada istnienia górnej granicy sorpcji i lepiej opisuje heterogeniczne powierzchnie. W praktyce Langmuir ma silniejsze uzasadnienie fizykochemiczne, a Freundlich służy głównie jako wygodna aproksymacja danych.
W jakich warunkach izoterma Langmuira najlepiej opisuje adsorpcję?
Model Langmuira sprawdza się szczególnie dobrze w zakresie umiarkowanych ciśnień lub stężeń, kiedy proces ogranicza się w przybliżeniu do tworzenia monowarstwy, a oddziaływania boczne między cząsteczkami adsorbatu są niewielkie. Typowe przykłady to chemisorpcja reagentów na aktywnych powierzchniach katalizatorów lub selektywna sorpcja jonów na jednorodnych sorbentach. Im bardziej jednorodna energetycznie powierzchnia oraz im dalej od warunków wielowarstwowości, tym lepsze dopasowanie modelu.
Jak praktycznie wyznacza się parametry qmax i b z danych eksperymentalnych?
Najczęściej mierzy się równowagową ilość zaadsorbowanej substancji q przy różnych ciśnieniach p lub stężeniach C, a następnie dopasowuje równanie Langmuira metodą najmniejszych kwadratów. Można skorzystać z nieliniowego dopasowania lub z liniaryzacji, np. w postaci p/q = (1/(b·qmax)) + (p/qmax). Z nachylenia i punktu przecięcia prostej na wykresie p/q względem p wyznacza się qmax oraz b. Nowoczesne podejścia preferują dopasowanie nieliniowe, aby uniknąć artefaktów liniaryzacji.
Dlaczego izoterma Langmuira jest ważna w katalizie heterogenicznej?
W katalizie heterogenicznej szybkość reakcji zależy od liczby cząsteczek reagentów zaadsorbowanych na powierzchni katalizatora. Izoterma Langmuira pozwala powiązać stopień pokrycia powierzchni z ciśnieniem lub stężeniem reagentów, co jest kluczowe przy budowaniu równań kinetycznych, takich jak mechanizm Langmuira–Hinshelwooda. Dzięki temu można przewidywać, jak zmiana warunków procesowych wpłynie na wydajność reakcji, identyfikować etap limitujący oraz porównywać aktywność różnych materiałów katalitycznych w ujednolicony sposób.