Acetylacja histonów jest jednym z kluczowych mechanizmów regulujących aktywność genów w komórkach eukariotycznych. Zrozumienie tego procesu pozwala wyjaśnić, w jaki sposób ta sama informacja genetyczna zawarta w DNA może prowadzić do powstania różnych typów komórek, reagować na sygnały środowiska oraz ulegać zaburzeniom w chorobach, takich jak nowotwory czy zaburzenia neurologiczne. Proces ten należy do szerszej dziedziny badań określanej mianem epigenetyki, która opisuje dziedziczone zmiany funkcji genomu niezwiązane ze zmianami sekwencji nukleotydów DNA.
Budowa chromatyny i rola histonów
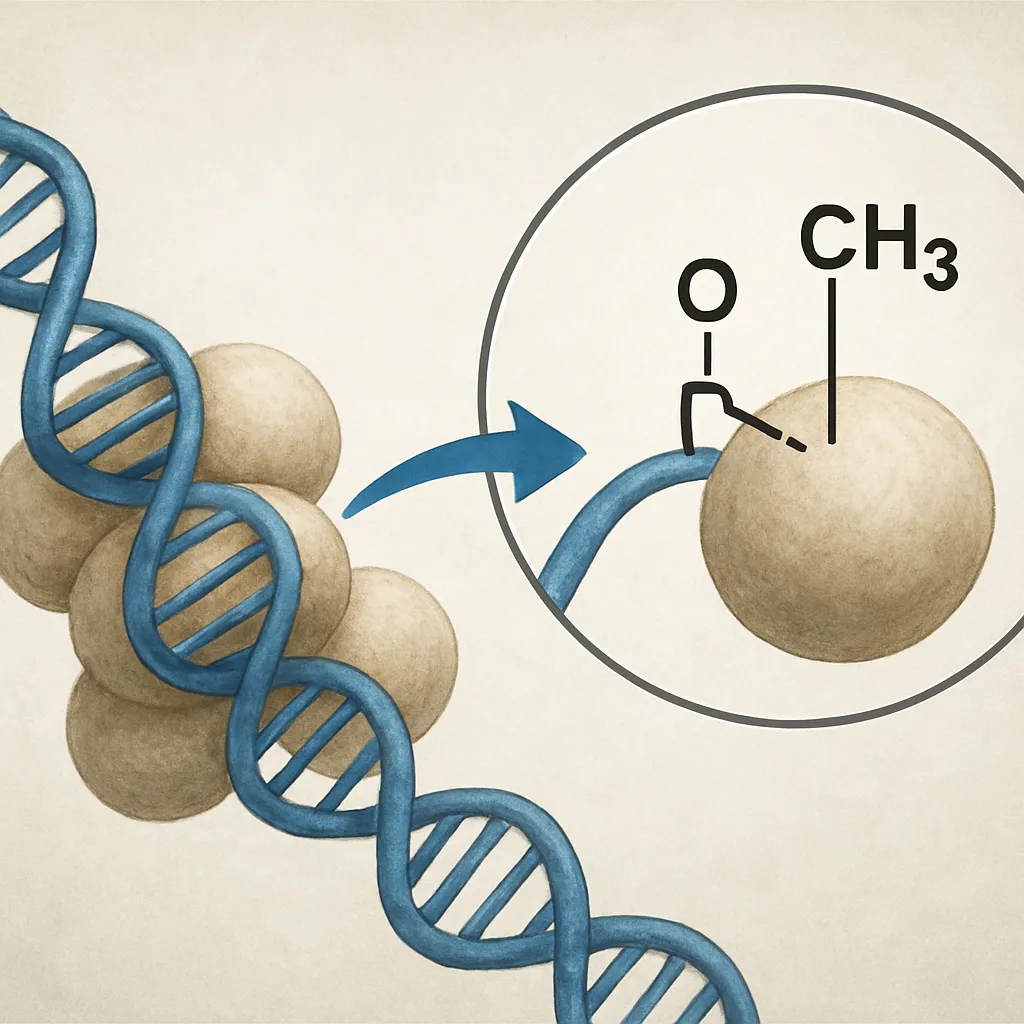
Materiał genetyczny komórek eukariotycznych jest uporządkowany w postaci chromatyny. Podstawową jednostką tej struktury jest nukleosom, złożony z fragmentu DNA owiniętego wokół rdzenia białkowego zbudowanego z histonów. Histony należą do grupy silnie dodatnio naładowanych białek zasadowych, co ułatwia ich oddziaływanie z ujemnie naładowanym DNA. Wyróżnia się cztery główne typy histonów rdzeniowych: H2A, H2B, H3 oraz H4, z których powstaje oktamer histonowy, wokół którego owija się około 147 par zasad DNA.
Oprócz histonów rdzeniowych występuje również histon H1, określany jako histon łącznikowy. Stabilizuje on wyższy poziom organizacji chromatyny, biorąc udział w formowaniu struktury włókna 30-nanometrowego oraz bardziej skondensowanych form. Istotną cechą histonów są ich N-końcowe ogony, wystające poza rdzeń nukleosomu. To właśnie na tych ogonach zachodzi większość modyfikacji potranslacyjnych, w tym acetylacja, metylacja, fosforylacja czy ubikwitynacja.
Chromatyna może występować w dwóch skrajnych stanach funkcjonalnych: jako luźniejsza euchromatyna, związana zazwyczaj z aktywną transkrypcją, oraz jako bardziej skondensowana heterochromatyna, w której geny są na ogół wyciszone. Przejścia między tymi stanami są dynamiczne i regulowane w dużej mierze przez zmiany w strukturze nukleosomów, wynikające z chemicznych modyfikacji histonów. Acetylacja histonów jest jednym z najważniejszych procesów modulujących stopień upakowania chromatyny.
Największe znaczenie dla regulacji genów mają modyfikacje białek histonowych zlokalizowanych w rejonach promotorowych i wzmacniaczowych genów. Obecność specyficznych znaków chemicznych na ogonach histonowych może przyciągać lub odpychać białka regulatorowe, w tym czynniki transkrypcyjne, kompleksy przebudowujące chromatynę oraz elementy maszynerii transkrypcyjnej. W ten sposób decydują one o tym, czy dany gen jest dostępny dla polimerazy RNA II, a więc czy może ulec ekspresji w danej komórce i w danym momencie.
Mechanizm acetylacji histonów
Acetylacja histonów polega na przyłączaniu grupy acetylowej do określonych reszt lizyny w N-końcowych ogonach histonów. Grupa acetylowa pochodzi najczęściej z cząsteczki acetylo-CoA i jest przenoszona na atom azotu w łańcuchu bocznym lizyny. Modyfikacja ta neutralizuje dodatni ładunek reszty lizyny, osłabiając elektrostatyczne oddziaływania między histonami a ujemnie naładowanym DNA. Skutkiem jest rozluźnienie lokalnej struktury chromatyny, które sprzyja dostępowi białek regulacyjnych do sekwencji DNA.
Proces acetylacji jest katalizowany przez enzymy określane jako acetylotransferazy histonowe (HAT, z ang. histone acetyltransferases). Enzymy te znajdują się zwykle w wielobiałkowych kompleksach, co umożliwia precyzyjne kierowanie ich aktywności do określonych rejonów genomu. Wyróżnia się kilka rodzin HAT, różniących się strukturą i specyficznością względem poszczególnych histonów oraz pozycji lizyn. Przykładowo, w komórkach ssaków do ważnych HAT należą białka z rodzin GNAT (np. GCN5), MYST (np. TIP60) oraz p300/CBP.
Reakcja odwrotna, czyli usuwanie grup acetylowych z lizyn histonowych, jest katalizowana przez deacetylazy histonowe (HDAC, z ang. histone deacetylases). Działanie HDAC przywraca dodatni ładunek lizyn, wzmacniając powinowactwo histonów do DNA i promując kondensację chromatyny. Z tego względu HAT i HDAC tworzą dynamicznie równoważący się system regulacyjny, w którym stopień acetylacji histonów jest wypadkową aktywności obu typów enzymów. Liczne kompleksy regulatorowe zawierają zarówno białka rozpoznające określone znaki epigenetyczne, jak i HAT lub HDAC, co pozwala na sprzężenie wielu szlaków sygnałowych.
Ważnym elementem zrozumienia funkcji acetylacji histonów jest koncepcja kodu histonowego. Zakłada ona, że kombinacje różnych modyfikacji (acetylacji, metylacji, fosforylacji i innych) na konkretnych resztach aminokwasowych są odczytywane przez białka zawierające wyspecjalizowane domeny rozpoznające te znaki. W przypadku acetylowanych lizyn kluczową rolę odgrywają białka z domeną bromodomeny, które przyłączają się do takich reszt i rekrutują dalsze czynniki niezbędne do aktywacji transkrypcji. Acetylacja histonów nie działa więc w izolacji, lecz współdziała z innymi modyfikacjami w skomplikowanej sieci epigenetycznej.
Należy podkreślić, że acetylacja histonów może być procesem przejściowym i odwracalnym. Często zmiany w poziomie acetylacji zachodzą szybko w odpowiedzi na sygnały zewnętrzne, takie jak hormony, cytokiny czy stres komórkowy. Dzięki temu możliwe jest krótkotrwałe włączanie lub wyłączanie genów, bez konieczności trwałej modyfikacji sekwencji DNA. Jednocześnie w niektórych przypadkach wzorce acetylacji mogą zostać utrwalone podczas kolejnych podziałów komórkowych, co pomaga zachować stabilną tożsamość komórek w obrębie tkanek.
Znaczenie acetylacji histonów dla ekspresji genów
Najbardziej bezpośrednim skutkiem acetylacji histonów jest zmiana dostępności DNA dla maszynerii transkrypcyjnej. Rozluźnienie struktury chromatyny w obszarach promotorowych umożliwia wiązanie się czynników transkrypcyjnych, kompleksu preinicjacyjnego oraz polimerazy RNA II. Wysoki poziom acetylacji określonych reszt lizyn, zwłaszcza w histonach H3 i H4, jest zazwyczaj markerem aktywnych lub potencjalnie aktywnych genów. Przykładowo, acetylacja lizyny 9 i 14 histonu H3 (H3K9ac, H3K14ac) koreluje z regionami aktywnie transkrybowanymi.
Acetylacja histonów ma również wpływ na inicjację oraz elongację transkrypcji. W początkowych etapach aktywacji genu kompleksy HAT są często rekrutowane przez specyficzne czynniki transkrypcyjne, które rozpoznają sekwencje promotorowe lub wzmacniaczowe. Po związaniu do DNA czynniki te przyciągają HAT, prowadząc do lokalnego zwiększenia acetylacji histonów i otwarcia chromatyny. Gdy promotor staje się dostępny, możliwe jest utworzenie kompleksu preinicjacyjnego z udziałem polimerazy RNA II. W dalszej fazie elongacji utrzymanie stanu rozluźnionej chromatyny ułatwia przenikanie polimerazy przez nukleosomy.
Co istotne, acetylacja histonów nie działa jedynie lokalnie. Zmiany w poziomie acetylacji na większych obszarach chromatyny mogą wpływać na tzw. domeny regulacyjne obejmujące grupy genów. W ten sposób pojedyncze sygnały komórkowe, aktywujące określone HAT lub hamujące HDAC, mogą prowadzić do skoordynowanych zmian ekspresji całych zestawów genów zaangażowanych w ten sam proces biologiczny, np. proliferację, różnicowanie komórkowe lub odpowiedź na stres oksydacyjny.
Istnieje także funkcjonalne sprzężenie między acetylacją histonów a modyfikacjami innych elementów aparatu transkrypcyjnego. Niektóre czynniki transkrypcyjne oraz białka współaktywatorowe ulegają własnej acetylacji, co może zmieniać ich zdolność wiązania DNA, interakcji z innymi białkami czy stabilność. W ten sposób powstają dodatnie pętle sprzężenia zwrotnego, w których acetylacja histonów i czynników transkrypcyjnych nawzajem się wzmacniają, prowadząc do silnej aktywacji wybranych genów docelowych.
Ważnym aspektem jest również udział acetylacji histonów w wyciszaniu genów, choć zjawisko to może wydawać się sprzeczne z ogólną zasadą, że acetylacja sprzyja aktywacji. W niektórych kontekstach komórkowych obecność specyficznych wzorców acetylacji stanowi sygnał rekrutujący białka represyjne lub kompleksy przebudowujące chromatynę, które zmieniają architekturę włókna chromatynowego w kierunku form mniej dostępnych transkrypcyjnie. Pokazuje to, że znaczenie funkcjonalne danej modyfikacji zależy od całego otaczającego kontekstu epigenetycznego.
Acetylacja histonów w rozwoju i różnicowaniu komórek
Podczas rozwoju organizmu wielokomórkowego z pojedynczej zygoty powstaje ogromna różnorodność wyspecjalizowanych typów komórek, takich jak neurony, hepatocyty czy limfocyty. Wszystkie one zawierają zasadniczo tę samą sekwencję DNA, lecz różnią się wzorcami ekspresji genów. Jednym z kluczowych mechanizmów umożliwiających utrwalenie specyficznych profili transkrypcyjnych jest właśnie regulacja epigenetyczna, w tym acetylacja histonów.
W komórkach macierzystych, zwłaszcza pluripotencjalnych, obserwuje się zazwyczaj wysoki poziom acetylacji histonów w rejonach promotorowych licznych genów rozwojowych. Taki stan, określany jako chromatycznie otwarty, umożliwia szybkie włączanie różnych programów różnicowania w odpowiedzi na sygnały zewnętrzne. W miarę specjalizacji komórek część tych regionów ulega odacetylacji i kondensacji, co prowadzi do trwałego wyciszenia genów niewłaściwych dla danej linii komórkowej.
Procesy różnicowania wiążą się z reprogramowaniem całych krajobrazów epigenetycznych, w którym istotną rolę odgrywają rodzinowo specyficzne HAT i HDAC. Przykładowo, w rozwoju układu nerwowego aktywacja genów neuronalnych koreluje ze zwiększeniem acetylacji histonu H3 w promotorach kluczowych regulatorów, podczas gdy geny charakterystyczne dla innych tkanek ulegają odacetylacji. Z kolei w hematopoezie, gdzie powstają różne typy krwinek, odpowiednie kombinacje czynników transkrypcyjnych i enzymów modyfikujących histony determinują los komórek progenitorowych.
Co ważne, zaburzenia w funkcjonowaniu enzymów odpowiedzialnych za acetylację i deacetylację histonów mogą prowadzić do nieprawidłowego przebiegu rozwoju. Mutacje w genach kodujących HAT lub HDAC, a także nieprawidłowa regulacja ich aktywności, zostały powiązane z licznymi zespołami wrodzonymi, charakteryzującymi się opóźnieniem rozwoju, wadami strukturalnymi narządów czy zaburzeniami neurologicznymi. Pokazuje to, że właściwy balans między stanem otwartym a zamkniętym chromatyny jest krytyczny dla prawidłowego formowania się tkanek.
Przeprogramowanie epigenetyczne, obejmujące również zmiany w acetylacji histonów, zachodzi także w procesach takich jak regeneracja tkanek czy indukcja pluripotencjalnych komórek macierzystych z komórek somatycznych. W tych kontekstach celowe modyfikowanie aktywności HAT i HDAC może zwiększać efektywność powrotu komórek do stanu bardziej plastycznego. Dlatego badania nad acetylacją histonów mają znaczenie nie tylko teoretyczne, ale również praktyczne w rozwoju medycyny regeneracyjnej.
Acetylacja histonów a choroby człowieka
Nieprawidłowa regulacja acetylacji histonów została szeroko powiązana z patogenezą wielu chorób, szczególnie nowotworów. W komórkach nowotworowych często obserwuje się globalne zmiany w poziomie acetylacji, jak również specyficzne zaburzenia w rejonach promotorowych genów supresorowych i onkogenów. Nadmierna aktywność niektórych HDAC może prowadzić do odacetylacji i wyciszenia genów hamujących proliferację lub indukujących apoptozę. Z kolei aberrantna aktywność HAT może nadmiernie aktywować ścieżki sprzyjające wzrostowi nowotworu.
Przykładem są ostre białaczki, w których rearanżacje chromosomalne mogą prowadzić do powstania fuzyjnych białek rekrutujących HDAC do promotorów genów koniecznych do różnicowania komórek krwi. Skutkiem jest utrzymanie komórek w stanie niedojrzałym i nadmierna proliferacja. Również w guzach litych, takich jak rak piersi czy rak prostaty, opisano zmienione wzorce acetylacji histonów oraz zaburzenia w ekspresji HAT i HDAC, korelujące z agresywnością choroby i rokowaniem pacjentów.
Acetylacja histonów odgrywa również rolę w chorobach neurodegeneracyjnych i psychiatrycznych. Neurony są szczególnie wrażliwe na zmiany w regulacji epigenetycznej, ponieważ ich plastyczność i zdolność do modyfikacji połączeń synaptycznych zależy od precyzyjnej kontroli ekspresji genów. Zmniejszona acetylacja histonów w określonych regionach mózgu została powiązana z zaburzeniami pamięci i uczenia się w modelach choroby Alzheimera, a także z objawami depresji i zaburzeń lękowych. Co więcej, niektóre leki psychotropowe wpływają pośrednio na aktywność HDAC, co może stanowić jeden z mechanizmów ich działania.
Kolejnym obszarem jest metabolizm i choroby metaboliczne. Ponieważ grupa acetylowa w reakcji acetylacji pochodzi z acetylo-CoA, stan energetyczny komórki i dostępność substratów metabolicznych mogą oddziaływać na poziom acetylacji histonów. Zmiany w diecie, otyłość czy cukrzyca mogą w ten sposób pośrednio wpływać na krajobraz epigenetyczny i regulację genów związanych z gospodarką energetyczną, stanem zapalnym czy stresem oksydacyjnym. Powstaje więc sieć powiązań między środowiskiem, metabolizmem a regulacją epigenetyczną.
Acetylacja histonów uczestniczy ponadto w odpowiedzi immunologicznej i procesach zapalnych. Aktywacja komórek układu odpornościowego, takich jak limfocyty T czy makrofagi, wiąże się z gwałtownymi zmianami w ekspresji licznych genów cytokin, chemokin i receptorów powierzchniowych. Zmiany te są wspomagane przez szybkie przeorganizowanie chromatyny, zależne m.in. od zwiększenia acetylacji histonów w odpowiednich loci. Przewlekłe zaburzenia tej regulacji mogą sprzyjać rozwojowi chorób autoimmunologicznych lub przewlekłych stanów zapalnych.
Farmakologiczna modulacja acetylacji histonów
Odkrycie roli acetylacji histonów w patogenezie chorób otworzyło drogę do rozwoju leków celujących w enzymy HAT i HDAC. Najbardziej zaawansowaną grupą są inhibitory deacetylaz histonowych, które zwiększają globalny poziom acetylacji i mogą reaktywować wyciszone geny supresorowe w komórkach nowotworowych. Część z nich, takich jak vorinostat czy romidepsyna, została już zatwierdzona do leczenia niektórych chłoniaków i innych nowotworów hematologicznych.
Inhibitory HDAC działają, wiążąc się z centrum katalitycznym enzymu i uniemożliwiając usuwanie grup acetylowych z lizyn. Skutkuje to bardziej otwartą strukturą chromatyny, wzrostem ekspresji wybranych genów oraz indukcją różnicowania lub apoptozy komórek nowotworowych. Jednak ze względu na szeroki zakres działania HDAC w różnych typach komórek oraz na inne substraty białkowe, leki te mogą wywoływać działania niepożądane, takie jak zmęczenie, zaburzenia żołądkowo-jelitowe czy mielosupresja. Dlatego intensywnie prowadzi się badania nad bardziej selektywnymi inhibitorami, skierowanymi przeciwko określonym klasom HDAC.
Mniej zaawansowane, ale równie obiecujące są próby opracowania inhibitorów HAT i związków modulujących białka rozpoznające acetylowane lizyny, takie jak bromodomeny. Inhibitory bromodomen (np. BET inhibitors) mogą blokować wiązanie białek regulatorowych z acetylowanymi histonami, co prowadzi do zahamowania ekspresji genów kluczowych dla utrzymania fenotypu nowotworowego. Wstępne badania kliniczne wskazują na potencjał tych leków nie tylko w onkologii, ale także w leczeniu chorób zapalnych czy sercowo-naczyniowych.
Poza klasycznymi małymi cząsteczkami, rozwija się także podejście wykorzystujące cząsteczki hybrydowe, takie jak PROTAC, które mogą selektywnie kierować określone HAT lub HDAC do degradacji w proteasomie. Dzięki temu możliwe jest precyzyjniejsze i odwracalne modulowanie konkretnych elementów maszynerii epigenetycznej. Takie narzędzia mają ogromne znaczenie również w badaniach podstawowych, pozwalając lepiej zrozumieć funkcje poszczególnych enzymów w różnych typach komórek.
Interesującym aspektem jest także wpływ czynników środowiskowych, stylu życia i diety na acetylację histonów. Składniki pożywienia, takie jak kwas masłowy wytwarzany przez mikrobiotę jelitową czy polifenole roślinne, mogą działać jako naturalne modulatory aktywności HDAC lub HAT. Otwiera to perspektywę opracowania interwencji żywieniowych wspierających utrzymanie korzystnego profilu epigenetycznego, choć wymaga to jeszcze wielu badań, aby przełożyć obserwacje laboratoryjne na praktyczne zalecenia kliniczne.
Perspektywy badań nad acetylacją histonów
Dynamiczny rozwój technik biologii molekularnej i genomiki pozwala coraz dokładniej mapować miejsca acetylacji histonów w genomie oraz śledzić zmiany zachodzące w odpowiedzi na różne bodźce. Metody takie jak ChIP-seq umożliwiają globalną analizę rozkładu określonych modyfikacji histonowych, w tym acetylacji wybranych reszt lizyn. Z kolei techniki jednokomórkowe, np. scATAC-seq, pozwalają badać dostępność chromatyny w pojedynczych komórkach, ujawniając heterogeniczność populacji komórkowych w tkankach zdrowych i chorych.
Coraz większe znaczenie zyskują również badania nad współzależnościami między acetylacją histonów a innymi warstwami regulacji epigenetycznej, takimi jak metylacja DNA, modyfikacje innych reszt w histonach czy struktura trójwymiarowa chromatyny. Okazuje się, że pełne zrozumienie regulacji genów wymaga integracji tych danych w spójną całość. W tym celu wykorzystuje się zaawansowane modele obliczeniowe i narzędzia sztucznej inteligencji, które pomagają identyfikować wzorce korelacji między sygnaturami epigenetycznymi a stanami komórkowymi.
Interesującym kierunkiem jest także badanie roli acetylacji histonów w mechanizmach dziedziczenia ponadpokoleniowego. Istnieją przesłanki, że niektóre wzorce modyfikacji histonowych mogą być przekazywane z komórek rozrodczych do zarodka, potencjalnie wpływając na fenotyp kolejnego pokolenia bez zmiany sekwencji DNA. Choć temat ten jest kontrowersyjny i wymaga dalszych potwierdzeń, otwiera fascynujące pytania o wpływ środowiska życia rodziców na epigenom potomstwa.
Rozwój precyzyjnych narzędzi edycji epigenomu, opartych np. na systemie CRISPR połączonym z domenami HAT lub HDAC, umożliwia coraz celniejsze modyfikowanie acetylacji w wybranych loci genomu. Umożliwia to nie tylko badanie przyczynowo-skutkowych związków między konkretnymi zmianami epigenetycznymi a ekspresją genów, ale w przyszłości może prowadzić do tworzenia terapii ukierunkowanych na naprawę nieprawidłowych wzorców acetylacji histonów w określonych chorobach.
FAQ – najczęstsze pytania dotyczące acetylacji histonów
Na czym dokładnie polega acetylacja histonów?
Acetylacja histonów to przyłączanie grupy acetylowej do reszt lizyny w ogonach białek histonowych. Reakcję tę katalizują enzymy nazywane acetylotransferazami histonowymi, wykorzystujące acetylo-CoA jako donor grupy acetylowej. Zmiana ta neutralizuje dodatni ładunek lizyn, osłabia wiązanie histonów z DNA i prowadzi do rozluźnienia struktury chromatyny. Dzięki temu wybrane fragmenty genomu stają się bardziej dostępne dla czynników transkrypcyjnych oraz polimerazy RNA, co zwykle sprzyja aktywacji genów.
Czym różnią się HAT od HDAC i dlaczego równowaga między nimi jest ważna?
HAT (acetylotransferazy histonowe) dodają grupy acetylowe do lizyn histonowych, podczas gdy HDAC (deacetylazy histonowe) usuwają te grupy. HAT zwykle wiążą się z aktywacją transkrypcji, ponieważ rozluźniają chromatynę, natomiast HDAC sprzyjają jej kondensacji i wyciszaniu genów. Równowaga między aktywnością tych enzymów decyduje o tym, które geny są aktywne, a które pozostają zablokowane. Zaburzenie tej homeostazy może prowadzić do chorób, w tym nowotworów, zaburzeń rozwojowych i neurologicznych.
Jak acetylacja histonów wpływa na rozwój organizmu?
Podczas rozwoju organizmu komórki przechodzą z pluripotencjalnych do wyspecjalizowanych, co wymaga trwałego przeprogramowania ekspresji genów. Acetylacja histonów pomaga określić, które geny pozostaną aktywne w danym typie komórki, a które zostaną wyciszone. W komórkach macierzystych wysoki poziom acetylacji utrzymuje chromatynę w stanie bardziej otwartym, umożliwiając elastyczną odpowiedź na sygnały różnicowania. W miarę specjalizacji określone obszary ulegają odacetylacji, stabilizując tożsamość komórkową.
Dlaczego acetylacja histonów jest istotna w nowotworach?
W komórkach nowotworowych często dochodzi do globalnych i lokalnych zaburzeń acetylacji histonów. Nadmierna aktywność deacetylaz może wyciszać geny supresorowe, które normalnie hamują podziały komórkowe lub indukują apoptozę. Z kolei nieprawidłowa aktywność HAT i białek rozpoznających acetylowane lizyny może sprzyjać nadekspresji onkogenów. Takie przesunięcie równowagi w stronę proliferacji i oporności na sygnały śmierci komórkowej stanowi jeden z mechanizmów transformacji nowotworowej.
Czy można celowo wpływać na acetylację histonów w terapii?
Tak, istnieją leki modulujące aktywność enzymów odpowiedzialnych za acetylację histonów. Najlepiej poznane są inhibitory deacetylaz histonowych, które zwiększają poziom acetylacji i mogą reaktywować wyciszone geny supresorowe. Kilka takich preparatów jest już stosowanych w leczeniu niektórych nowotworów hematologicznych. Trwają też badania nad inhibitorami HAT oraz białek rozpoznających acetylowane lizyny, a także nad precyzyjnymi narzędziami edycji epigenomu, co daje nadzieję na bardziej celowane i bezpieczne terapie.