Pojęcie punktu krytycznego zajmuje szczególne miejsce w chemii, fizyce i inżynierii, ponieważ łączy w sobie mikroskopowy obraz materii z jej wyraźnie obserwowalnymi własnościami makroskopowymi. To właśnie w pobliżu parametrów krytycznych substancje zachowują się w sposób skrajnie odmienny od codziennej intuicji: zacierają się granice między fazami, rosną fluktuacje gęstości, a małe zmiany temperatury lub ciśnienia prowadzą do ogromnych efektów. Zrozumienie natury punktu krytycznego pozwala nie tylko pogłębić wiedzę o stanie skupienia materii, ale też projektować zaawansowane technologie separacji, syntezy materiałów oraz nowoczesne procesy w przemyśle chemicznym i farmaceutycznym.
Podstawy pojęcia punktu krytycznego w chemii fizycznej
Punkt krytyczny to szczególny stan substancji, w którym zanikają różnice pomiędzy fazą ciekłą a gazową. W określonej, ściśle zdefiniowanej temperaturze krytycznej Tk i ciśnieniu krytycznym pk granica fazowa przestaje istnieć, a ciecz i para stają się nierozróżnialne. Odpowiada temu konkretna gęstość krytyczna ρk, przy której właściwości układu stają się niezwykle wrażliwe na najmniejsze zakłócenia. Powyżej temperatury krytycznej nie można już skroplić substancji samym zwiększaniem ciśnienia, co ma fundamentalne znaczenie dla termodynamiki i technologii procesowej.
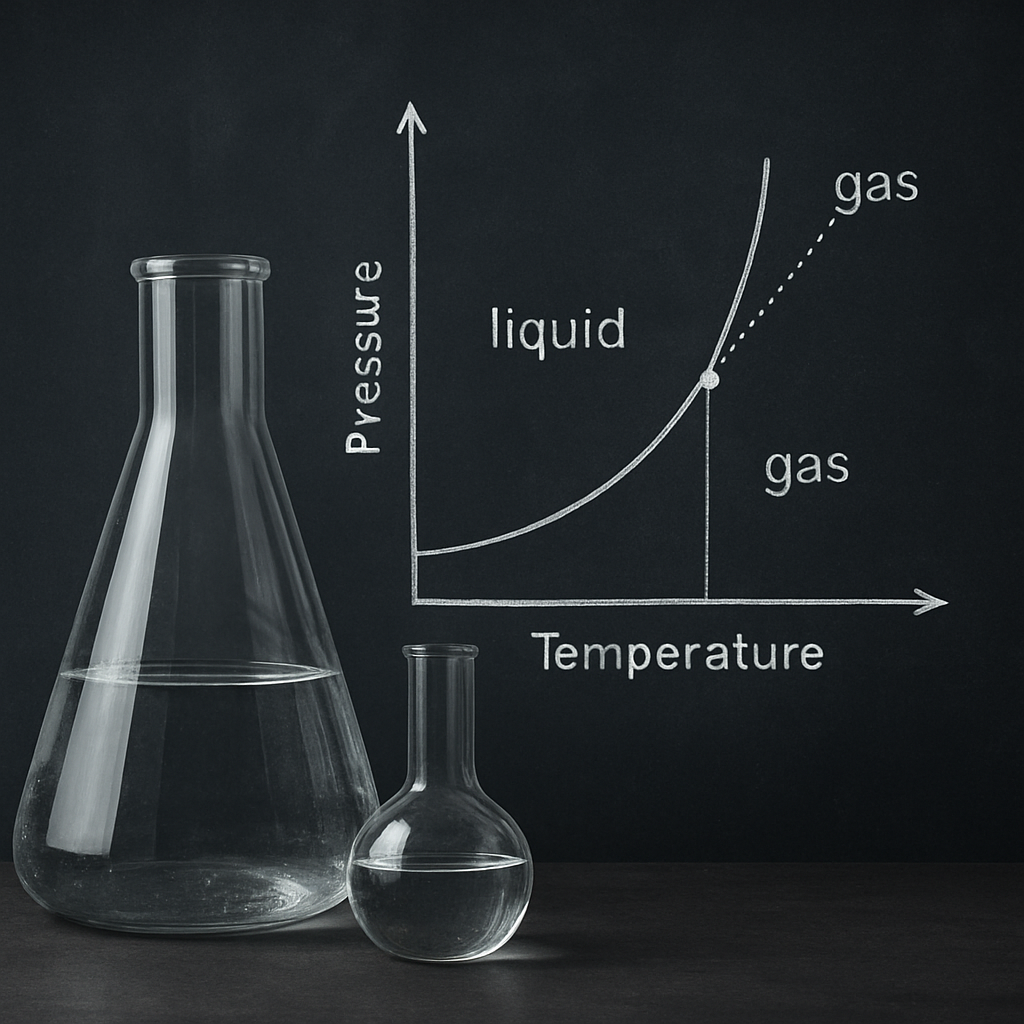
Aby uchwycić istotę tego zjawiska, warto rozważyć klasyczny wykres fazowy p–T. Dla większości substancji pojawia się na nim linia równowagi ciecz–para, kończąca się właśnie w punkcie krytycznym. Poniżej temperatury krytycznej zmiana ciśnienia pozwala przechodzić od cieczy do pary przez wyraźne parowanie i skraplanie; powyżej Tk układ przechodzi w jednorodny, ciągły stan, określany jako płyn nadkrytyczny. Zanik napięcia powierzchniowego sprawia, że nie da się już zdefiniować wyraźnej granicy między fazami, a cały obszar staje się jednorodny fizycznie, choć wciąż może wykazywać silne fluktuacje gęstości.
Z punktu widzenia termodynamiki równowagi, punkt krytyczny to taki stan, w którym pewne pochodne potencjałów termodynamicznych stają się nieskończenie duże lub przyjmują wartości skrajne. W typowym opisie używa się równania stanu, na przykład równania Van der Waalsa, które uwzględnia skończone rozmiary cząsteczek oraz ich wzajemne przyciąganie. W tym formalizmie punkt krytyczny wyznacza się z warunku, że na izotermie krytycznej zanikają pierwsza i druga pochodna ciśnienia względem objętości molowej, co geometrycznie odpowiada punktowi przegięcia o poziomej stycznej.
Istotną rolę odgrywają także wielkości takie jak ściśliwość izotermiczna, pojemność cieplna i przenikalność dielektryczna. W pobliżu punktu krytycznego wiele z nich wykazuje zachowanie osobliwe: dramatycznie rośnie lub maleje, co opisuje się językiem tzw. krytycznych wykładników potęgowych. Te niestandardowe własności sprawiają, że punkt krytyczny jest jednym z najlepszych poligonów doświadczalnych do weryfikacji teorii przejść fazowych i zjawisk krytycznych w fizyce statystycznej.
Modele teoretyczne i własności w pobliżu punktu krytycznego
Za matematyczny opis punktu krytycznego i zachowania substancji w jego otoczeniu odpowiada cała dziedzina zwana teorią zjawisk krytycznych. W podstawowym przybliżeniu korzysta się z uogólnionych równań stanu, takich jak równanie Van der Waalsa, Redlicha-Kwonga, Peng-Robinsona czy bardziej wyrafinowane równania bazujące na teorii perturbacyjnej. Wspólną ich cechą jest wprowadzenie efektywnych parametrów oddziaływań międzycząsteczkowych, które decydują o tym, gdzie w przestrzeni temperatury i ciśnienia pojawi się punkt krytyczny oraz jak będzie wyglądała powierzchnia równowagi fazowej.
Choć proste równania stanu dobrze ilustrują istnienie punktu krytycznego, nie oddają w pełni bogactwa zjawisk krytycznych. W okolicach punktu krytycznego występuje tzw. opalescencja krytyczna, polegająca na silnym rozpraszaniu światła przez fluktuacje gęstości o bardzo dużej długości fali. Makroskopowo substancja zaczyna przypominać migoczący, mętny układ, mimo że formalnie wciąż jest jednorodnym płynem. Zjawisko to tłumaczy się wzrostem korelacji międzycząsteczkowych: cząsteczki przestają zachowywać się niezależnie, a ich ruchy łączą się w rozległe obszary zbiorowej dynamiki.
Kluczowym pojęciem jest długość korelacji, zwykle oznaczana ξ. Mierzy ona zasięg, na jakim cząsteczki oddziałują ze sobą w sposób skorelowany. W pobliżu punktu krytycznego ξ rośnie, dążąc do wartości makroskopowych; opisuje się to za pomocą zależności potęgowych, w których odchylenie temperatury od temperatury krytycznej wchodzi do mianownika. Podobne zależności dotyczą innych wielkości, takich jak podatność, ściśliwość czy ciepło właściwe. Zbiór tych praw nazywa się uniwersalnymi skalowaniami krytycznymi i charakteryzuje się przez współczynniki krytyczne, które okazują się niezależne od szczegółów mikroskopowych konkretnej substancji.
To prowadzi do zaskakującego wniosku: bardzo różne układy fizyczne, od prostych cieczy po skomplikowane magnesy czy polimery, mogą należeć do tych samych klas uniwersalności. Oznacza to, że ich zachowanie w pobliżu punktu krytycznego opisują te same liczby krytyczne i te same funkcje skalujące. W chemii i fizyce materii skondensowanej jest to niezwykle cenne, ponieważ pozwala przewidywać własności złożonych układów na podstawie prostszych modeli, bez konieczności szczegółowego odtwarzania każdego oddziaływania międzycząsteczkowego.
Matematyczne narzędzia używane w tym obszarze obejmują metody grupy renormalizacji, modele sieciowe, takie jak model Isinga, oraz zaawansowane techniki symulacji komputerowych, w tym dynamikę molekularną i Monte Carlo. Szczególnie ważne okazało się wprowadzenie pojęcia skalowania, zgodnie z którym własności układu w różnych skalach długości można przekształcać w siebie za pomocą odpowiednich operacji renormalizacyjnych. To właśnie te metody pozwoliły wyjaśnić, dlaczego wartość niektórych eksponentów krytycznych jest identyczna dla różnych substancji, jeśli tylko podlegają one temu samemu mechanizmowi przejścia fazowego.
W praktyce inżynierskiej i laboratoryjnej nie zawsze interesuje nas sam punkt krytyczny, ale także linia krytyczna w mieszaninach wieloskładnikowych oraz tak zwane pseudokrytyczne zachowanie przy zmiennym składzie. W przypadku mieszanin dwuskładnikowych można zaobserwować bogate diagramy fazowe, w których pojawiają się zarówno górne, jak i dolne krytyczne temperatury rozpuszczalności. W takich układach dochodzi do powstawania zjawisk krytycznych nie tylko pomiędzy fazą ciekłą a gazową, ale również pomiędzy dwiema niemieszającymi się cieczami, co dodatkowo komplikuje opis teoretyczny, a jednocześnie otwiera drogę do bardziej wyszukanych zastosowań w procesach separacyjnych.
Płyny nadkrytyczne i zastosowania technologiczne punktu krytycznego
Bezpośrednim następstwem istnienia punktu krytycznego jest możliwość otrzymania płynu nadkrytycznego, czyli stanu materii występującego powyżej temperatury i ciśnienia krytycznego. W tym obszarze układ łączy cechy, które w warunkach normalnych traktujemy jako właściwe oddzielnie dla gazu i cieczy. Płyn nadkrytyczny charakteryzuje się gęstością zbliżoną do cieczy, a jednocześnie zachowuje wysoką dyfuzyjność i niską lepkość typową dla gazów. Ta kombinacja własności sprawia, że staje się on doskonałym medium do ekstrakcji, transportu masy i ciepła oraz selektywnego rozpuszczania związków chemicznych.
Najbardziej znanym i rozpowszechnionym technologicznie przykładem jest nadkrytyczny dwutlenek węgla. Jego stosunkowo niska temperatura krytyczna (ok. 31 °C) i umiarkowane ciśnienie krytyczne (ok. 7,4 MPa) sprawiają, że może być łatwo generowany i wykorzystywany w warunkach przemysłowych. Nadkrytyczny CO2 jest chemicznie obojętny, nietoksyczny, niepalny i łatwo usuwalny po procesie dzięki prostemu obniżeniu ciśnienia, co czyni go doskonałym rozpuszczalnikiem w tzw. zielonej chemii. Znalazł on zastosowanie w ekstrakcji superkrytycznej, m.in. przy usuwaniu kofeiny z kawy, odzyskiwaniu olejków eterycznych, oczyszczaniu farmaceutyków czy przetwarzaniu produktów spożywczych.
Mechanizm ekstrakcji nadkrytycznej wykorzystuje fakt, że własności rozpuszczalnika można precyzyjnie modulować poprzez zmianę ciśnienia i temperatury w obszarze nadkrytycznym. Niewielkie zwiększenie ciśnienia może istotnie podnieść gęstość nadkrytycznego CO2, a co za tym idzie – jego siłę rozpuszczającą względem związków hydrofobowych. Jednocześnie obniżenie ciśnienia na późniejszym etapie procesu prowadzi do gwałtownej utraty zdolności rozpuszczania i wytrącenia się ekstrahowanej substancji, co umożliwia jej łagodne odzyskanie bez konieczności stosowania wysokich temperatur czy agresywnych rozpuszczalników organicznych.
Innym ważnym obszarem zastosowań punktu krytycznego jest suszenie nadkrytyczne. Klasyczne suszenie cieczy, np. wody, wymaga przejścia przez granicę faz ciecz–gaz, co wiąże się z działaniem napięcia powierzchniowego i może prowadzić do zniszczenia delikatnych struktur porowatych. W przypadku suszenia nadkrytycznego ciecz jest najpierw doprowadzana do stanu nadkrytycznego, a następnie stopniowo obniża się ciśnienie, tak aby nie przechodzić przez linię przemiany fazowej. Dzięki temu unika się tworzenia menisków kapilarnych i związanych z nimi sił kapilarnych, co pozwala zachować strukturę materiału. Technika ta stosowana jest w otrzymywaniu aerżeli, zaawansowanych materiałów izolacyjnych, katalizatorów i biomateriałów.
Znajomość parametrów krytycznych i zachowania substancji w ich pobliżu ma również kluczowe znaczenie w projektowaniu aparatury wysokociśnieniowej. Reaktory, autoklawy, kolumny ekstrakcyjne czy wymienniki ciepła muszą być konstruowane z uwzględnieniem zarówno mechanicznej wytrzymałości, jak i bezpieczeństwa procesu, a także zmienności własności fizykochemicznych medium roboczego. W pobliżu punktu krytycznego przewodnictwo cieplne, lepkość, ściśliwość czy współczynniki przewodzenia masy mogą zmieniać się w sposób nieliniowy, co wymaga użycia zaawansowanych modeli obliczeniowych i precyzyjnych danych eksperymentalnych.
Zaawansowane zastosowania obejmują także wykorzystanie płynów nadkrytycznych w syntezie nanomateriałów, modyfikacji powierzchni, polimeryzacji oraz w procesach katalitycznych. Wysoka przenikalność do porowatych struktur, możliwość regulacji siły rozpuszczającej oraz specyficzne oddziaływania z polimerami pozwalają projektować procesy, w których tradycyjne rozpuszczalniki organiczne byłyby zbyt toksyczne, niestabilne lub mało efektywne. Łączenie wiedzy o punkcie krytycznym z inżynierią reakcji i projektowaniem materiałów otwiera drogę do tworzenia technologii przyjaznych środowisku i efektywnych energetycznie.
Nie należy zapominać, że punkt krytyczny odgrywa również ważną rolę w geochemii i naukach o Ziemi. W ekstremalnych warunkach panujących w głębokich partiach skorupy i płaszcza Ziemi woda, dwutlenek węgla oraz inne lotne składniki mogą występować w stanach zbliżonych do nadkrytycznych. Ich zdolność do rozpuszczania minerałów i transportu pierwiastków śladowych ma wpływ na powstawanie złóż rud metali, krążenie substancji w systemach hydrotermalnych oraz dynamikę geochemiczną planet. Z kolei w astrofizyce pojęcie punktu krytycznego rozszerza się na bardziej egzotyczne formy materii, choć podstawowe idee związane z zanikiem granic fazowych i pojawieniem się uniwersalnego zachowania pozostają podobne.
Eksperyment, pomiar i praktyczne wyznaczanie punktów krytycznych
Wyznaczanie punktu krytycznego substancji w warunkach laboratoryjnych jest zadaniem wymagającym precyzji, ale dostępnym dla dobrze wyposażonych laboratoriów chemii fizycznej. W przypadku prostych substancji czystych, takich jak CO2, etan czy woda, klasyczne metody opierają się na obserwacji zanikania menisku pomiędzy fazą ciekłą a gazową w przezroczystej komorze wysokociśnieniowej. W miarę zbliżania się do temperatury krytycznej i odpowiedniego regulowania ciśnienia menisk staje się coraz mniej wyraźny, aż w pewnym momencie całkowicie znika. Temperatura i ciśnienie w tym punkcie są przyjmowane jako przybliżone wartości krytyczne.
Dokładniejsze metody wykorzystują pomiar własności fizycznych, które w pobliżu punktu krytycznego wykazują charakterystyczne zmiany. Można na przykład badać gęstość cieczy i pary w funkcji temperatury i ciśnienia oraz analizować ich zbieganie się do wspólnej wartości krytycznej. Inną możliwością jest precyzyjne wyznaczanie ściśliwości izotermicznej z pomiarów objętości w funkcji ciśnienia. Blisko punktu krytycznego ściśliwość gwałtownie rośnie, co ułatwia identyfikację tego obszaru. Stosuje się również pomiar przenikalności dielektrycznej, współczynników załamania światła czy przewodności elektrycznej, które reagują na rosnące fluktuacje gęstości i składu.
Nowoczesne techniki eksperymentalne coraz częściej wspiera się symulacjami komputerowymi, które pozwalają przewidywać zachowanie złożonych układów, zwłaszcza mieszanin wieloskładnikowych i roztworów polimerowych. Dynamika molekularna, symulacje Monte Carlo oraz metody pola średniego zapewniają możliwość obliczania temperatury i ciśnienia krytycznego na podstawie znanych potencjałów oddziaływania międzycząsteczkowego. Choć wyniki takich obliczeń wymagają zawsze weryfikacji eksperymentalnej, stanowią one cenne narzędzie wstępnego projektowania procesów, w których kluczową rolę odgrywają parametry krytyczne.
Wyzwaniem jest także wyznaczanie punktów krytycznych w mieszaninach. W układach dwuskładnikowych lub wieloskładnikowych obok klasycznego punktu krytycznego ciecz–para pojawiają się dodatkowe zjawiska, takie jak krytyczne punkty rozpuszczalności, azeotropy krytyczne czy linie krytyczne. Eksperymentalne badanie takich układów wymaga łączenia technik równowagi fazowej z analizą składu poszczególnych faz, np. chromatografią gazową, spektroskopią czy analizą termiczną. W celu interpretacji wyników korzysta się z rozbudowanych modeli termodynamicznych, takich jak równania stanu obejmujące oddziaływania specyficzne czy teorie nadmiarowej energii swobodnej.
W praktyce przemysłowej istotne jest również określenie tzw. pseudokrytycznych własności mieszanin gazów. W wielu zastosowaniach inżynierskich, np. w projektowaniu rurociągów, wymienników ciepła czy instalacji kriogenicznych, mieszaniny są traktowane jako gazy pseudoczyste, dla których można zdefiniować efektywną temperaturę i ciśnienie krytyczne. Dane te następnie służą do przybliżonego obliczania współczynników transportu, entalpii czy pojemności cieplnych, co znacznie upraszcza obliczenia, choć wymaga ostrożności w interpretacji, zwłaszcza w obszarach silnie zbliżonych do rzeczywistych punktów krytycznych składników.
Bezpieczeństwo pracy z układami bliskimi stanowi krytycznemu wymaga szczególnej uwagi. Duże wartości ściśliwości i podatności na niewielkie zmiany parametrów mogą prowadzić do gwałtownych odpowiedzi układu na drobne zaburzenia. Wysokie ciśnienia, wymagane do osiągnięcia stanów nadkrytycznych, wiążą się z ryzykiem mechanicznym, a zmiany fazowe mogą powodować gwałtowne rozprężenie lub niekontrolowane powstawanie pęcherzyków. Dlatego wszystkie urządzenia operujące w pobliżu punktów krytycznych muszą być wyposażone w odpowiednie systemy zabezpieczeń, zawory bezpieczeństwa, czujniki ciśnienia i temperatury oraz procedury awaryjne.
Z chemicznego punktu widzenia badanie punktu krytycznego dostarcza unikalnej wiedzy na temat natury oddziaływań międzycząsteczkowych. Położenie parametrów krytycznych w układzie p–T jest ściśle związane z siłą i zasięgiem sił przyciągających i odpychających pomiędzy cząsteczkami. Porównując wartości temperatury i ciśnienia krytycznego dla różnych substancji, można wnioskować o ich polaryzowalności, obecności wiązań wodorowych, oddziaływań elektrostatycznych czy efektów kształtu cząsteczki. Dzięki temu analiza krytyczna staje się narzędziem do pośredniego badania struktury i własności molekularnych, uzupełniającym klasyczne techniki spektroskopowe i dyfrakcyjne.
FAQ – najczęściej zadawane pytania
Co to jest punkt krytyczny w chemii?
Punkt krytyczny w chemii to specyficzna kombinacja temperatury, ciśnienia i gęstości, przy której zanika granica między fazą ciekłą a gazową danej substancji. Oznacza to, że nie można rozróżnić, czy mamy do czynienia z cieczą, czy z parą, ponieważ ich właściwości stają się identyczne. Powyżej tej temperatury nie da się już skroplić substancji samym zwiększaniem ciśnienia, a powyżej ciśnienia krytycznego nie obserwuje się klasycznej przemiany fazowej ciecz–gaz.
Czym różni się płyn nadkrytyczny od zwykłej cieczy i gazu?
Płyn nadkrytyczny występuje, gdy temperatura i ciśnienie przekraczają wartości krytyczne danej substancji. Łączy cechy cieczy i gazu: ma gęstość zbliżoną do cieczy, a jednocześnie wysoką dyfuzyjność i niską lepkość podobną do gazu. Brak jest w nim wyraźnej granicy faz, czyli menisku. Dzięki temu płyny nadkrytyczne mogą łatwo penetrować porowate materiały, skutecznie rozpuszczać wybrane związki i być wykorzystywane jako regulowane, “dostrajane” rozpuszczalniki procesowe.
Dlaczego punkt krytyczny jest ważny w przemyśle chemicznym?
Punkt krytyczny wyznacza obszar, w którym można tworzyć i stosować płyny nadkrytyczne, szczególnie cenione w nowoczesnych technologiach. Pozwala to projektować procesy ekstrakcji, oczyszczania i suszenia, w których uzyskuje się wysoką selektywność i wydajność przy mniejszym zużyciu energii oraz ograniczonym użyciu toksycznych rozpuszczalników. Przykładem jest nadkrytyczny CO₂ stosowany do dekofeinizacji kawy, pozyskiwania olejków czy w przetwórstwie farmaceutycznym i tworzyw sztucznych.
Jak eksperymentalnie wyznacza się punkt krytyczny substancji?
Punkt krytyczny wyznacza się, obserwując zanikanie menisku między cieczą a parą w przezroczystej komorze wysokociśnieniowej przy kontroli temperatury i ciśnienia. Dodatkowo mierzy się gęstości obu faz, ściśliwość, własności optyczne czy przenikalność dielektryczną, śledząc ich gwałtowne zmiany w pobliżu parametrów krytycznych. Współcześnie dane eksperymentalne często uzupełnia się symulacjami komputerowymi i modelami termodynamicznymi, co zacieśnia zakres niepewności i umożliwia przewidywanie zachowania mieszanin.
Jakie są najczęstsze zastosowania nadkrytycznego CO₂?
Nadkrytyczny CO₂ jest wykorzystywany przede wszystkim w ekstrakcji superkrytycznej do usuwania kofeiny z kawy i herbaty, odzyskiwania olejków eterycznych, frakcjonowania tłuszczów oraz oczyszczania substancji aktywnych w farmacji. Stosuje się go także w suszeniu nadkrytycznym do otrzymywania delikatnych materiałów porowatych i aerżeli, w modyfikacji powierzchni polimerów oraz jako alternatywny, bardziej przyjazny środowisku rozpuszczalnik, zastępujący tradycyjne rozpuszczalniki organiczne w wybranych procesach technologicznych.