Gradient protonowy stanowi jedno z fundamentalnych zjawisk bioenergetycznych, dzięki któremu komórki żywych organizmów mogą przekształcać energię chemiczną w użyteczną formę. To właśnie ten proces umożliwia wytwarzanie większości cząsteczek ATP, głównego nośnika energii w komórce. Zrozumienie natury gradientu protonowego, sposobu jego powstawania oraz roli w funkcjonowaniu mitochondriów, chloroplastów i błon komórkowych jest kluczowe dla współczesnej biologii, biochemii i medycyny.
Istota gradientu protonowego i jego znaczenie bioenergetyczne
Gradient protonowy to różnica stężeń jonów wodorowych (protonów, H⁺) po dwóch stronach błony biologicznej. Najczęściej opisuje się go na przykładzie wewnętrznej błony mitochondrium, błon tylakoidów w chloroplastach oraz błon komórek bakteryjnych. Różnica ta ma charakter zarówno chemiczny (odmienna liczba protonów), jak i elektryczny (różnica ładunków), dlatego mówimy o potencjale elektrochemicznym protonów.
W strukturach komórkowych gradient protonowy powstaje wtedy, gdy wyspecjalizowane kompleksy białkowe, działające jak pompy, przemieszczają protony wbrew ich naturalnemu kierunkowi dyfuzji. Wymaga to zużycia energii, zazwyczaj pochodzącej z reakcji utleniania związków organicznych lub z absorpcji światła. W rezultacie po jednej stronie błony gromadzi się większe stężenie protonów niż po drugiej. Powstała różnica tworzy rodzaj potencjalnej energii, określanej często jako siła protonomotoryczna.
Koncept gradientu protonowego został ujęty teoretycznie w hipotezie chemiosmotycznej zaproponowanej przez Petera Mitchella. Według tego ujęcia, energia z reakcji utleniania w łańcuchu oddechowym nie jest przekazywana bezpośrednio na syntezę ATP, ale najpierw wykorzystywana do pompowania protonów przez błonę. Dopiero ich powrotny przepływ zgodnie z gradientem jest sprzężony z syntezą ATP przez kompleks syntazy ATP.
Znaczenie gradientu protonowego można porównać do wody spiętrzonej za tamą. Sama różnica poziomów wody nie wykonuje jeszcze pracy mechanicznej, ale stworzone warunki potencjalnie ją umożliwiają. W komórce tę rolę pełni różnica stężeń protonów i potencjał elektryczny. Gdy protony mają możliwość kontrolowanego przepływu przez określone kanały białkowe, ich ruch zostaje przekształcony w przydatną energię chemiczną, mechaniczną lub transportową.
Na poziomie organizmu gradient protonowy jest absolutnie niezbędny do podtrzymania życia. Znacząca część metabolizmu – od oddychania komórkowego u zwierząt, po fotosyntezę u roślin – opiera się na tworzeniu i wykorzystywaniu gradientów protonowych. Bez tych delikatnie regulowanych różnic stężeń komórki nie byłyby w stanie utrzymać homeostazy, prowadzić aktywnego transportu ani przeprowadzać wielu reakcji biochemicznych wymagających dostaw energii.
Powstawanie gradientu protonowego: pompy, łańcuchy oddechowe i fotosynteza
Głównym miejscem powstawania gradientu protonowego w komórkach eukariotycznych są mitochondria, określane często mianem elektrowni komórkowych. W ich wewnętrznej błonie zlokalizowany jest łańcuch transportu elektronów, złożony z szeregu kompleksów białkowych. Kompleksy te przyjmują elektrony z NADH i FADH₂, powstających w procesach takich jak glikoliza czy cykl kwasu cytrynowego, a następnie przekazują je kolejnym przenośnikom, aż do tlenu cząsteczkowego.
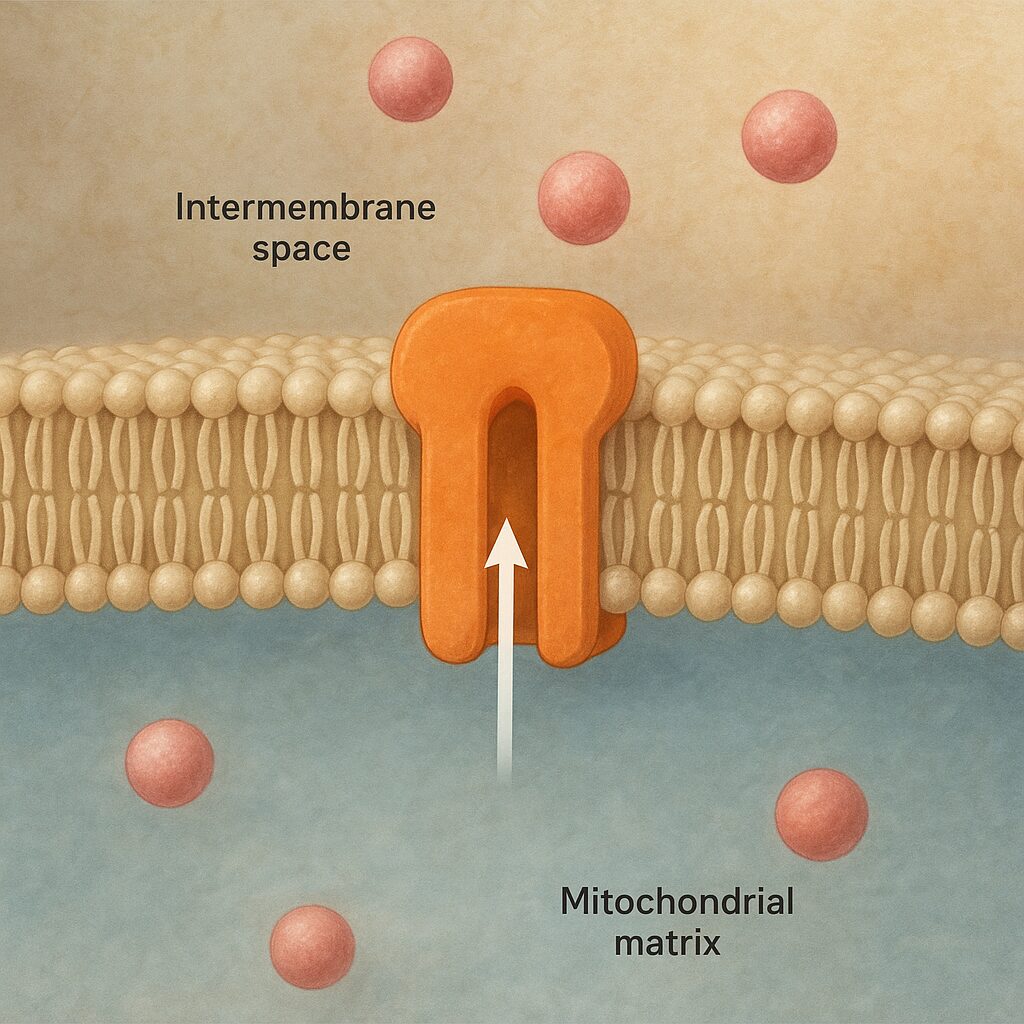
Podczas przepływu elektronów uwalnia się energia, która nie jest tracona w postaci ciepła, lecz wykorzystywana do aktywnego pompowania protonów z macierzy mitochondrialnej do przestrzeni międzybłonowej. Tworzy się w ten sposób różnica stężeń protonów: ich nadmiar pojawia się po stronie przestrzeni międzybłonowej, a niedobór w macierzy. Równocześnie powstaje różnica ładunków, ponieważ protony wnoszą dodatni ładunek elektryczny. Łącznie decyduje to o wielkości wytworzonej siły protonomotorycznej.
Proces ten można przedstawić w kilku krokach:
- utlenianie substratów odżywczych prowadzi do redukcji przenośników NAD⁺ i FAD do NADH i FADH₂
- NADH i FADH₂ przekazują elektrony do łańcucha transportu elektronów w błonie
- energia uwalniana z przepływu elektronów jest wykorzystywana do pompowania protonów przez błonę
- narasta gradient elektrochemiczny protonów
W chloroplastach, w trakcie fotosyntezy, gradient protonowy powstaje w wyniku działania dwóch fotosystemów umieszczonych w błonie tylakoidów. Światło wzbudza elektrony w barwnikach chlorofilowych, które następnie przechodzą przez łańcuch przenośników. Równocześnie zachodzi fotoliza wody, prowadząca do uwolnienia protonów do wnętrza tylakoidów. Połączenie pompowania protonów z cyklu transportu elektronów i ich uwalniania z wody tworzy znaczny gradient pomiędzy światłem tylakoidów a stromą chloroplastów.
W organizmach prokariotycznych, takich jak bakterie, gradient protonowy jest tworzony bezpośrednio na błonie komórkowej. Ponieważ bakterie nie mają oddzielnych organelli z własnymi błonami wewnętrznymi, cała maszyneria transportu elektronów i pomp protonowych znajduje się właśnie tam. U bakterii tlenowych ostatnim akceptorem elektronów jest tlen, natomiast wiele bakterii beztlenowych wykorzystuje inne cząsteczki, jak azotany, siarczany czy dwutlenek węgla, ale mechanizm pompowania protonów pozostaje kluczowy.
Oprócz łańcuchów oddechowych i fotosyntetycznych, istotną rolę odgrywają również inne białka błonowe, jak ATP-azy działające jako pompy protonowe napędzane hydrolizą ATP, czy pompy sprzężone z transportem sodu. W niektórych tkankach gradient protonowy może także powstawać dzięki aktywności specyficznych białek rozprzęgających, które modulują przepływ protonów i przekształcają część energii w ciepło, co ma znaczenie np. w termogenezie u ssaków.
Istotne jest, że utrzymanie gradientu protonowego wymaga ciągłego dopływu energii i nieustannego działania pomp. Komórki inwestują w to znaczną część potencjału metabolicznego. Bez stałego zasilania w substraty oddechowe gradient uległby wyrównaniu w wyniku dyfuzji i ruchów termicznych, a komórka straciłaby zdolność syntezy ATP i aktywnego transportu.
Wykorzystanie gradientu protonowego: synteza ATP, transport i regulacja komórkowa
Najbardziej znanym sposobem wykorzystania gradientu protonowego jest synteza ATP przez syntazę ATP. Jest to złożony kompleks białkowy, który działa jak molekularny silnik obrotowy. Część błonowa enzymu tworzy kanał dla protonów, natomiast część wystająca do macierzy cytoplazmatycznej lub mitochondrialnej jest miejscem syntezy ATP. Gdy protony przepływają przez kanał zgodnie z gradientem, powodują rotację elementów białka. Ruch obrotowy wywołuje zmiany konformacji w miejscach aktywnych, co umożliwia połączenie ADP i nieorganicznego fosforanu w cząsteczkę ATP.
Mechanizm ten jest niezwykle wydajny energetycznie. Szacuje się, że podczas pełnego utlenienia jednej cząsteczki glukozy w łańcuchu oddechowym powstaje kilkadziesiąt cząsteczek ATP, a kluczową rolę odgrywa właśnie sprzężenie gradientu protonowego z działaniem syntazy ATP. Bez tego sprzężenia energia z utleniania substancji odżywczych byłaby w dużej mierze rozpraszana w postaci ciepła.
Gradient protonowy jest również źródłem siły napędowej dla aktywnego transportu różnych jonów i cząsteczek przez błony biologiczne. Białka transportujące mogą wykorzystywać przepływ protonów do przemieszczenia innych substancji wbrew ich własnemu gradientowi stężeń. Przykładem są symportery i antyportery protonowe, które sprzęgają ruch protonów z transportem cukrów, aminokwasów czy jonów metali. W ten sposób gradient protonowy, oprócz roli w syntezie ATP, staje się uniwersalnym źródłem energii dla ruchu substancji w komórce.
Istnienie gradientu protonowego wpływa również na pH różnych przedziałów komórkowych. Na przykład w mitochondriach przestrzeń międzybłonowa jest bardziej zakwaszona niż macierz, co może mieć znaczenie dla przebiegu niektórych reakcji enzymatycznych. Z kolei w chloroplastach zakwaszenie światła tylakoidów ma znaczenie nie tylko dla działania syntazy ATP, ale także dla regulacji aktywności enzymów cyklu Calvina poprzez zmiany pH w stromie.
W komórkach zwierzęcych gradient protonowy na błonach lizosomów, endosomów i innych pęcherzyków wewnątrzkomórkowych decyduje o ich środowisku chemicznym. Pompy protonowe typu V-ATP-aza zakwaszają wnętrze lizosomów, co jest niezbędne dla działania enzymów hydrolitycznych uczestniczących w trawieniu wewnątrzkomórkowym. Również w nerkach i żołądku specjalistyczne pompy protonowe biorą udział w regulacji pH płynów ustrojowych i soku żołądkowego, co ma kluczowe znaczenie dla homeostazy organizmu.
Gradient protonowy stanowi także narzędzie regulacyjne. Zmiany w jego wielkości mogą sygnalizować stan energetyczny komórki. Gdy zapotrzebowanie na ATP jest wysokie, przepływ protonów przez syntazę ATP przyspiesza, a gradient częściowo się zmniejsza. W odpowiedzi łańcuch transportu elektronów intensyfikuje pompowanie protonów, kompensując zużycie. W ten sposób system tworzy dynamiczną równowagę między tworzeniem i wykorzystaniem gradientu.
Warto podkreślić, że w niektórych sytuacjach gradient protonowy może być celowo „rozprzęgany”. Białka rozprzęgające umożliwiają przepływ protonów przez błonę z pominięciem syntazy ATP, przez co energia gradientu zostaje częściowo zamieniona na ciepło. Zjawisko to jest wykorzystywane m.in. w brunatnej tkance tłuszczowej ssaków, gdzie szybkie rozpraszanie gradientu protonowego zapewnia produkcję ciepła i utrzymanie temperatury ciała.
Wreszcie, zaburzenia w tworzeniu lub utrzymaniu gradientu protonowego mają poważne konsekwencje dla zdrowia. Defekty białek łańcucha oddechowego, mutacje w genach kodujących elementy syntazy ATP lub pomp protonowych prowadzą do chorób mitochondrialnych, zaburzeń metabolizmu, a nawet do śmierci komórki. Z tego powodu mechanizmy związane z gradientem protonowym są przedmiotem intensywnych badań w kontekście starzenia, chorób neurodegeneracyjnych, nowotworów oraz farmakologii.
Znaczenie gradientu protonowego w ewolucji i badaniach naukowych
Gradient protonowy uważany jest za jedno z najbardziej uniwersalnych rozwiązań ewolucyjnych w dziedzinie bioenergetyki. W wielu hipotezach dotyczących powstania życia zakłada się, że pierwotne formy organizmów wykorzystywały naturalne gradienty protonów występujące w środowisku, na przykład w pobliżu kominów hydrotermalnych na dnie oceanów. Z czasem mechanizmy te zostały ujęte w struktury błonowe i przekształcone w wewnętrzne systemy generowania i wykorzystywania gradientu.
Współczesne organizmy, od bakterii po człowieka, korzystają z bardzo podobnych zasad działania łańcuchów oddechowych i syntaz ATP, co wskazuje na głęboką konserwację tego rozwiązania w toku ewolucji. Różnice dotyczą głównie szczegółów budowy kompleksów białkowych, zestawu przenośników elektronów czy rodzaju końcowych akceptorów. Ogólny schemat – pompowanie protonów, tworzenie gradientu, sprzężenie z syntezą ATP – pozostaje jednak zadziwiająco podobny.
Badania nad gradientem protonowym i zjawiskami z nim powiązanymi doprowadziły do znaczących odkryć, za które przyznano kilka Nagród Nobla. Dotyczy to zarówno zrozumienia mechanizmów fosforylacji oksydacyjnej, jak i struktury syntazy ATP oraz funkcjonowania fotosystemów. Analiza gradientów protonowych wymagała rozwoju nowych technik pomiarowych, w tym zastosowania barwników fluorescencyjnych, sond pH, elektrod wrażliwych na jony oraz nowoczesnych metod obrazowania.
W dziedzinie medycyny i farmakologii gradient protonowy jest obiektem zainteresowania jako potencjalny cel terapeutyczny. Niektóre leki i toksyny działają poprzez zaburzenie tworzenia gradientu, blokowanie kompleksów łańcucha oddechowego lub bezpośrednie rozprzęganie fosforylacji oksydacyjnej. Wiąże się to zarówno z działaniem niepożądanym, jak i możliwością celowanego wpływania na metabolizm komórek, na przykład nowotworowych.
W biotechnologii gradient protonowy jest wykorzystywany w projektowaniu sztucznych systemów bioenergetycznych i biosensorów. Dzięki rekombinacji genetycznej i inżynierii białek naukowcy próbują tworzyć zmodyfikowane łańcuchy transportu elektronów oraz syntazy ATP o pożądanych właściwościach. Celem może być produkcja energii, związków chemicznych, a nawet napędzanie nanorobotów. Zrozumienie i kontrola gradientów protonowych są również istotne w konstrukcji sztucznych komórek i modeli minimalnych systemów życiowych.
W kontekście ekologii i nauk o środowisku gradient protonowy odgrywa rolę w cyklach biogeochemicznych. Mikroorganizmy żyjące w ekstremalnych warunkach, takich jak gorące źródła, słone jeziora czy głębiny oceaniczne, wykorzystują zróżnicowane łańcuchy oddechowe, ale zawsze opierają się na mechanizmie pomp protonowych. W ten sposób uczestniczą w obiegu pierwiastków, m.in. siarki, azotu i węgla, co wpływa na funkcjonowanie całych ekosystemów.
W perspektywie teoretycznej gradient protonowy jest inspiracją dla badań interdyscyplinarnych, łączących biologię, fizykę i chemię. Opis jego powstawania i działania wymaga odwołania się do pojęć takich jak potencjał elektrochemiczny, termodynamika nierównowagowa, transport jonowy czy mechanika statystyczna. Analiza tych zjawisk pozwala lepiej zrozumieć, jak żywe układy utrzymują porządek i organizację w środowisku dążącym do wyrównania różnic i wzrostu entropii.
Znaczenie gradientu protonowego w badaniach naukowych nie ogranicza się wyłącznie do poziomu komórkowego. Coraz częściej analizuje się także jego rolę w funkcjonowaniu tkanek, narządów i całych organizmów. Przykładowo, w mięśniach szkieletowych i sercowym efektywność tworzenia i wykorzystania gradientu protonowego wpływa na wydolność fizyczną. W tkance nerwowej zaburzenia mitochondrialne i związane z nimi zmiany gradientu mogą przyczyniać się do procesów neurodegeneracyjnych.
Wraz z rozwojem metod badawczych, takich jak mikroskopia superrozdzielcza, spektroskopia czy modelowanie komputerowe, możliwe staje się coraz dokładniejsze śledzenie dynamicznych zmian gradientu protonowego w czasie rzeczywistym oraz na poziomie pojedynczych organelli. Pozwala to na budowanie bardziej szczegółowych modeli funkcjonowania komórek i ich reakcji na stres, bodźce środowiskowe czy działanie leków.
Gradient protonowy, mimo że opiera się na prostym zjawisku różnicy stężeń jonów po dwóch stronach błony, okazuje się jednym z najbardziej eleganckich i uniwersalnych mechanizmów wykorzystywania energii w świecie żywym. Łączy w sobie aspekty chemiczne, fizyczne, biologiczne i ewolucyjne, a jego badanie wciąż dostarcza nowych pytań i inspiracji dla nauk przyrodniczych.
FAQ – najczęściej zadawane pytania o gradient protonowy
Czym jest gradient protonowy w prostych słowach?
Gradient protonowy to różnica stężenia jonów wodorowych (protonów) po dwóch stronach błony komórkowej lub błony organellum, takiego jak mitochondrium. Powstaje, gdy specjalne białka przepompowują protony na jedną stronę błony, zużywając energię. W efekcie po jednej stronie jest ich więcej, a po drugiej mniej, co tworzy rodzaj „magazynu” energii, który komórka może później wykorzystać do różnych procesów.
Jak powstaje gradient protonowy w mitochondriach?
W mitochondriach gradient protonowy powstaje podczas oddychania komórkowego. Elektrony pochodzące z utleniania składników odżywczych przepływają przez łańcuch transportu elektronów w wewnętrznej błonie mitochondrialnej. Energia z tego przepływu napędza pompy białkowe, które transportują protony z macierzy do przestrzeni międzybłonowej. Tworzy to różnicę stężenia i ładunku elektrycznego, stanowiącą źródło energii dla syntezy ATP.
Do czego komórka wykorzystuje gradient protonowy?
Komórka używa gradientu protonowego przede wszystkim do syntezy ATP za pomocą enzymu syntazy ATP. Protony przepływają przez ten enzym zgodnie z gradientem, co napędza reakcję łączenia ADP i fosforanu w ATP. Dodatkowo gradient protonowy dostarcza energii do aktywnego transportu innych substancji przez błony, reguluje pH różnych przedziałów komórkowych i może być wykorzystywany do produkcji ciepła, na przykład w brunatnej tkance tłuszczowej ssaków.
Czym jest siła protonomotoryczna?
Siła protonomotoryczna to miara energii zakumulowanej w gradiencie protonowym. Uwzględnia ona zarówno różnicę stężeń protonów, jak i różnicę potencjału elektrycznego po obu stronach błony. Im większa jest ta różnica, tym większy jest potencjał do wykonania pracy, na przykład do syntezy ATP lub napędzania transportu innych cząsteczek. Można ją porównać do napięcia w baterii, które określa, ile energii można z niej uzyskać.
Jakie są konsekwencje zaburzeń gradientu protonowego dla organizmu?
Zaburzenia gradientu protonowego prowadzą do poważnych problemów komórkowych, ponieważ utrudniają syntezę ATP i zakłócają transport przez błony. Mogą wynikać z mutacji w genach kodujących białka łańcucha oddechowego, syntazy ATP lub pomp protonowych, a także z działania toksyn czy niektórych leków. Konsekwencją są choroby mitochondrialne, obniżenie wydolności tkanek o dużym zapotrzebowaniu na energię, zaburzenia nerwowo-mięśniowe, a nawet śmierć komórek.