Mutacje stanowią jedno z kluczowych zjawisk leżących u podstaw zmienności genetycznej organizmów. Bez nich nie byłaby możliwa ani ewolucja, ani powstawanie nowych cech, ale towarzyszą im również liczne konsekwencje zdrowotne. Wśród różnych typów zmian w DNA szczególne miejsce zajmują mutacje strukturalne chromosomów, do których należy mutacja inwersji. Zrozumienie, czym jest inwersja, jak powstaje, oraz w jaki sposób wpływa na funkcjonowanie organizmu, pozwala lepiej pojąć mechanizmy dziedziczenia, powstawania chorób genetycznych i adaptacji populacji do środowiska.
Podstawy organizacji materiału genetycznego
Każda komórka organizmu (z wyjątkiem komórek rozrodczych i kilku wyspecjalizowanych typów komórek) zawiera kompletny zestaw informacji genetycznej zapisany w postaci DNA. Cztery rodzaje nukleotydów – adenina, tymina, cytozyna i guanina – tworzą sekwencje, które są instrukcjami budowy białek oraz regulacji procesów życiowych. U eukariontów DNA nie jest luźno rozproszony w jądrze, lecz upakowany w struktury zwane chromosomami. Pojedynczy chromosom obejmuje długą cząsteczkę DNA związaną z białkami histonowymi i niehistonowymi, tworząc złożony kompleks nazywany chromatyną.
Chromosomy mają charakterystyczną budowę: można wyróżnić ich krótsze i dłuższe ramię, połączone w rejonie centromeru. Na tych ramionach ułożone są geny – odcinki DNA kodujące białka lub różne rodzaje RNA. Pomiędzy genami znajdują się sekwencje niekodujące, które mogą pełnić funkcje regulacyjne, strukturalne lub być pozostałością dawnych zdarzeń ewolucyjnych. Stabilność sekwencji DNA jest kluczowa dla prawidłowego funkcjonowania organizmu, jednak na skutek błędów replikacji, działania czynników mutagennych lub zaburzeń rekombinacji może dochodzić do różnego rodzaju zmian, zarówno punktowych, jak i obejmujących większe fragmenty chromosomów.
Mutacje chromosomowe strukturalne obejmują takie procesy jak delecje (utrata fragmentu), duplikacje (podwojenie fragmentu), translokacje (przeniesienie fragmentu pomiędzy chromosomami) oraz inwersje, czyli odwrócenie fragmentu o 180 stopni. Choć wszystkie te zjawiska wpływają na organizację genomu, inwersje zajmują szczególne miejsce, gdyż niekoniecznie zmieniają ilość materiału genetycznego, ale w sposób zasadniczy modyfikują układ genów oraz wzory ich dziedziczenia.
Czym jest mutacja inwersji
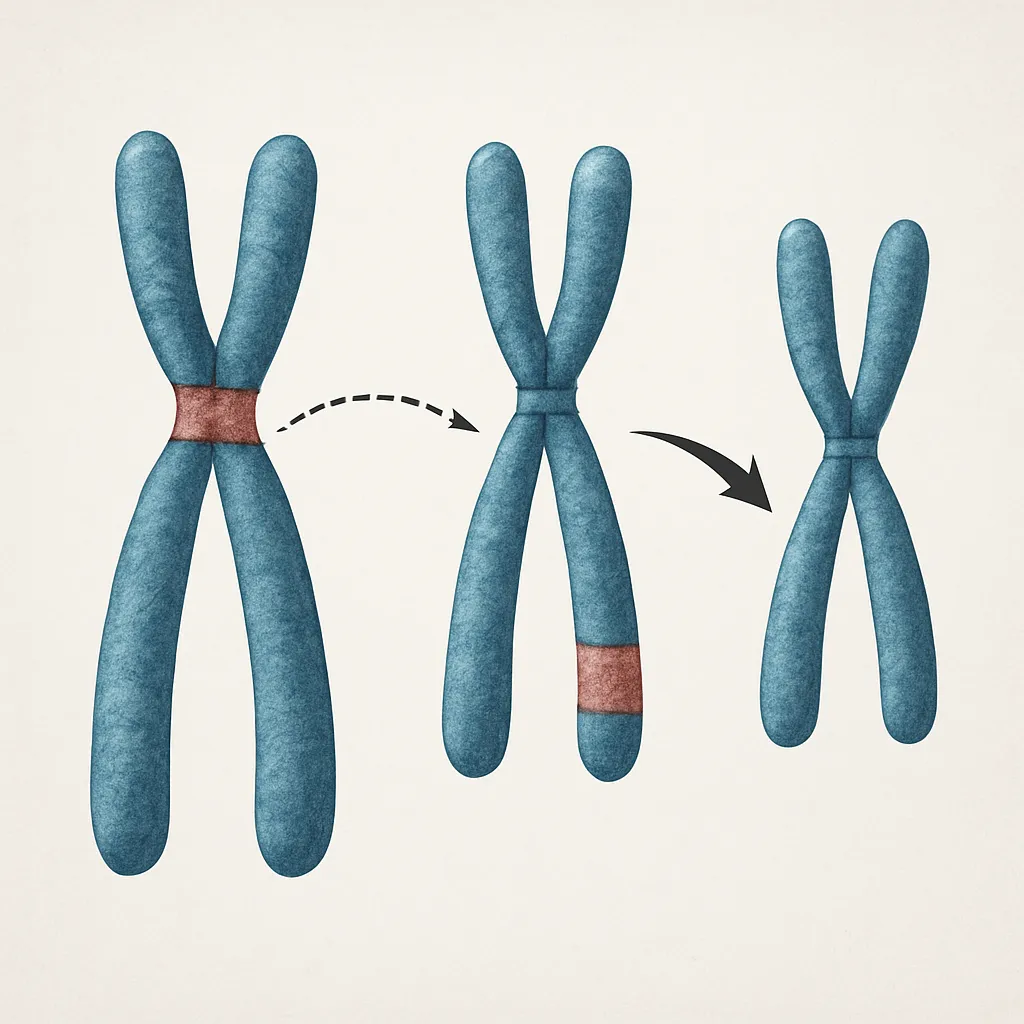
Mutacja inwersji to zmiana struktury chromosomu polegająca na odwróceniu o 180 stopni odcinka DNA w obrębie tego samego chromosomu. Oznacza to, że fragment chromosomu ulega przerwaniu w dwóch punktach, następnie odcinek pomiędzy tymi punktami zostaje obrócony, po czym dochodzi do ponownego połączenia końców z resztą chromosomu. Taka zmiana nie musi wiązać się z utratą lub zyskiem materiału genetycznego – ilość DNA pozostaje zazwyczaj taka sama, jednak jego wewnętrzna organizacja, orientacja sekwencji oraz wzajemne położenie genów ulegają przekształceniu.
W kontekście genetyki cytologicznej wyróżnia się dwa główne typy inwersji: paracentryczną i perycentryczną. Inwersja paracentryczna obejmuje fragment jednego ramienia chromosomu i nie zawiera centromeru. W tym przypadku oba punkty pęknięcia znajdują się po jednej stronie centromeru, a obrócony odcinek dotyczy jednego ramienia. Inwersja perycentryczna natomiast obejmuje centromer – oznacza to, że pęknięcia zachodzą na obu ramionach chromosomu, a odwrócony fragment zawiera centromer. Ten podział ma istotne znaczenie dla przebiegu mejozy, rekombinacji oraz skutków fenotypowych.
Od strony molekularnej inwersje mogą obejmować różne długości DNA: od krótkich odcinków kilku tysięcy par zasad, wykrywalnych jedynie metodami sekwencjonowania, aż po duże regiony cytogenetyczne widoczne w postaci zmian w prążkowaniu chromosomów w mikroskopie świetlnym. Ich powstawanie wiąże się najczęściej z obecnością powtarzalnych sekwencji w genomie, sprzyjających nieprawidłowemu parowaniu i rekombinacji homologiczej.
Rodzaje i mechanizmy powstawania inwersji
Na poziomie biologii komórki inwersje pojawiają się najczęściej jako efekt błędów w naprawie uszkodzeń DNA, zwłaszcza pęknięć dwuniciowych. Komórka dysponuje złożonymi mechanizmami naprawczymi, m.in. rekombinacją homologiczna oraz łączeniem końców niehomologicznych. W normalnych warunkach procesy te przywracają pierwotną strukturę DNA, ale w obecności licznych sekwencji powtórzonych lub w sytuacji intensywnego stresu genotoksycznego mogą powstawać połączenia w niewłaściwej orientacji, prowadząc do inwersji.
Inwersje paracentryczne powstają, gdy dwa pęknięcia wystąpią w obrębie jednego ramienia chromosomu. Końce DNA znajdujące się po przeciwnych stronach odcinka ulegają następnie połączeniu w odwrotnej orientacji. W trakcie mejozy chromosom z inwersją musi dopasować się do swojego prawidłowego homologa, co powoduje powstanie charakterystycznej pętli inwersyjnej podczas parowania chromosomów homologicznych w profazie I. Jeżeli dojdzie w tej pętli do crossing-over, może to skutkować powstawaniem chromosomów dicentrycznych (z dwoma centromerami) i acentrycznych (bez centromeru), które są zwykle niestabilne i nieprawidłowo rozdzielane do komórek potomnych.
Inwersje perycentryczne obejmującej centromer mają odmienną dynamikę. Pęknięcia zachodzą na obu ramionach chromosomu, a centromer zostaje obrany w skład odwróconego fragmentu. W wyniku crossing-over w obrębie pętli inwersyjnej przy inwersjach perycentrycznych powstają gamety zawierające chromosomy z delecjami i duplikacjami różnych fragmentów. Takie gamety niosą niesymetryczny materiał genetyczny i najczęściej prowadzą do obumarcia zarodków lub poważnych wad rozwojowych.
Na poziomie molekularnym mechanizmy prowadzące do inwersji obejmują między innymi nierówny crossing-over pomiędzy sekwencjami silnie podobnymi, mogącymi sparować się w nietypowej konfiguracji. W genomie obecne są liczne rozproszone powtórzenia, transpozony i elementy ruchome, które sprzyjają takim nieprawidłowym zdarzeniom rekombinacyjnym. Dodatkowo stres oksydacyjny, promieniowanie jonizujące oraz niektóre substancje chemiczne zwiększają częstość pęknięć DNA, co wtórnie może zwiększać ryzyko powstawania inwersji. W komórkach płciowych skutki takich zdarzeń są szczególnie istotne, gdyż inwersje mogą zostać przekazane potomstwu.
Konsekwencje inwersji dla organizmu
Mutacja inwersji ma charakter rearanżacji strukturalnej: zmienia się położenie i orientacja fragmentu chromosomu, ale zazwyczaj nie dochodzi do istotnej zmiany całkowitej ilości DNA. Z tego powodu w wielu przypadkach inwersje mogą być fenotypowo niemal obojętne dla nosiciela, o ile nie naruszają struktury ważnych genów ani ich regionów regulatorowych oraz nie zaburzają prawidłowego przebiegu mejozy. Jednak często konsekwencje są bardziej złożone i obejmują zarówno skutki na poziomie ekspresji genów, jak i płodności czy ryzyka urodzenia potomstwa z aberracjami chromosomowymi.
Kiedy miejsce pęknięcia znajduje się w obrębie genu, może dojść do jego przerwania. Powstaje wówczas niekompletne białko lub produkt całkowicie nieaktywowany, co może skutkować chorobą genetyczną. Jeśli pęknięcie i ponowne połączenie wystąpią w pobliżu regionów regulatorowych, np. promotorów czy enhancerów, orientacja tych elementów może ulec zaburzeniu lub mogą one znaleźć się w nowym kontekście chromosomowym. W efekcie ekspresja genu może zostać wyciszona, nadmiernie pobudzona lub niewłaściwie regulowana w czasie i przestrzeni. Nawet, gdy sekwencja genu pozostaje nienaruszona, zmiana jego sąsiedztwa chromosomowego może prowadzić do tzw. efektu pozycji, czyli odmiennego wzoru aktywności transkrypcyjnej.
Istotnym skutkiem inwersji jest wpływ na proces powstawania gamet. Nosiciel heterozygotyczny, mający jeden chromosom z inwersją i jeden prawidłowy, jest narażony na powstawanie gamet o nieprawidłowej zawartości genetycznej w wyniku crossing-over w obrębie pętli inwersyjnej. W przypadku inwersji paracentrycznych rekombinowane chromatydy mogą tworzyć struktury dicentryczne i acentryczne, co zwykle prowadzi do ich utraty. W efekcie wielu zarodków dochodzi do wczesnych poronień, a urodzone potomstwo częściej jest zdrowe, choć deficyt płodności może być zauważalny. Przy inwersjach perycentrycznych częściej dochodzi do powstania zrównoważonych i niezrównoważonych gamet, z których niektóre mogą dawać potomstwo z delecjami lub duplikacjami fragmentów chromosomów, co manifestuje się różnym stopniem upośledzeń rozwojowych.
Konsekwencje kliniczne inwersji zależą zatem od wielkości odwróconego fragmentu, lokalizacji punktów pęknięcia, obecności istotnych genów w jego obrębie, a także od tego, czy nosiciel jest homozygotą (obie kopie chromosomu zawierają tę samą inwersję) czy heterozygotą (inwersja obecna tylko w jednej kopii). Homozygotyczne inwersje są często znacznie mniej szkodliwe dla płodności, gdyż nie dochodzi wówczas do tworzenia pętli inwersyjnych w czasie mejozy, a chromosomy homologiczne dobrze się parują. Jednak sama obecność inwersji może wpływać na ekspresję genów i organizację chromatyny, co bywa trudne do przewidzenia i oceny bez szczegółowych badań molekularnych.
Inwersje w populacjach i ewolucji
Mutacje inwersji, choć często postrzegane wyłącznie jako potencjalne źródło zaburzeń, pełnią ważną funkcję w ewolucji. Inwersje mogą ograniczać rekombinację w obrębie odwróconego fragmentu u osobników heterozygotycznych. Zmniejszona wymiana fragmentów chromatyd oznacza, że zestaw alleli w tym regionie pozostaje bardziej trwały w kolejnych pokoleniach. Jeżeli dana kombinacja alleli okaże się korzystna w określonych warunkach środowiskowych, inwersja może sprzyjać zachowaniu tej korzystnej konfiguracji, działając jak blok ewolucyjny, który utrudnia „rozprucie” adaptacyjnego układu genów przez rekombinację.
W populacjach dzikich zwierząt i roślin opisano liczne przykłady inwersji związanych z adaptacją klimatyczną, sezonowością rozrodu czy odpornością na patogeny. W pewnych regionach geograficznych częstotliwość określonych inwersji jest wyższa, co koreluje np. z temperaturą, wilgotnością lub obecnością specyficznych czynników stresowych. U muszki owocowej zaobserwowano gradienty częstości inwersji wzdłuż osi geograficznych, co interpretuje się jako wynik długotrwałej selekcji naturalnej faworyzującej odmienne układy genów w różnych klimatach. Dzięki inwersjom możliwe jest łączenie w „pakiety” alleli wspólnie zapewniających przewagę selekcyjną, co ułatwia utrzymywanie złożonych cech adaptacyjnych.
Inwersje odgrywają również rolę w procesie specjacji, czyli powstawania nowych gatunków. Ograniczenie rekombinacji w obrębie dużych regionów chromosomalnych może sprzyjać nagromadzaniu się różnic genetycznych pomiędzy populacjami, które rzadko wymieniają materiał genetyczny. W takim przypadku inwersje mogą przyczyniać się do powstawania barier reprodukcyjnych: potomstwo hybrydowe pomiędzy osobnikami z różnymi układami chromosomów może być mniej płodne lub mniej żywotne. W efekcie przepływ genów pomiędzy populacjami ulega ograniczeniu, co sprzyja ich genetycznemu i fenotypowemu rozdzieleniu.
W genomach wielu gatunków, w tym człowieka, wykryto tzw. polimorfizmy inwersyjne – warianty strukturalne obecne z istotną częstością w populacji, które nie zawsze wiążą się z chorobą. Zidentyfikowano regiony, w których część osób posiada chromosom w orientacji odwróconej, a część w orientacji „referencyjnej”. Tego typu polimorfizmy mogą być neutralne lub modulować ryzyko wystąpienia określonych schorzeń, wpływać na cechy ilościowe, jak wzrost, masa ciała czy metabolizm, a także oddziaływać na odpowiedź na czynniki środowiskowe. Analiza tych struktur jest jednym z dynamicznie rozwijających się obszarów genomiki populacyjnej i medycyny personalizowanej.
Metody wykrywania inwersji chromosomowych
Identyfikacja mutacji inwersji wymaga zastosowania metod cytogenetycznych i molekularnych o różnej rozdzielczości. Klasyczna cytogenetyka opiera się na analizie preparatów chromosomowych w metafazie, barwionych tak, aby uzyskać charakterystyczne prążkowanie. Zmiana układu prążków na jednym z chromosomów może sugerować obecność inwersji, zwłaszcza w przypadku dużych rearanżacji. Metoda ta pozwala na wykrywanie zmian obejmujących miliony par zasad, ale jest niewystarczająco czuła dla małych inwersji. Ponadto interpretacja prążkowania wymaga znacznego doświadczenia i porównania z mapami referencyjnymi.
Nowocześniejsze techniki molekularne, takie jak hybrydyzacja fluorescencyjna in situ (FISH), umożliwiają dokładniejsze mapowanie fragmentów chromosomów. Dzięki zastosowaniu sond znakowanych fluorescencyjnie możliwe jest wykazanie, że określony odcinek DNA zmienił położenie lub orientację. W przypadku inwersji sondy umieszczone po obu stronach spodziewanego miejsca pęknięcia pozwalają ocenić, czy kolejność sygnałów na chromosomie jest zgodna z oczekiwaną, czy też odwrócona. Jednak także FISH ma ograniczoną rozdzielczość i jest stosunkowo pracochłonna, dlatego chętnie łączy się ją z innymi metodami.
Rozwój technologii sekwencjonowania DNA przyniósł rewolucję w wykrywaniu zmian strukturalnych. Sekwencjonowanie całogenomowe umożliwia identyfikację przerwań ciągłości sekwencji, odwróconych odcinków oraz punktów łączenia charakterystycznych dla inwersji. Analiza par odczytów sekwencyjnych, które mapują się w nietypowej orientacji lub z nieoczekiwanym odstępem, pozwala wnioskować o obecności rearanżacji. Dodatkowe potwierdzenie uzyskuje się przez analizę głębokości pokrycia, lokalne składanie sekwencji czy zastosowanie technologii długich odczytów, które ułatwiają odwzorowanie złożonych regionów powtórzeniowych.
W praktyce klinicznej diagnostyka inwersji chromosomowych często łączy kilka podejść: klasyczne badanie kariotypu, FISH ukierunkowaną na wybrane regiony oraz techniki sekwencjonowania. W zależności od wskazań – podejrzenia choroby genetycznej, niepłodności, nawracających poronień czy planowania potomstwa – dobiera się odpowiednie testy o wymaganej rozdzielczości. Coraz częściej stosuje się też metody bioinformatyczne integrujące dane z różnych platform, co pozwala na kompleksową ocenę struktury genomu pacjenta.
Znaczenie inwersji dla medycyny człowieka
W medycynie inwersje chromosomowe stanowią istotny przedmiot zainteresowania zarówno w kontekście chorób dziedzicznych, jak i onkologii. U części pacjentów z niepłodnością, poronieniami nawracającymi lub urodzeniem dzieci z wadami wrodzonymi wykrywa się zrównoważone inwersje chromosomowe. Zrównoważone oznacza w tym przypadku brak widocznej utraty czy zysku dużych fragmentów DNA, a jedynie ich przestawienie. Nosiciele takich układów są często fenotypowo zdrowi, ale obarczeni zwiększonym ryzykiem powstawania gamet niezrównoważonych, zawierających delecje lub duplikacje regionów objętych pętlą inwersyjną.
Poradnictwo genetyczne dla nosicieli inwersji obejmuje szczegółową analizę typu i lokalizacji zmiany, ocenę dostępnych danych literaturowych oraz, gdy to możliwe, zbadanie innych członków rodziny. Na tej podstawie szacuje się prawdopodobieństwo urodzenia dziecka z nieprawidłowym kariotypem lub ciężkimi wadami rozwojowymi. W zależności od sytuacji klinicznej możliwe jest skorzystanie z diagnostyki prenatalnej, badań preimplantacyjnych w ramach procedury zapłodnienia pozaustrojowego lub innych form monitorowania. Decyzje w tym obszarze zawsze wymagają indywidualnego podejścia i wsparcia psychologicznego.
Inwersje biorą również udział w powstawaniu niektórych nowotworów. Przemiana nowotworowa często wiąże się z niestabilnością genomu i licznymi rearanżacjami chromosomowymi. Odwrócenie fragmentu może prowadzić do powstania genów fuzyjnych, w których początkowy fragment jednego genu łączy się z fragmentem innego, tworząc nowy produkt białkowy o zmienionej funkcji. Takie białka fuzyjne mogą działać jako onkogeny, pobudzając niekontrolowane podziały komórkowe lub zaburzając mechanizmy regulacji cyklu komórkowego i apoptozy. Identyfikacja charakterystycznych inwersji jest w wielu przypadkach elementem diagnostyki nowotworów, umożliwia klasyfikację typu choroby oraz dobór terapii celowanych.
Przykłady klinicznie istotnych inwersji obejmują zarówno zmiany specyficzne dla linii komórkowej nowotworu, jak i germinalne inwersje dziedziczone w rodzinach obciążonych predyspozycją do określonych schorzeń. Postęp technik genomowych ujawnia coraz więcej subtelnych inwersji, których znaczenie funkcjonalne dopiero jest poznawane. Włączenie informacji o nich do modeli ryzyka chorób wieloczynnikowych, takich jak cukrzyca, choroby serca czy zaburzenia neurologiczne, stanowi jedno z wyzwań nowoczesnej medycyny genomowej.
FAQ – najczęstsze pytania o mutację inwersji
Czy mutacja inwersji zawsze jest szkodliwa dla organizmu?
Inwersja nie musi być jednoznacznie szkodliwa. W wielu przypadkach nosiciele zrównoważonych inwersji nie wykazują żadnych objawów klinicznych i prowadzą normalne życie. Problem pojawia się, gdy punkty pęknięcia naruszają ważne geny lub ich sekwencje regulatorowe albo gdy inwersja zaburza proces mejozy, powodując powstawanie gamet niezrównoważonych. Wtedy może dojść do poronień, niepłodności lub urodzenia dziecka z wadami rozwojowymi. Część inwersji może być też neutralna lub nawet sprzyjać adaptacji populacji do środowiska.
Jak można wykryć inwersję chromosomową u człowieka?
Wykrywanie inwersji opiera się na połączeniu metod cytogenetycznych i molekularnych. Duże inwersje są widoczne w klasycznym badaniu kariotypu z wykorzystaniem prążkowania chromosomów. Mniejsze rearanżacje wymagają zastosowania bardziej czułych technik, takich jak hybrydyzacja fluorescencyjna in situ (FISH) z odpowiednimi sondami czy sekwencjonowanie całogenomowe. Analiza bioinformatyczna danych sekwencyjnych pozwala zlokalizować punkty pęknięcia i odwrócenia. Dobór testu zależy od wskazań klinicznych, rodzaju podejrzewanej zmiany oraz dostępności technologii.
Czy osoba z inwersją chromosomową może mieć zdrowe dzieci?
Osoba nosząca inwersję chromosomową ma zwykle zwiększone ryzyko powstania gamet o nieprawidłowym składzie genetycznym, zwłaszcza gdy jest heterozygotą. Nie oznacza to jednak, że każde dziecko będzie chore. Część gamet zachowuje prawidłowy lub zrównoważony układ chromosomów, co pozwala na rozwój zdrowego potomstwa. Ryzyko zależy od typu inwersji, jej wielkości, lokalizacji punktów pęknięcia oraz danych rodzinnych. W takich sytuacjach zaleca się konsultację z genetykiem klinicznym i rozważenie diagnostyki prenatalnej lub preimplantacyjnej.
Czym inwersja różni się od delecji i translokacji chromosomowej?
Inwersja jest rearanżacją wewnątrz jednego chromosomu i polega na odwróceniu fragmentu o 180 stopni, bez koniecznej utraty lub zysku materiału genetycznego. Delecja natomiast oznacza utratę odcinka chromosomu, co prowadzi do bezpowrotnego braku obecnych tam genów. Translokacja obejmuje przeniesienie fragmentu pomiędzy różnymi chromosomami lub innym miejscem na tym samym chromosomie. W translokacjach zrównoważonych ilość DNA może pozostać zachowana, ale zmienia się jego położenie. Każdy z tych typów zmian ma odmienny wpływ na dziedziczenie i ryzyko chorób.
Czy inwersje odgrywają rolę w ewolucji i adaptacji gatunków?
Inwersje są ważnym czynnikiem ewolucyjnym. U heterozygot ograniczają rekombinację w obrębie odwróconego regionu, co sprzyja zachowaniu stałych układów alleli. Jeśli taki zestaw genów zwiększa przystosowanie do określonych warunków środowiska, inwersja może być faworyzowana przez selekcję naturalną. W wielu gatunkach obserwuje się gradienty częstości poszczególnych inwersji związane np. z klimatem. Długotrwale utrzymujące się różnice w układzie inwersji pomiędzy populacjami mogą przyczyniać się do powstawania barier rozrodczych i w konsekwencji do wyodrębniania się nowych gatunków.