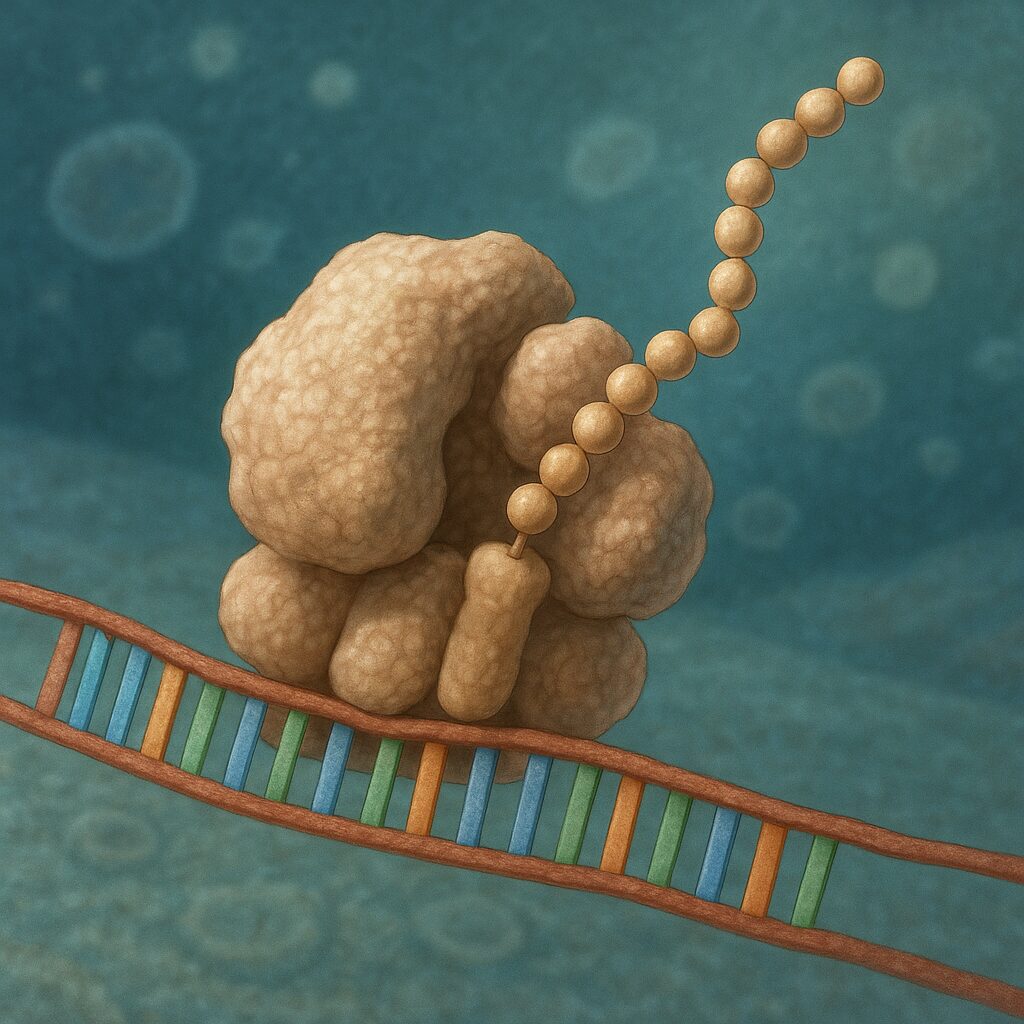
Rybosom jest jednym z najbardziej niezwykłych tworów materii ożywionej: złożonym kompleksem cząsteczek, który potrafi odczytać informację genetyczną i zamienić ją w konkretne białka. Bez rybosomów nie mogłyby powstać enzymy, hormony, elementy cytoszkieletu ani receptory błonowe, a więc żaden z procesów życiowych nie mógłby przebiegać prawidłowo. Zrozumienie budowy i działania rybosomu stało się fundamentem współczesnej biologii molekularnej, genetyki oraz medycyny, pozwalając lepiej pojąć naturę chorób, mechanizm działania leków i ewolucyjne pokrewieństwo organizmów.
Budowa rybosomu i jego zróżnicowanie w świecie organizmów
Rybosom jest dużym, wieloskładnikowym kompleksem zbudowanym z rybosomalnego RNA (rRNA) oraz specyficznych białek rybosomalnych. Choć w uproszczeniu przedstawia się go jako drobny punkt w cytoplazmie, w rzeczywistości jest to złożona maszyna molekularna o precyzyjnej architekturze. Podstawowy podział strukturalny obejmuje dwie podjednostki: małą i dużą. Obie razem tworzą funkcjonalny rybosom zdolny do prowadzenia translacji, czyli syntezy białka na matrycy mRNA.
W komórkach prokariotycznych, takich jak bakterie i archeony, występują rybosomy typu 70S. S to jednostka współczynnika sedymentacji w polu siły odśrodkowej, która nie sumuje się liniowo, dlatego połączenie podjednostek 30S i 50S daje rybosom 70S. W komórkach eukariotycznych, czyli roślin, zwierząt, grzybów i protistów, dominują rybosomy 80S, zbudowane z podjednostek 40S i 60S. Różnice te są kluczowe dla farmakologii, ponieważ wiele antybiotyków celuje w cechy charakterystyczne rybosomów bakteryjnych, nie naruszając (lub w mniejszym stopniu naruszając) rybosomów gospodarza.
Mała podjednostka rybosomu odpowiada głównie za wiązanie mRNA i dopasowywanie kodonów do odpowiednich cząsteczek tRNA. Zawiera ona rRNA pełniący funkcję szkieletu strukturalnego oraz powierzchnię wiążącą, która rozpoznaje sekwencje inicjacyjne na mRNA. Duża podjednostka jest miejscem, gdzie zachodzą reakcje chemiczne tworzenia wiązań peptydowych. Znajdują się w niej kluczowe fragmenty rRNA, które działają jak katalizator, czyli pełnią funkcję rybozymu. Oznacza to, że podstawową aktywność enzymatyczną rybosomu zapewnia nie białko, lecz RNA.
Wewnątrz dużej podjednostki wyróżnia się trzy główne miejsca wiązania tRNA: A (aminoacylo), P (peptydylowe) i E (wyjścia). W miejscu A przyłącza się nowa cząsteczka tRNA niosąca kolejny aminokwas. W miejscu P znajduje się tRNA z rosnącym łańcuchem polipeptydowym, a w miejscu E tRNA opuszcza rybosom po oddaniu swojego aminokwasu. Ta przestrzenna organizacja umożliwia sekwencyjne przesuwanie się tRNA i wydłużanie powstającego białka w sposób uporządkowany i wysoce skoordynowany.
W komórkach eukariotycznych rybosomy nie występują wyłącznie w cytoplazmie. Znajdujemy je przytwierdzone do błon retikulum endoplazmatycznego szorstkiego, co tworzy wyspecjalizowaną strefę produkcji białek przeznaczonych do wydzielania, wbudowania w błony lub do lizosomów. Rybosomy wolne w cytoplazmie syntetyzują przede wszystkim białka działające wewnątrz cytoplazmy, jąder komórkowych czy mitochondriów.
Interesującą cechą komórek eukariotycznych jest obecność własnych rybosomów w mitochondriach i chloroplastach. Mają one typ 70S, podobny do bakteryjnych, co wspiera teorię endosymbiozy, według której mitochondria i chloroplasty wywodzą się z dawnych symbiotycznych bakterii. Ta różnorodność rybosomów w obrębie jednej komórki wskazuje, jak głęboko w historię życia sięga ewolucja aparatu translacyjnego i jak złożona była droga prowadząca do współczesnych form komórkowych.
Poza klasycznym rozróżnieniem na 70S i 80S, istnieją też subtelne różnice składu białkowego i sekwencji rRNA pomiędzy gatunkami. Pozwala to używać rybosomalnego RNA jako markera filogenetycznego w badaniach pokrewieństwa ewolucyjnego. Analiza sekwencji 16S rRNA u prokariontów i 18S rRNA u eukariontów stanowi filar nowoczesnej systematyki oraz ekologii mikroorganizmów, umożliwiając identyfikację drobnoustrojów na podstawie ich materiału genetycznego z próbek środowiskowych.
Jak działa rybosom: od informacji genetycznej do białka
Podstawową funkcją rybosomu jest translacja, czyli przekładanie zapisu genetycznego na język białek. Informacja zawarta w DNA zostaje najpierw przepisana na mRNA w procesie transkrypcji, który zachodzi w jądrze komórkowym u eukariontów lub w cytoplazmie u prokariontów. Dopiero dojrzała cząsteczka mRNA staje się matrycą dla rybosomu. Proces translacji dzieli się na trzy główne etapy: inicjację, elongację i terminację, a każdy z nich wymaga udziału licznych czynników białkowych i energii w postaci GTP.
Inicjacja rozpoczyna się od rozpoznania sekwencji startowej na mRNA. W komórkach bakteryjnych jest to zwykle sekwencja Shine-Dalgarno, w eukariontowych natomiast kompleks rybosomalny przesuwa się wzdłuż mRNA, aż natrafi na pierwszy kodon AUG w odpowiednim kontekście. Do małej podjednostki dołącza inicjatorowy tRNA niosący aminokwas metioninę, który rozpoznaje kodon startowy. Po prawidłowym ustawieniu kompleksu dołącza duża podjednostka, tworząc w pełni funkcjonalny rybosom zdolny do wydłużania łańcucha polipeptydowego.
Podczas elongacji rybosom przesuwa się wzdłuż mRNA w kierunku od końca 5′ do 3′, odczytując kolejne kodony, czyli trójki nukleotydów. Każdy kodon determinuje, jaki aminokwas zostanie włączony do powstającego białka. Specyficzne cząsteczki tRNA, niosące odpowiednie aminokwasy, dopasowują swoje antykodony do kodonów mRNA w miejscu A rybosomu. Gdy poprawne sparowanie zostanie rozpoznane, w centrum katalitycznym dużej podjednostki zachodzi powstanie nowego wiązania peptydowego pomiędzy ostatnim aminokwasem łańcucha a nowo przyłączonym aminokwasem.
Rybosom pełni zatem rolę molekularnego korektora, który rozpoznaje właściwe dopasowanie par zasad i minimalizuje błędy translacji. Choć błędy mogą się zdarzać, ich częstość jest zadziwiająco niska, co ma kluczowe znaczenie dla stabilności funkcji komórkowych. Nadmiernie wysoki poziom pomyłek skutkowałby powstawaniem wadliwych białek o zaburzonych strukturach, co mogłoby być toksyczne lub prowadzić do zaburzeń metabolicznych.
W trakcie elongacji rybosom wykonuje ruchy określane mianem translokacji. Po utworzeniu wiązania peptydowego łańcuch polipeptydowy zostaje przeniesiony z tRNA w miejscu P na tRNA znajdujący się w miejscu A. Następnie całe białko rybosomalne przesuwa się o jeden kodon, tak że tRNA z rosnącym łańcuchem przechodzi do miejsca P, a tRNA pozbawiony aminokwasu trafia do miejsca E i opuszcza rybosom. Ten cykliczny proces jest napędzany hydrolizą GTP przez czynniki elongacyjne, co zapewnia kierunkowość oraz wysoką sprawność translacji.
Terminacja następuje, gdy rybosom napotka jeden z kodonów stop: UAA, UAG lub UGA. Nie istnieją tRNA komplementarne do tych kodonów; zamiast tego do miejsca A wiążą się specjalne czynniki terminacyjne. Powodują one hydrolityczne odcięcie łańcucha polipeptydowego od tRNA w miejscu P i uwolnienie świeżo zsyntetyzowanego białka. Po zakończeniu translacji podjednostki rybosomu rozdzielają się i mogą zostać wykorzystane ponownie w kolejnym cyklu syntezy białka.
W organizmach o wysokiej aktywności metabolicznej rybosomy często tworzą struktury zwane polisomami (polirybosomami). Jest to zespół wielu rybosomów jednocześnie translatujących tę samą cząsteczkę mRNA. W ten sposób komórka znacząco zwiększa wydajność produkcji konkretnego białka, co ma kluczowe znaczenie w warunkach intensywnego wzrostu, odpowiedzi immunologicznej czy rozwoju embrionalnego. Tworzenie polisomów pozwala na błyskawiczne dostosowanie poziomu białek do aktualnych potrzeb fizjologicznych.
Istotnym aspektem działania rybosomów jest ich współpraca z innymi elementami komórki. Podczas translacji białka przeznaczone do wydzielania lub wbudowania w błony są rozpoznawane przez sekwencje sygnałowe na nowo powstającym łańcuchu. Kompleks rozpoznający sygnał kieruje taki rybosom do błony retikulum endoplazmatycznego. Dzięki temu translacja i translokacja białka do światła retikulum zachodzą jednocześnie, co minimalizuje ryzyko jego nieprawidłowego fałdowania w cytoplazmie.
Warto podkreślić, że mimo olbrzymiej złożoności procesów zachodzących na rybosomie, całość odbywa się w skalach rozmiarów i czasów trudnych do wyobrażenia. Pojedynczy rybosom może syntetyzować łańcuchy polipeptydowe z prędkością kilkunastu do kilkudziesięciu aminokwasów na sekundę, zachowując jednocześnie wysoką dokładność. Ta wydajność sprawia, że rybosom jest jedną z najbardziej efektywnych maszyn biologicznych, jakie znamy.
Znaczenie rybosomów w medycynie, biotechnologii i ewolucji
Rybosomy odgrywają kluczową rolę nie tylko w podstawowych procesach życiowych, lecz również w medycynie i biotechnologii. Wielu klasycznych antybiotyków, takich jak tetracykliny, makrolidy czy aminoglikozydy, działa poprzez wiązanie się z rybosomami bakteryjnymi i blokowanie translacji. Leki te wykorzystują subtelne różnice strukturalne między rybosomami prokariontów i eukariontów, co pozwala na selektywne zahamowanie wzrostu bakterii przy ograniczonym wpływie na komórki gospodarza. Mechanizm ten pokazuje, jak znajomość budowy rybosomu może zostać wykorzystana do projektowania skutecznych terapii.
Jednocześnie narastająca antybiotykooporność stanowi poważne wyzwanie. Bakterie mogą modyfikować swoje rRNA lub białka rybosomalne, produkować enzymy inaktywujące antybiotyki albo pompować leki na zewnątrz komórki. Wszystkie te strategie utrudniają wiązanie antybiotyku do rybosomu lub zmniejszają jego skuteczność. Zrozumienie struktury rybosomu na poziomie atomowym, uzyskane między innymi dzięki krystalografii rentgenowskiej i mikroskopii krioelektronowej, umożliwia projektowanie nowych leków, które pokonują powstałe już mechanizmy oporności.
W biotechnologii rybosomy są podstawą technologii produkcji białek rekombinowanych. Wykorzystując bakterie, drożdże lub komórki ssacze jako systemy ekspresji, naukowcy wprowadzają do nich sztucznie skonstruowane geny kodujące pożądane białka: hormony, przeciwciała, enzymy przemysłowe czy składniki szczepionek. Rybosomy komórek gospodarza dokonują translacji tych obcych genów tak samo jak własnych, produkując duże ilości określonych białek. Dzięki temu możliwa stała się masowa produkcja insuliny ludzkiej, czynników krzepnięcia, enzymów trawiennych i wielu innych substancji o znaczeniu terapeutycznym.
Rozwijają się także systemy translacji in vitro, w których rybosomy są wykorzystywane poza żywą komórką. Specjalnie przygotowane ekstrakty komórkowe zawierające rybosomy, tRNA, aminokwasami i niezbędnymi czynnikami translacyjnymi pozwalają na syntezę białek bezpośrednio z dostarczonego mRNA w probówce. Techniki te umożliwiają szybkie testowanie wariantów białek, projektowanie nowych enzymów czy badanie działania leków na proces translacji bez konieczności hodowli komórek. Coraz bardziej zaawansowane są też próby sztucznego modyfikowania rybosomów tak, by włączały do białek niekanoniczne aminokwasy o nowych właściwościach chemicznych.
Rybosomy odgrywają również fundamentalną rolę w rozwoju terapii genowej i technologii mRNA. Szczepionki oparte na mRNA korzystają z faktu, że rybosomy komórek organizmu potrafią odczytać dostarczoną cząsteczkę informacyjną i wytworzyć odpowiednie białko antygenowe, pobudzające odpowiedź immunologiczną. Samo mRNA jest ulotne i po pewnym czasie degradowane, natomiast rybosomy działają jako uniwersalny aparat wykonawczy, zdolny przełożyć różnorodne sekwencje genetyczne na konkretne struktury białkowe.
W kontekście chorób genetycznych i zaburzeń komórkowych szczególne znaczenie mają tzw. rybosomopatie – schorzenia wynikające z mutacji w genach kodujących białka rybosomalne lub czynniki zaangażowane w biogenezę rybosomów. Przykładem jest anemia Blackfana-Diamonda, w której defekty w składaniu rybosomów prowadzą do upośledzonej produkcji erytrocytów. Inne choroby wiążą się z nieprawidłową funkcją mitochondriów, gdzie zaburzenia w działaniu rybosomów mitochondialnych skutkują deficytem energii i objawami wielonarządowymi. Badania nad tymi rzadkimi schorzeniami rzucają światło na to, jak precyzyjnie musi być regulowana produkcja białek, by komórka działała prawidłowo.
W onkologii coraz więcej dowodów wskazuje, że zmiany w biogenezie rybosomów i regulacji translacji mogą przyczyniać się do rozwoju nowotworów. Komórki rakowe często mają zwiększoną liczbę rybosomów i intensywniejszą syntezę białek, co wspiera ich szybkie dzielenie się i inwazyjny charakter. Niektóre onkogeny wpływają bezpośrednio na aktywność czynników inicjacji translacji, przesuwając równowagę w stronę nadprodukcji białek proproliferacyjnych. W związku z tym trwają prace nad lekami celującymi w elementy aparatu translacyjnego, które mogłyby selektywnie hamować wzrost komórek nowotworowych.
Rybosomy są również kluczem do zrozumienia ewolucji życia. Sekwencje rRNA, ze względu na swoją konserwatywność i jednoczesną obecność zmiennych regionów, stały się wiarygodnym narzędziem odtwarzania drzewa życia. Analizy porównawcze ujawniły zaskakujące pokrewieństwa między organizmami i doprowadziły do wyłonienia trzech domen życia: Bacteria, Archaea i Eukarya. Różnice w strukturze rRNA oraz składzie białkowym rybosomów odzwierciedlają miliardy lat ewolucji, a jednocześnie zachowanie podstawowego schematu działania rybosomu wskazuje, jak wcześnie musiał on powstać w historii życia.
Hipotezy dotyczące początków życia, takie jak koncepcja świata RNA, przypisują rybosomom szczególnie istotną rolę. Rybosom jest bowiem przykładem złożonej cząsteczki RNA o właściwościach katalitycznych – rybozymu – która współpracuje z białkami. Sugeruje to, że pierwotne systemy biologiczne mogły opierać się niemal wyłącznie na RNA, a białka dołączyły później, stopniowo przejmując wiele funkcji enzymatycznych. Rybosom, jako hybryda RNA i białka, może być reliktem tej dawnej epoki, łącząc w sobie ślady bardzo wczesnych etapów ewolucji molekularnej.
Tak rozumiana perspektywa ewolucyjna sprawia, że rybosom staje się nie tylko obiektem badań strukturalnych i funkcjonalnych, ale także swoistym archiwum historii życia. Każda cząsteczka rRNA w naszych komórkach niesie w sobie zapis ewolucyjnych modyfikacji, które zaszły od wspólnego przodka wszystkich organizmów. Analizując te sekwencje, naukowcy próbują odpowiedzieć na pytania o pochodzenie komórek eukariotycznych, stopień spokrewnienia różnych grup archeonów oraz o to, jak wyglądały pierwsze systemy translacyjne, zanim osiągnęły znaną dziś złożoność.
Znaczenie rybosomów wykracza także poza klasyczną biologię i medycynę, obejmując zagadnienia inżynierii biologicznej oraz syntezy życia. Projekty tworzenia minimalnych komórek, zdolnych do samopodtrzymującej się replikacji, zawsze uwzględniają aparat translacyjny jako jeden z absolutnie niezbędnych elementów. Bez zestawu rybosomów, tRNA i czynników translacyjnych nie jest możliwe odtwarzanie białkowych składników komórki, a zatem utrzymanie jej struktury i funkcji. Próby wprowadzenia do rybosomów zmodyfikowanych zasad azotowych czy rozszerzonego alfabetu aminokwasów stanowią krok w stronę projektowania organizmów o zupełnie nowych właściwościach chemicznych, wykraczających poza granice naturalnego życia.
FAQ – najczęściej zadawane pytania o rybosomy
Czym różni się rybosom prokariotyczny od eukariotycznego?
Rybosomy prokariotyczne (bakterii i archeonów) mają typ 70S i składają się z podjednostek 30S i 50S, natomiast eukariotyczne – typ 80S z podjednostek 40S i 60S. Różnią się one masą, składem rRNA i białek oraz szczegółami struktury trójwymiarowej. Te różnice umożliwiają działanie wielu antybiotyków, które selektywnie blokują rybosomy bakteryjne, z minimalnym wpływem na komórki zwierzęce czy roślinne, co ma kluczowe znaczenie terapeutyczne.
Gdzie w komórce znajdują się rybosomy?
Rybosomy występują zarówno wolno w cytoplazmie, jak i przytwierdzone do błon retikulum endoplazmatycznego, tworząc tzw. siateczkę szorstką. Wolne rybosomy syntetyzują głównie białka działające wewnątrz cytoplazmy lub kierowane do jądra. Związane z retikulum produkują białka przeznaczone do wydzielania, wbudowania w błony komórkowe lub do lizosomów. Dodatkowo, osobne rybosomy znajdują się w mitochondriach i chloroplastach, gdzie uczestniczą w lokalnej syntezie białek organellowych.
Dlaczego rybosom uważany jest za rybozym?
Kluczowa aktywność katalityczna rybosomu, czyli tworzenie wiązań peptydowych pomiędzy aminokwasami, jest realizowana przez rybosomalne RNA znajdujące się w dużej podjednostce, a nie przez białka. Oznacza to, że rRNA pełni funkcję katalizatora reakcji chemicznej, co klasyfikuje je jako rybozym. Białka rybosomalne stabilizują strukturę kompleksu i uczestniczą w regulacji, ale sam rdzeń aktywny ma naturę RNA. To odkrycie wsparło koncepcję świata RNA w badaniach nad początkiem życia.
Jak powstają rybosomy w komórce?
Biogeneza rybosomów jest złożonym procesem zachodzącym głównie w jąderku u eukariontów. Tam transkrybowane są geny rRNA, a następnie RNA jest modyfikowane chemicznie i łączone z białkami rybosomalnymi importowanymi z cytoplazmy. Tworzą się prekursory podjednostek, które po dojrzewaniu są transportowane przez pory jądrowe do cytoplazmy. W cytoplazmie podjednostki łączą się w funkcjonalne rybosomy. U prokariontów cały proces odbywa się w cytoplazmie, lecz również wymaga precyzyjnej koordynacji wielu etapów.
W jaki sposób antybiotyki wpływają na rybosomy?
Wiele antybiotyków wiąże się z określonymi miejscami na rybosomach bakteryjnych, hamując różne fazy translacji. Tetracykliny blokują przyłączanie tRNA do miejsca A, makrolidy zakłócają przesuwanie mRNA i powstawanie łańcucha peptydowego, a aminoglikozydy zwiększają częstość błędów w odczytywaniu kodonów. Dzięki różnicom między rybosomami 70S bakterii a 80S eukariontów leki te są względnie selektywne. Jednak mutacje w rRNA lub białkach rybosomalnych mogą prowadzić do oporności, utrudniając leczenie zakażeń.