Synapsa jest jednym z najbardziej fascynujących elementów układu nerwowego, ponieważ właśnie w tym mikroskopijnym miejscu dochodzi do przekazywania informacji między komórkami nerwowymi. Zrozumienie, czym jest synapsa, jak powstaje i jak działa, stanowi klucz do wyjaśnienia mechanizmów pamięci, uczenia się, emocji, a także wielu chorób neurologicznych i psychiatrycznych. Wiedza o synapsach łączy w sobie osiągnięcia neurobiologii, biofizyki, biochemii oraz medycyny, tworząc niezwykle dynamiczny obszar współczesnej nauki.
Budowa i rodzaje synaps
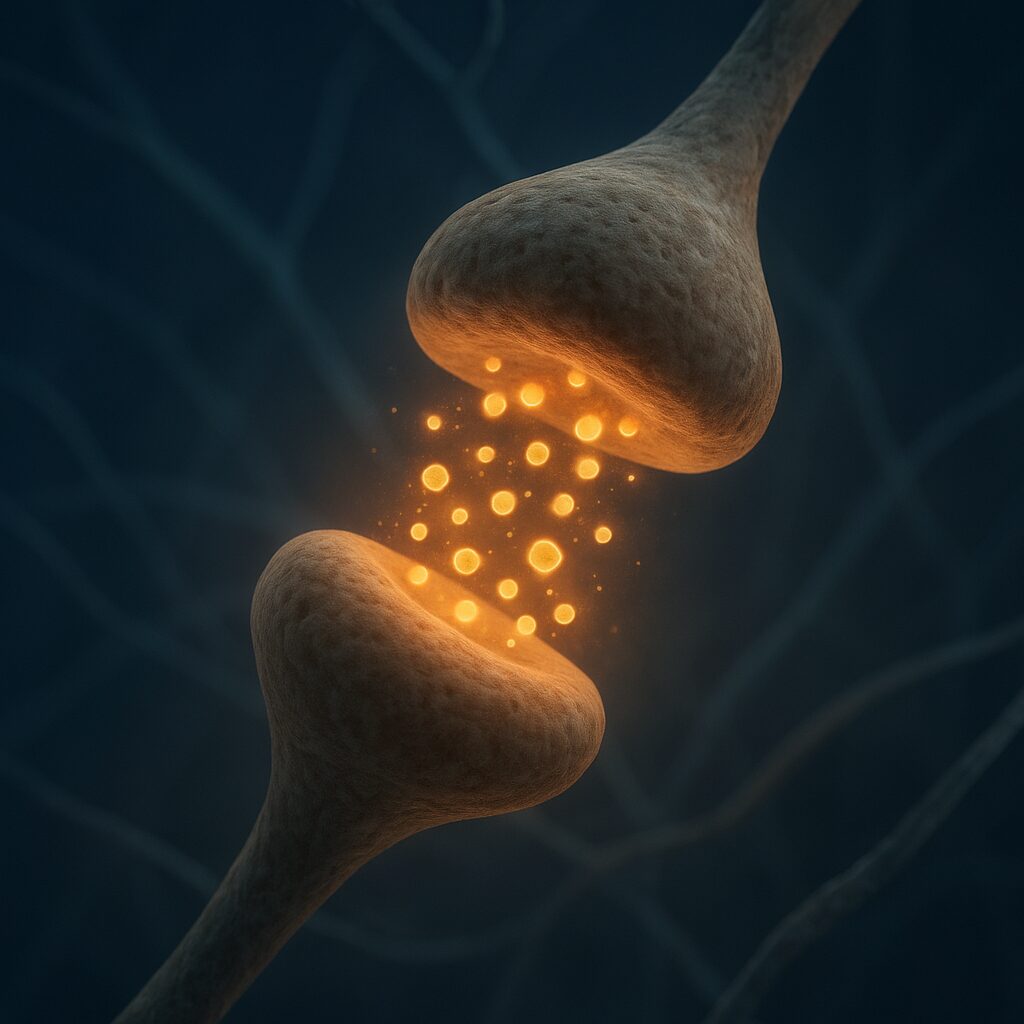
Synapsa to specjalistyczne połączenie pomiędzy dwiema komórkami: najczęściej między dwiema neuronami, ale też między neuronem a komórką mięśniową czy gruczołową. Strukturalnie wyróżnia się zakończenie presynaptyczne, szczelinę synaptyczną oraz element postsynaptyczny. Każdy z tych komponentów pełni inną funkcję, a ich współdziałanie pozwala układowi nerwowemu na szybkie i selektywne przekazywanie sygnałów.
W zakończeniu presynaptycznym znajdują się pęcherzyki synaptyczne wypełnione neuroprzekaźnikami, czyli substancjami chemicznymi odpowiedzialnymi za przeniesienie informacji. Błona presynaptyczna obfituje w kanały jonowe wrażliwe na zmiany napięcia elektrycznego. Dzięki nim impuls nerwowy docierający do zakończenia aksonu może zostać przekształcony na sygnał chemiczny. To właśnie ta konwersja – z natury elektrycznej na chemiczną – jest jednym z najważniejszych aspektów funkcjonowania synaps chemicznych.
Szczelina synaptyczna to bardzo wąska przestrzeń (rzędu kilkudziesięciu nanometrów) oddzielająca błonę presynaptyczną od postsynaptycznej. Choć zdaje się tylko „pustą przerwą”, w rzeczywistości jest środowiskiem dynamicznym, w którym neuroprzekaźnik szybko dyfunduje, a następnie jest usuwany, by nie doprowadzić do nadmiernej stymulacji. Z uwagi na rozmiar tej przestrzeni i właściwości fizykochemiczne cząsteczek, czas przejścia sygnału chemicznego przez szczelinę synaptyczną jest niezwykle krótki, co gwarantuje wysoką prędkość komunikacji w sieci neuronalnej.
Po drugiej stronie znajduje się błona postsynaptyczna, wyposażona w wyspecjalizowane receptory. To one „rozpoznają” określony neuroprzekaźnik i po jego związaniu inicjują szereg reakcji wewnątrz komórki odbiorczej. Receptory mogą być kanałami jonowymi otwieranymi przez ligand lub białkami sprzężonymi z białkami G, które wywołują bardziej złożone kaskady sygnałowe. Od typu receptorów zależy, czy synapsa będzie działać pobudzająco, czy hamująco na komórkę postsynaptyczną.
Najczęściej dzieli się synapsy na chemiczne i elektryczne. Synapsy chemiczne, dominujące w ośrodkowym układzie nerwowym kręgowców, wykorzystują neuroprzekaźniki jako nośnik informacji. Synapsy elektryczne są oparte na połączeniach szczelinowych (gap junctions), przez które bezpośrednio przepływają jony i małe cząsteczki. Dzięki temu przekaz jest niemal natychmiastowy i często dwukierunkowy. Synapsy elektryczne występują na przykład w niektórych obwodach odruchowych oraz w sieciach neuronów odpowiedzialnych za skoordynowane wyładowania, jak w jądrach pnia mózgu czy siatkówce.
Innym ważnym kryterium klasyfikacji jest typ kontaktujących się komórek. Mówimy o synapsach nerwowo-nerwowych, nerwowo-mięśniowych oraz nerwowo-gruczołowych. Synapsa nerwowo-mięśniowa, zwana płytką motoryczną, jest miejscem, w którym neuron ruchowy przekazuje sygnał do włókna mięśniowego, inicjując jego skurcz. W tym przypadku głównym neuroprzekaźnikiem jest acetylocholina, a wysoka precyzja działania synapsy jest kluczowa dla prawidłowej kontroli ruchów.
Mechanizm przewodzenia sygnału w synapsie
Proces przekazywania informacji w synapsie chemicznej rozpoczyna się, gdy potencjał czynnościowy dociera do zakończenia presynaptycznego neuronu. Zmiana napięcia błony aktywuje napięciozależne kanały wapniowe. Napływ jonów wapnia do wnętrza zakończenia jest sygnałem do fuzji pęcherzyków synaptycznych z błoną presynaptyczną. Białka odpowiedzialne za dokowanie i łączenie pęcherzyków, w tym kompleksy SNARE, umożliwiają bardzo szybkie uwolnienie neuroprzekaźnika do szczeliny synaptycznej.
Po uwolnieniu cząsteczki neuroprzekaźnika zaczynają dyfundować w kierunku błony postsynaptycznej. Tam, na specyficznych miejscach wiążących, czekają receptory o wysokim powinowactwie do danego liganda. Związanie neuroprzekaźnika z receptorem powoduje otwarcie kanałów jonowych lub uruchomienie wtórnych przekaźników wewnątrz komórki. W efekcie do wnętrza neuronu postsynaptycznego napływają określone jony (np. sodu, wapnia) lub z niego wypływają (np. potasu, chlorku), co zmienia jego potencjał błonowy.
Jeśli dominującym efektem działania synapsy jest depolaryzacja, mówimy o pobudzającym potencjale postsynaptycznym (EPSP). Gdy przeważa hiperpolaryzacja, czyli zwiększenie ujemnego ładunku wewnątrz komórki, powstaje hamujący potencjał postsynaptyczny (IPSP). Pojedyncza synapsa zazwyczaj generuje niewielką zmianę potencjału, ale plastyczność sieci neuronalnej polega na tym, że neuron integruje sygnały z setek lub tysięcy synaps jednocześnie. Dopiero suma tych pobudzeń i hamowań decyduje, czy zostanie wygenerowany nowy potencjał czynnościowy.
Bardzo istotnym etapem w funkcjonowaniu synapsy jest zakończenie działania neuroprzekaźnika. Gdyby cząsteczki pozostały długo w szczelinie synaptycznej, komórka postsynaptyczna byłaby ciągle pobudzona lub hamowana, co uniemożliwiłoby precyzyjne sterowanie informacją. Organizmy wykształciły kilka mechanizmów szybkiego „wyłączania” sygnału. Po pierwsze, neuroprzekaźnik może być rozkładany przez wyspecjalizowane enzymy, jak acetylocholinesteraza w synapsach cholinergicznych. Po drugie, istnieje wychwyt zwrotny, czyli aktywny transport neuroprzekaźnika z powrotem do zakończenia presynaptycznego lub komórek glejowych.
Wychwyt zwrotny odgrywa szczególną rolę w regulacji transmisji w synapsach z udziałem serotoniny, dopaminy czy noradrenaliny. Zahamowanie tego procesu przez leki – na przykład selektywne inhibitory wychwytu zwrotnego serotoniny – zwiększa stężenie neuroprzekaźnika w szczelinie synaptycznej, co wzmacnia przekazywany sygnał i może prowadzić do poprawy nastroju u osób z depresją. Jest to klasyczny przykład, jak wiedza o mechanizmach synaptycznych przekłada się na praktykę kliniczną i rozwój nowoczesnych terapii farmakologicznych.
W synapsach elektrycznych mechanizm przekazywania sygnału jest odmienny i opiera się na bezpośrednim przepływie prądu jonowego przez kanały tworzone przez koneksony. Dwie sąsiadujące komórki są połączone szeregiem takich kanałów, które ustalają niskooporową drogę dla jonów. Potencjał czynnościowy w jednej komórce może wówczas bez zwłoki powodować lokalne zmiany napięcia w sąsiedniej. Przekaz jest tu szybszy niż w synapsie chemicznej, ale też mniej plastyczny – trudniej o subtelne modulacje siły połączenia.
Synapsa a uczenie się i pamięć
Jednym z fundamentalnych pytań neurobiologii jest: jak układ nerwowy koduje doświadczenia i zamienia je w trwałe ślady pamięciowe? Kluczem do odpowiedzi okazała się właśnie synapsa. Już w połowie XX wieku Donald Hebb zaproponował, że jeśli dwa neurony są aktywne jednocześnie, to połączenie między nimi ulega wzmocnieniu. Takie „uczenie hebbowskie” zakłada, że częste, skorelowane pobudzenie sprzyja trwałej zmianie właściwości synapsy. Dziś wiadomo, że długotrwałe wzmocnienie synaptyczne (LTP) i długotrwałe osłabienie synaptyczne (LTD) są podstawowymi mechanizmami leżącymi u podłoża pamięci i uczenia się.
W LTP powtarzająca się, intensywna stymulacja synapsy glutaminergicznej prowadzi do zwiększenia odpowiedzi postsynaptycznej. Dzieje się tak między innymi dzięki receptorom NMDA, które są wrażliwe zarówno na obecność glutaminianu, jak i na poziom depolaryzacji błony postsynaptycznej. Gdy oba warunki zostaną spełnione, receptor przepuszcza jony wapnia, uruchamiając kaskadę procesów wewnątrzkomórkowych. W efekcie zwiększa się liczba receptorów AMPA w błonie postsynaptycznej, zmienia się struktura kolców dendrytycznych, a synapsa staje się silniejsza.
Odwrotnym zjawiskiem jest LTD, czyli długotrwałe osłabienie synaptyczne, występujące przy słabszych, ale częstszych pobudzeniach lub przy specyficznym wzorcu aktywności. Zmniejszenie odpowiedzi postsynaptycznej wiąże się na przykład z internalizacją części receptorów AMPA lub zmianą właściwości białek sygnałowych. Choć na pierwszy rzut oka osłabianie synaps może wydawać się niekorzystne, w rzeczywistości jest kluczowe dla plastyczności sieci. Bez LTD mózg byłby „przeciążony” stale rosnącą liczbą wzmocnionych połączeń, co uniemożliwiałoby selekcję informacji i adaptację do nowych warunków.
Synapsy są również plastyczne strukturalnie. Oznacza to, że z czasem mogą powstawać nowe kontakty synaptyczne, istniejące mogą się rozgałęziać lub zanikać. Neuroobrazowanie oraz badania histologiczne pokazały, że doświadczenie, takie jak nauka nowej umiejętności, zmienia gęstość kolców dendrytycznych w określonych obszarach mózgu. Mechanizmy molekularne tej strukturalnej plastyczności obejmują regulację ekspresji genów, syntezę białek cytoszkieletu i cząsteczek adhezyjnych, a także działania czynników troficznych.
Plastyczność synaptyczna leży także u podstaw zjawisk patologicznych, takich jak uzależnienia. W przypadku przewlekłego narażenia na substancje psychoaktywne, jak kokaina czy alkohol, dochodzi do głębokich zmian w synapsach dopaminergicznych w układzie nagrody. Zmienia się liczba receptorów, siła połączeń oraz dynamika uwalniania neuroprzekaźników. Te adaptacje powodują, że mózg „uczy się” reagować w specyficzny sposób na daną substancję, co prowadzi do silnego przymusu jej przyjmowania i trudności w przerwaniu nałogu.
Plastyczność synaptyczna jest również kluczowa w procesie rehabilitacji po uszkodzeniach mózgu, na przykład po udarze. Utracone funkcje nie są zwykle w pełni odtwarzane przez regenerację dokładnie tych samych połączeń, lecz poprzez reorganizację istniejących sieci. Sąsiadujące obszary mogą przejmować funkcje uszkodzonego regionu, tworząc nowe synapsy i wzmacniając alternatywne drogi przewodzenia impulsów. Rehabilitacja ruchowa czy terapia mowy opierają się właśnie na stymulowaniu takich korzystnych zmian plastycznych.
Synapsa w zdrowiu i chorobie
Synapsy odgrywają kluczową rolę nie tylko w codziennym funkcjonowaniu mózgu, ale także w rozwoju wielu chorób neurologicznych i psychicznych. Zmiany w ilości, strukturze lub funkcji synaps są obserwowane w zaburzeniach spektrum autyzmu, schizofrenii, chorobie Alzheimera, padaczce, a także w zaburzeniach lękowych i depresyjnych. Szeroka gama białek synaptycznych – od receptorów i kanałów jonowych, po białka kotwiczące i transportery – może podlegać mutacjom genetycznym lub dysregulacji, co zakłóca prawidłowe przekazywanie sygnałów w mózgu.
W chorobie Alzheimera jednym z wczesnych objawów na poziomie komórkowym jest utrata synaps, zanim jeszcze dojdzie do znacznej śmierci neuronów. Białka patologiczne, takie jak beta-amyloid i tau, zaburzają funkcjonowanie synaps glutaminergicznych i cholinergicznych, prowadząc do stopniowego zanikania plastyczności i deficytów pamięci. Obecnie wiele badań koncentruje się na ochronie synaps przed uszkodzeniem oraz na próbach przywrócenia funkcji synaptycznych poprzez modulowanie aktywności receptorów lub usuwanie toksycznych agregatów białkowych.
W padaczce, szczególnie ogniskowej, obserwuje się nadmierną synchronizację aktywności neuronów w danym rejonie mózgu. Przyczyną może być zaburzenie równowagi między synapsami pobudzającymi a hamującymi. Jeśli synapsy GABA-ergiczne (hamujące) są osłabione lub synapsy glutaminergiczne (pobudzające) nadmiernie aktywne, sieć neuronalna staje się podatna na generowanie niekontrolowanych wyładowań. Terapie przeciwpadaczkowe często celują w przywrócenie tej równowagi, modulując funkcję kanałów jonowych lub zwiększając transmisję hamującą.
Synapsy są także głównym celem wielu leków psychotropowych. Leki przeciwdepresyjne, przeciwpsychotyczne, przeciwlękowe czy stabilizujące nastrój wpływają na stężenia neuroprzekaźników, ich wychwyt, degradację lub wrażliwość receptorów. Na przykład leki przeciwpsychotyczne moduluje transmisję dopaminergiczną w określonych szlakach mózgowych, co może łagodzić objawy psychozy, ale też powodować działania niepożądane związane z ruchem. Zrozumienie, jakie synapsy są modulowane przez określony lek, pozwala przewidywać jego działanie oraz projektować środki o bardziej selektywnym profilu.
Nie można pominąć roli komórek glejowych, takich jak astrocyty i mikroglej, w utrzymaniu zdrowych synaps. Astrocyty regulują skład jonowy środowiska zewnątrzkomórkowego, uczestniczą w wychwycie zwrotnym neuroprzekaźników i wydzielają czynniki troficzne. Mikroglej odpowiada za „przycinanie” nadmiarowych synaps w rozwoju mózgu, a także za reakcję na uszkodzenie. Zaburzenia tych procesów mogą prowadzić do nieprawidłowego kształtowania się sieci synaptycznych lub do nadmiernej utraty połączeń, co z kolei skutkuje deficytami poznawczymi i behawioralnymi.
W ostatnich latach pojawiła się koncepcja synaptopatii – chorób, których wspólnym mianownikiem są pierwotne defekty synaptyczne. Do tej grupy zalicza się część zaburzeń neurorozwojowych oraz ustalone genetycznie formy padaczki. Identyfikacja mutacji w genach kodujących białka synaptyczne umożliwia coraz bardziej szczegółową klasyfikację tych schorzeń i otwiera drogę do terapii ukierunkowanych molekularnie. Na przykład modulacja działania określonych receptorów lub przywracanie prawidłowej struktury białek za pomocą terapii genowych staje się realnym celem badań klinicznych.
Znaczenie synaps w badaniach naukowych i technologii
Synapsy znajdują się w centrum zainteresowania współczesnej neurobiologii nie tylko dlatego, że umożliwiają komunikację neuronów, ale także dlatego, że inspirują nowe rozwiązania technologiczne. Jednym z dynamicznie rozwijających się obszarów jest neuromorficzne przetwarzanie informacji, czyli tworzenie układów elektronicznych wzorowanych na strukturze i funkcji mózgu. Elementy takie jak memrystory są projektowane tak, aby naśladować właściwości plastyczne synaps, zmieniając swoją przewodność w odpowiedzi na przepływ prądu. Dzięki temu możliwe jest budowanie sztucznych sieci, które uczą się w sposób zbliżony do biologicznych.
Badania nad synapsami korzystają z zaawansowanych metod obrazowania, takich jak mikroskopia superrozdzielcza, która pozwala wizualizować pojedyncze białka w obrębie specjalizacji synaptycznych. Dzięki tej technologii naukowcy mogą śledzić, jak zmienia się rozmieszczenie receptorów po stymulacji, jak reorganizuje się cytoszkielet w kolcach dendrytycznych oraz jak dochodzi do formowania się nowych połączeń. Połączenie mikroskopii z metodami elektrofizjologicznymi, jak patch-clamp, daje wyjątkowo pełny obraz funkcji synapsy na poziomie molekularnym i biofizycznym.
W dziedzinie medycyny personalizowanej coraz większe znaczenie ma analiza indywidualnych różnic w funkcjonowaniu synaps. Polimorfizmy genetyczne w genach kodujących receptory, transportery czy enzymy związane z synapsą mogą wpływać na reakcję pacjenta na leki, ryzyko wystąpienia działań niepożądanych oraz podatność na określone choroby. Rozwój sekwencjonowania genomu i technik edycji, takich jak CRISPR-Cas9, umożliwia modelowanie złożonych zaburzeń synaptycznych w organizmach zwierzęcych i komórkach pochodzących od pacjentów.
Synapsy są także kluczowym elementem badań nad świadomością i złożonymi stanami psychicznymi. Chociaż nie ma prostego „receptora świadomości”, to dynamika aktywności w sieciach synaptycznych decyduje o tym, jakie treści są aktualnie reprezentowane w mózgu. Za pomocą technik neuroobrazowania, takich jak fMRI czy EEG, można śledzić wzorce aktywności w dużych sieciach neuronalnych, ale to na poziomie synaptycznym decyduje się, które połączenia zostają wzmocnione, a które wygasają.
Interesującym kierunkiem jest również badanie wpływu stylu życia na funkcjonowanie synaps. Aktywność fizyczna, dieta, sen i poziom stresu modulują produkcję czynników neurotroficznych, takich jak BDNF, które wpływają na przeżycie neuronów i plastyczność synaptyczną. Regularny wysiłek fizyczny sprzyja powstawaniu nowych synaps w hipokampie, co koreluje z lepszą pamięcią i odpornością na stres. Z kolei przewlekły stres i brak snu mogą upośledzać plastyczność, prowadząc do problemów poznawczych i zwiększonego ryzyka zaburzeń nastroju.
Rozwój technologii pozwala także na coraz bardziej precyzyjną stymulację i modulację aktywności synaptycznej. Przykładem jest optogenetyka, w której światłoczułe białka wbudowane w błony neuronów pozwalają na kontrolę ich pobudliwości za pomocą światła. Dzięki temu można badać, jak konkretny typ synaps w wybranym obwodzie mózgowym wpływa na zachowanie zwierzęcia. Tego rodzaju eksperymenty stanowią potężne narzędzie do odkrywania przyczynowo-skutkowych relacji między aktywnością synaptyczną a złożonymi funkcjami poznawczymi.
FAQ – najczęstsze pytania o synapsy
Co to jest synapsa w prostych słowach?
Synapsa to miejsce kontaktu między dwiema komórkami, najczęściej neuronami, w którym przekazywana jest informacja. Jeden neuron wysyła sygnał, uwalniając cząsteczki zwane neuroprzekaźnikami, a drugi go odbiera za pomocą wyspecjalizowanych receptorów. Dzięki synapsom komórki nerwowe mogą tworzyć ogromne sieci, odpowiedzialne za nasze myśli, emocje, ruchy i pamięć. Bez synaps mózg nie byłby w stanie komunikować się wewnętrznie ani z resztą organizmu.
Jaka jest różnica między synapsą chemiczną a elektryczną?
W synapsie chemicznej sygnał przekazywany jest za pomocą substancji chemicznych, czyli neuroprzekaźników, które uwalniane są do szczeliny synaptycznej i wiążą się z receptorami na komórce odbiorczej. Przekaz jest jednokierunkowy i wolniejszy, ale umożliwia precyzyjną regulację i plastyczność. W synapsie elektrycznej komórki połączone są kanałami białkowymi, przez które bezpośrednio przepływają jony, co daje bardzo szybki, często dwukierunkowy sygnał, lecz o mniejszych możliwościach modulacji.
W jaki sposób synapsy są związane z pamięcią?
Pamięć opiera się na trwałych zmianach w sile i liczbie synaps. Gdy wielokrotnie uczymy się tej samej informacji, określone połączenia między neuronami ulegają wzmocnieniu (LTP), co zwiększa prawdopodobieństwo ich wspólnej aktywacji w przyszłości. Inne, mniej używane synapsy mogą się osłabiać (LTD) lub zanikać. W ten sposób mózg selekcjonuje ważne doświadczenia i utrwala je jako ślady pamięciowe. Strukturalne modyfikacje synaps, jak zmiany w kolcach dendrytycznych, to fizyczna podstawa zapamiętywania.
Jakie choroby są związane z zaburzeniami synaps?
Nieprawidłowe funkcjonowanie synaps, zwłaszcza zaburzenia w liczbie, budowie lub aktywności receptorów i neuroprzekaźników, występują w wielu schorzeniach. W chorobie Alzheimera obserwuje się wczesną utratę synaps i osłabienie plastyczności, co prowadzi do problemów z pamięcią. W padaczce dochodzi do zachwiania równowagi między synapsami pobudzającymi i hamującymi. Zaburzenia spektrum autyzmu, schizofrenia czy depresja wiążą się z mutacjami genów synaptycznych lub dysregulacją transmisji chemicznej w określonych obwodach mózgowych.
Czy można wpływać na synapsy poprzez styl życia?
Na funkcjonowanie synaps znacząco oddziałują codzienne nawyki. Regularna aktywność fizyczna zwiększa poziom czynników neurotroficznych, sprzyjając powstawaniu nowych połączeń i poprawie pamięci. Odpowiedni sen jest konieczny do konsolidacji śladów pamięciowych i „porządkowania” sieci synaptycznych. Dieta bogata w kwasy tłuszczowe omega-3 i antyoksydanty wspiera zdrowie neuronów, natomiast przewlekły stres i używki mogą upośledzać plastyczność synaptyczną, zwiększając podatność na zaburzenia nastroju i deficyty poznawcze.