Wiązanie koordynacyjne jest jednym z kluczowych pojęć współczesnej chemii, mimo że często bywa pomijane w prostych opisach budowy materii. Dzięki niemu można wyjaśnić strukturę wielu jonów metali, barwę roztworów, działanie katalizatorów przemysłowych, a nawet funkcjonowanie białek niezbędnych do życia, takich jak hemoglobina. Zrozumienie istoty tego typu wiązania pozwala połączyć wiedzę z zakresu chemii nieorganicznej, fizycznej, analitycznej i biochemii w spójny obraz opisujący zachowanie atomów i cząsteczek w różnorodnych środowiskach.
Istota wiązania koordynacyjnego
Wiązanie koordynacyjne, nazywane także wiązaniem donorowo–akceptorowym, jest szczególnym przypadkiem wiązania kowalencyjnego. Różni się od klasycznego wiązania kowalencyjnego tym, że obie wspólne elektrony w parze pochodzą od jednego z atomów – donora. Drugi atom, nazywany akceptorem, dysponuje pustą powłoką lub orbitalem, na którym może przyjąć tę parę elektronową. Gdy para zostanie udostępniona, między atomami powstaje wspólna chmura elektronowa, a więc wiązanie, które ma w dużej mierze charakter kowalencyjny, choć opisuje się je w inny sposób formalny.
W szczególności jon lub atom pełniący funkcję akceptora – najczęściej jest to kation metalu przejściowego – tworzy tak zwany kompleks koordynacyjny z cząsteczkami lub jonami otaczającymi go w przestrzeni. Te cząsteczki lub jony, określane mianem ligandów, udostępniają swoje wolne pary elektronowe do utworzenia wiązań koordynacyjnych. Każde takie wiązanie można przedstawić symbolicznie strzałką skierowaną od liganda do centrum metalicznego, co podkreśla kierunek przepływu pary elektronowej.
Z formalnego punktu widzenia wiązanie koordynacyjne nie różni się energią ani długością od zwykłego wiązania kowalencyjnego tego samego typu. Gdy już powstanie, obserwowalne właściwości – takie jak odległość między atomami czy energia dysocjacji – zależą od natury uczestniczących w nim atomów i otoczenia, a nie od tego, z którego z atomów początkowo pochodziły elektrony. Różnica ma charakter przede wszystkim opisowy i jest wygodna przy analizowaniu budowy związków kompleksowych.
Kluczowym parametrem opisującym centrum metaliczne w kompleksie jest tak zwana liczba koordynacyjna, czyli liczba wiązań koordynacyjnych tworzących bezpośrednie otoczenie metalu. Typowe wartości to 4 lub 6, choć znane są kompleksy o liczbach koordynacyjnych od 2 do 12. Liczba koordynacyjna zależy od wielkości jonu metalu, jego ładunku oraz przestrzennej budowy i powinowactwa ligandów. To właśnie ona determinuje podstawową geometrię kompleksu: oktaedryczną, tetraedryczną, kwadratowo–płaską czy liniową.
Ligandy i geometria kompleksów koordynacyjnych
Ligand to cząsteczka lub jon zawierający co najmniej jedną wolną parę elektronową, zdolną do utworzenia wiązania z centrum metalicznym. Może to być prosty jon, jak Cl⁻, cząsteczka wody H₂O, amoniaku NH₃ lub bardziej złożony związek organiczny, jak etylenodiamina czy porfiryny. W zależności od liczby miejsc przyłączenia do metalu mówimy o ligandach monodentatowych (jedno zębowych), bidentatowych (dwuzębowych) oraz polidentatowych. Ligandy polidentatowe są podstawą zjawiska chelatacji, które stabilizuje kompleks poprzez utworzenie pierścieni z atomem metalu w środku.
Najprostszym przykładem liganda monodentatowego jest woda. Każda cząsteczka H₂O posiada dwie wolne pary elektronowe na atomie tlenu, lecz zwykle w prostych kompleksach używa jednej z nich do utworzenia wiązania koordynacyjnego. W jonach metali, takich jak [Cu(H₂O)₆]²⁺ czy [Fe(H₂O)₆]³⁺, sześć cząsteczek wody otacza centralny jon metalu, tworząc otoczkę hydratacyjną. Tego typu struktury są typowe w roztworach wodnych i odpowiadają za barwę wielu roztworów soli metali przejściowych.
Ligandy bidentatowe, na przykład etylenodiamina (en), wiążą się z metalem za pomocą dwóch atomów donorowych – zwykle dwóch atomów azotu. Tworzą one z metalem pięcioczłonowy pierścień, który jest termodynamicznie korzystny. Stabilizacja wynikająca z tworzenia takich pierścieni nazywana jest efektem chelatowym i jest ogromnie znacząca w chemii biologicznej oraz przemysłowej. Klasycznym chelatorem jest EDTA (kwas etylenodiaminotetraoctowy), ligand heksadentatowy, zdolny do „objęcia” jonu metalu kilkoma zębami i bardzo silnego jego związania.
Geometria kompleksów zależy od liczby koordynacyjnej oraz natury liganda. Dla liczby koordynacyjnej 6 najbardziej typową geometrią jest oktaedr, w którym sześć ligandów rozmieszcza się wokół jonu metalu w wierzchołkach wyimaginowanego sześcianu. W przypadku liczby koordynacyjnej 4 możliwe są geometrie tetraedryczna lub kwadratowo–płaska. Geometria ta wynika z minimalizacji odpychania między elektronami w wiązaniach oraz z bardziej subtelnych efektów, takich jak rozdwojenie poziomów energetycznych d–orbitali metalu, opisywane przez teorię pola ligandowego.
Klasyczna teoria pola krystalicznego i bardziej zaawansowana teoria pola ligandowego tłumaczą, w jaki sposób ligandy wpływają na rozszczepienie poziomów energetycznych d–orbitali metalu. Rozszczepienie to jest źródłem charakterystycznych barw wielu kompleksów. Gdy foton światła widzialnego zostaje zaabsorbowany, elektron przechodzi między rozszczepionymi poziomami energetycznymi, a my obserwujemy kolor odpowiadający światłu odbitemu lub przepuszczonemu. Z tego powodu roztwory soli miedzi(II), chromu(III) czy niklu(II) często mają intensywne barwy, podczas gdy kompleksy z metalami bez elektronów d, jak Zn(II), bywają bezbarwne.
Oprócz geometrii pierwszej sfery koordynacyjnej istotna jest również organizacja ligandów w przestrzeni. W kompleksach oktaedrycznych mogą istnieć izomery geometryczne, na przykład cis i trans, różniące się wzajemnym ułożeniem dwóch określonych ligandów. Niekiedy możliwy jest także izomer mer i fac, opisujący, czy trzy określone ligandy leżą w jednej płaszczyźnie, czy tworzą „twarz” oktaedru. Te subtelne różnice strukturalne mogą prowadzić do odmiennych właściwości fizycznych, biologicznych i katalitycznych.
Rola wiązań koordynacyjnych w chemii i biologii
Znaczenie wiązań koordynacyjnych wykracza daleko poza klasyczną chemię nieorganiczną. Jednym z najbardziej spektakularnych przykładów jest rola jonów metali w układach biologicznych. W centrum cząsteczki hemu, składnika hemoglobiny odpowiedzialnej za transport tlenu we krwi, znajduje się jon żelaza(II) skoordynowany do makrocyklicznego liganda – porfiryny. Dodatkowe miejsca koordynacyjne zajmują atom azotu z białka globinowego oraz cząsteczka tlenu.
Wiązanie tlenu do hemoglobiny jest procesem koordynacyjnym: cząsteczka O₂ przyłącza się do centrum metalicznego, tworząc wiązanie, które można przedstawić jako donorowo–akceptorowe. Zdolność tego kompleksu do odwracalnego wiązania i uwalniania tlenu zależy od delikatnej równowagi między stopniem utlenienia żelaza, naturą liganda porfirynowego oraz otaczającym środowiskiem białkowym. Zbyt silne wiązanie unieruchomiłoby tlen, zbyt słabe uniemożliwiłoby jego efektywny transport. Ten subtelny kompromis jest wynikiem milionów lat ewolucji.
Podobne zasady rządzą funkcjonowaniem innych białek metaloproteinowych. W centrach aktywnych wielu enzymów – na przykład karbonic anhydrazy, dehydrogenaz, oksydaz czy transferaz – znajdują się jony Zn(II), Cu(II), Fe(II/III), Mn(II) lub Co(II), skoordynowane do grup aminokwasowych: imidazolowych grup histydyny, tiolowych cysteiny czy karboksylanowych asparaginianu. Zmiana konfiguracji koordynacyjnej w trakcie reakcji enzymatycznej pozwala na przyłączanie substratów, aktywację cząsteczek wody, przeprowadzanie wieloelektronowych procesów redoks i stabilizację stanów przejściowych reakcji.
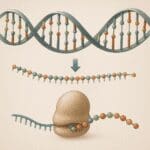
Wiązanie koordynacyjne odgrywa ważną rolę także w funkcjonowaniu kwasów nukleinowych. Jony Mg(II) i innych metali dwu– oraz trójwartościowych oddziałują koordynacyjnie z grupami fosforanowymi łańcucha DNA i RNA, stabilizując ich strukturę przestrzenną. Dzięki temu możliwe jest prawidłowe zwijanie się struktur RNA oraz działanie rybozymów i rybosomów. W wielu przypadkach metal pełni funkcję katalityczną, ułatwiając atak nukleofilowy w reakcjach fosfodiestrowych.
W chemii analitycznej wykorzystuje się ogromną selektywność i czułość oddziaływań koordynacyjnych do wykrywania śladowych ilości metali. Przykładowo, klasyczne miareczkowanie kompleksometryczne z użyciem EDTA opiera się na tworzeniu bardzo trwałego kompleksu metal–EDTA, co pozwala na precyzyjne oznaczanie stężenia jonów wapnia, magnezu, cynku i wielu innych. Zmiana barwy wskaźników metalochromowych sygnalizuje moment, w którym wszystkie jony metalu zostały związane przez ligand, umożliwiając dokładne wyznaczenie punktu równoważnikowego.
W przemyśle katalitycznym kompleksy koordynacyjne pełnią rolę centrów aktywnych wielu procesów. Katalizatory najnowszej generacji do polimeryzacji olefin – tzw. katalizatory Zieglera–Natty, kompleksy metali późnych czy katalizatory na bazie metali ziem rzadkich – działają dzięki zdolności centrum metalicznego do dynamicznej zmiany liczby koordynacyjnej i przyłączania cząsteczek monomeru. Przejściowe kompleksy koordynacyjne umożliwiają kontrolowane otwieranie i zamykanie wiązań podwójnych oraz wzrost łańcucha polimerowego z dużą precyzją stereochemiczną.
Szczególnie interesujące są kompleksy z ligandami makrocyklicznymi, takimi jak koronandowe etery, kryptandy, kaliksareny czy porfiryny syntetyczne. Tworzą one „kieszenie” o określonym rozmiarze i kształcie, zdolne do selektywnego wiązania określonych jonów lub cząsteczek. Tego typu układy stanowią podstawę chemii supramolekularnej, gdzie dzięki precyzyjnym oddziaływaniom koordynacyjnym możliwe jest tworzenie kapsuł molekularnych, receptorów, czujników oraz materiałów o zaprojektowanych właściwościach magnetycznych, luminescencyjnych czy przewodzących.
Wiązania koordynacyjne są również odpowiedzialne za toksyczność lub lecznicze działanie wielu związków metali ciężkich. Kompleks platyny – cisplatyna – jest jednym z najważniejszych leków stosowanych w terapii nowotworowej. Jej działanie polega na tworzeniu wiązań koordynacyjnych z atomami azotu w zasadach purynowych DNA, co prowadzi do powstawania mostków wewnątrz nici i między nićmi. Struktura helisy zostaje zakłócona, procesy replikacji i transkrypcji ulegają zahamowaniu, a komórka nowotworowa jest kierowana na drogę apoptozy. Z kolei toksyczność jonów metali, takich jak Pb(II) czy Hg(II), wynika w dużej mierze z ich zdolności do tworzenia silnych kompleksów z grupami tio- i amino–białek, co zaburza ich funkcję biologiczną.
FAQ – najczęściej zadawane pytania
Czym różni się wiązanie koordynacyjne od kowalencyjnego?
Wiązanie koordynacyjne jest formalnie odmianą wiązania kowalencyjnego, ponieważ w obu przypadkach powstaje wspólna para elektronowa między dwoma atomami. Różnica polega na pochodzeniu elektronów: w zwykłym wiązaniu kowalencyjnym każdy atom wnosi po jednym elektronie, natomiast w koordynacyjnym cała para pochodzi od liganda–donora. Po utworzeniu wiązania nie da się fizycznie rozróżnić, skąd pochodziły elektrony; różnica ma głównie znaczenie opisowe i księgowe.
Co to jest liczba koordynacyjna i od czego zależy?
Liczba koordynacyjna to liczba ligandów bezpośrednio związanych z atomem metalu w kompleksie, czyli liczba wiązań koordynacyjnych tworzących jego najbliższe otoczenie. Typowe wartości to 4 i 6, ale możliwe są też inne. Zależy ona od rozmiaru i ładunku jonu metalu, właściwości ligandów (wielkości, twardości, kształtu) oraz warunków środowiskowych, takich jak rozpuszczalnik czy stężenie reagentów. To właśnie liczba koordynacyjna determinuje podstawową geometrię kompleksu.
Dlaczego roztwory kompleksów metali przejściowych są barwne?
Barwa roztworów kompleksów metali przejściowych wynika z rozszczepienia poziomów energetycznych d–orbitali metalu w polu ligandów. Gdy cząsteczka absorbuje światło widzialne, elektron może przeskoczyć z niżej położonego poziomu na wyższy. Energia tego przejścia odpowiada konkretnemu zakresowi długości fali, z którego światło jest pochłaniane. Kolor, który widzimy, to wypadkowa fal niezaabsorbowanych, a więc światła odbitego lub przenikającego przez roztwór.
Na czym polega efekt chelatowy?
Efekt chelatowy to zwiększona trwałość kompleksów, w których metal jest związany ligandami polidentatowymi, tworzącymi pierścieniowe struktury z atomem metalu w środku. Gdy ligand ma kilka zębów donorowych, przyłączenie go do metalu prowadzi do powstania kilku wiązań jednocześnie, a rozerwanie kompleksu wymaga równoczesnego rozerwania wszystkich tych interakcji. Efekt ten ma podłoże termodynamiczne – wiąże się m.in. ze wzrostem entropii roztworu i lepszym dopasowaniem przestrzennym liganda do jonu metalu.
Jakie znaczenie ma wiązanie koordynacyjne w organizmach żywych?
Wiązania koordynacyjne są niezbędne w biologii, ponieważ umożliwiają funkcjonowanie wielu białek i enzymów zawierających jony metali. W hemoglobinie koordynacja Fe(II) do porfiryny i tlenu umożliwia transport O₂. W enzymach, takich jak karbonic anhydraza czy dehydrogenazy, metale aktywują cząsteczki wody, uczestniczą w reakcjach redoks i stabilizują stany przejściowe. Jony Mg(II) i inne stabilizują struktury DNA i RNA, wpływając na ich własności katalityczne oraz zdolność do specyficznych oddziaływań z białkami.